名校
解题方法
1 . Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为4Li+2SOCl2=4LiCl+S+SO2。请回答下列问题:
(1)电池的负极材料为_____ ,发生的电极反应为______________ 。
(2)电池正极发生的电极反应为_______________ 。
(1)电池的负极材料为
(2)电池正极发生的电极反应为
您最近一年使用:0次
名校
解题方法
2 . 最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH) 下列说法正确的是( )
| A.该电池Zn为负极,ZnO为正极,MnO2为催化剂 |
| B.该电池的正极反应为:MnO2+e-+H2O=MnO(OH)+OH- |
| C.导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| D.电池工作时OH-能通过薄层纸片向附着二氧化锰的电极移动。 |
您最近一年使用:0次
2020-01-16更新
|
289次组卷
|
5卷引用:湖北省随州市曾都一中2019-2020学年高一下学期期末考试化学试题
湖北省随州市曾都一中2019-2020学年高一下学期期末考试化学试题(已下线)2014届浙江省衢州一中高三上学期期中考试化学试卷新疆生产建设兵团第二中学2016-2017学年高一下学期第二次月考化学试题黑龙江省大庆市第十中学2019-2020学年高二上学期期末考试化学试题(已下线)第04章 电化学基础(A卷基础篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)
名校
3 . 2019年度诺贝尔化学奖授予研究锂离子电池的三位化学家,以表彰他们在锂离子电池发展方面所做出的突出贡献。锂锰电池是一种常用的锂离子电池,它体积小、性能优良,该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2,下列说法错误的是( )


| A.外电路的电流方向是由b极流向a极 |
| B.电池正极反应式为MnO2+e-+Li+=LiMnO2 |
| C.可用水代替电池中的混合有机溶剂 |
| D.电路中每通过1mol电子,就有NA个Li+移向b极 |
您最近一年使用:0次
2020-01-16更新
|
191次组卷
|
3卷引用:湖北省荆门市2019-2020学年高二上学期期末学业水平选择性考试阶段性检测化学试题
解题方法
4 . 下列实验操作、现象与结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 用铂蘸取某碱金属的盐溶液刻灼烧 | 火焰呈紫色 | 证明其中含有K+ |
| B | 向CuSO4溶液中通入H2S气体 | 出现黑色沉淀 | 酸性:H2S>H2SO4 |
| C | 将等浓度等体积的KI溶液和 FeC13溶液混合,充分反应后 滴入KSCN溶液 | 溶液变红 | 溶液中存在平衡: 2Fe3++2I-  2Fe2++I2 2Fe2++I2 |
| D | 用稀硫酸和锌粒制取H2时, 加几滴CusO4溶液 | 反应速率加快 | CuSO4是该反应的催化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-01-09更新
|
302次组卷
|
2卷引用:湖北省荆门市2019—2020学年高三上学期元月调研考试理综化学试题
5 . 美国科学家JohnB.Goodenough荣获2019年诺贝尔化学奖,他指出固态体系锂电池是锂电池未来发展方向。Kumar等人首次研究了固态可充电、安全性能优异的锂空气电池,其结构如图所示。已知单位质量的电极材料放出电能的大小称为电池的比能量。下列说法错误的是( )


| A.a极反应为“Li-e-=Li+,b极发生还原反应 |
| B.充电时,Li+由a极通过固体电解液向b极移动 |
| C.电路中转移4mol电子,大约需要标准状况下112L空气 |
| D.与铅蓄电池相比,该电池的比能量大 |
您最近一年使用:0次
名校
6 . 锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示。下列说法正确的是


| A.电解液中,Li+由多孔电极迁移向锂电极 |
| B.该电池放电时,负极发生了还原反应 |
| C.充电时,电池正极的反应式为Li2O2-2e-=2Li++O2↑ |
| D.电池中的电解液可以是有机电解液或稀盐酸等 |
您最近一年使用:0次
2019-12-24更新
|
937次组卷
|
6卷引用:湖北省黄冈市浠水县实验高级中学2019-2020学年高二上学期9月份月考化学试题
湖北省黄冈市浠水县实验高级中学2019-2020学年高二上学期9月份月考化学试题福建省泉州市2018届普通高中高三单科质量检查化学试题人教版高中化学(2019)必修第二册第六章《化学反应与能量》检测题黑龙江省哈尔滨市第三十二中学2020-2021学年高二上学期期末考试化学试题(已下线)专题08 电化学(化学电源、离子交换膜电池、信息类电化学等)-2021年高考化学必做热点专题黑龙江省牡丹江市第二高级中学2023-2024学年高二上学期1月期末化学试题
7 . 火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会对环境造成严重影响。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。
利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为________________ 。
(2)脱碳。
将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后 ,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图所示,则上述CO2转化为甲醇的反应热△H3_____ 0(填“>”、“<”或“=”),该反应的平衡常数表达式为_______________ 。
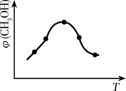
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图所示,试回答:
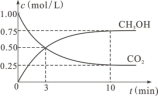
0~10 min内,氢气的平均反应速率为___________________ mol/(L·min)。第10 min后,若向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时CH3OH(g)的体积分数____________ (填“增大”、“减小”或“不变”,下同),反应的平衡常数_____________________ 。
(3)脱硫。
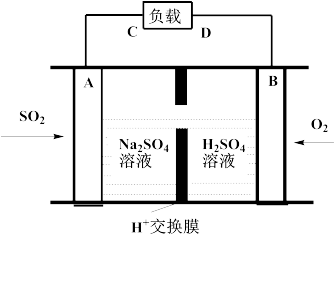
①有学者想利用如图所示装置用原电池原理将SO2转化为重要的化工原料。A、B是惰性电极,A极的电极反应式为:_________ 。
②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。常温下,将NH4NO3 溶解于水中,为了使该溶液中的NH4+ 和 NO3-离子的物质的量浓度之比等于1 : 1,可以采取的正确措施为_________ 。
A.加入适量的硝酸,抑制 NH4+的水解
B.加入适量的氨水,使溶液的 PH = 7
C.加入适量的 NaOH 溶液,使溶液的PH = 7
D.加入适量的NH4NO3
(1)脱硝。
利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为
(2)脱碳。
将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3①取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应

②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图所示,试回答:

0~10 min内,氢气的平均反应速率为
(3)脱硫。
①有学者想利用如图所示装置用原电池原理将SO2转化为重要的化工原料。A、B是惰性电极,A极的电极反应式为:

②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。常温下,将NH4NO3 溶解于水中,为了使该溶液中的NH4+ 和 NO3-离子的物质的量浓度之比等于1 : 1,可以采取的正确措施为
A.加入适量的硝酸,抑制 NH4+的水解
B.加入适量的氨水,使溶液的 PH = 7
C.加入适量的 NaOH 溶液,使溶液的PH = 7
D.加入适量的NH4NO3
您最近一年使用:0次
13-14高三·湖北孝感·阶段练习
名校
8 . 我国某知名企业开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其他电池,电池总反应为V2O5+xLi LixV2O5。下列说法中正确的是( )
LixV2O5。下列说法中正确的是( )
 LixV2O5。下列说法中正确的是( )
LixV2O5。下列说法中正确的是( )| A.电池在放电时,Li+向负极移动 |
| B.锂在放电时做正极,充电时做阳极 |
| C.该电池充电时阳极的反应为LixV2O5-xe-=V2O5+xLi+ |
| D.V2O5只是锂发生反应的载体,不参与电池反应 |
您最近一年使用:0次
2019-11-15更新
|
624次组卷
|
19卷引用:2015届湖北省孝感高中高三十月阶段性考试化学试卷
(已下线)2015届湖北省孝感高中高三十月阶段性考试化学试卷(已下线)2015届浙江省柯桥中学高三月考(10月)化学试卷(已下线)2015届江西省新余一中高三上学期第三次模拟化学试卷2016届四川省成都石室中学高三上学期第一次月考化学试卷2016届黑龙江省哈尔滨第六中学高三上期中测试化学试卷2016-2017学年河北省邯郸市成安一中、永年二中高二上期中化学卷黑龙江省哈尔滨市第六中学2018届高三上学期期中考试化学试题河北省邯郸市2016-2017学年高二上学期期中考试化学试题安徽省六安市第一中学2018届高三上学期第五次月考化学试题高二人教版选修4 第四章 第二节 化学电源河北安平中学2019-2020学年高二上学期第二次月考化学试题福建省厦门外国语学校2019-2020学年高二上学期期中考试化学试题(已下线)2019年11月26日 《每日一题》化学人教版(选修4)——二次电池的工作原理福建省南安第一中学2019-2020学年高二上学期第二次月考化学(选考)试题黑龙江省伊春市第二中学2020届高三上学期期末考试理综化学试题湖南省邵阳市邵阳县第二中学2019年-2020学年高二下学期期末考试化学试题河南省宏力学校2020-2021学年高二上学期期末考试化学试题河北省保定市博野中学2021-2022学年高二上学期12月月考化学试题河北省石家庄市藁城区第一中学2021-2022学年高二上学期12月月考化学试题
名校
9 . 一种碳纳米管能够吸附氢气,用这种材料制备的电池其原理如图所示,该电池的电解质为6mol·L-1KOH溶液。下列说法中不正确 的是( )
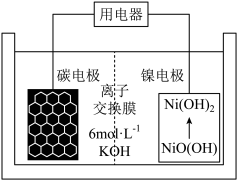

| A.放电时镍电极作负极 |
| B.放电时K+移向正极 |
| C.放电时碳电极的电极反应为H2-2e-+2OH-=2H2O |
| D.该反应过程中KOH溶液的浓度基本保持不变 |
您最近一年使用:0次
2019-11-10更新
|
193次组卷
|
3卷引用:湖北省随州一中2019-2020学年高二上学期期中考试化学试题
10 . 某碱性电池的总反应为:3HO2-+2Al=OH-+2AlO2-+H2O,工作原理如图所示。下列叙述错误的是


| A.电子迁移方向:Al→用电器→Pt |
| B.电池工作时,负极附近溶液pH减小 |
| C.正极反应式为:HO2-+3H+ +2e-=2H2O |
| D.负极会发生副反应:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
您最近一年使用:0次
2019-09-11更新
|
249次组卷
|
2卷引用:湖北省武汉市部分学校2020届新高三起点质量监测化学试题



