解题方法
1 . 我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如图。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述正确的是( )
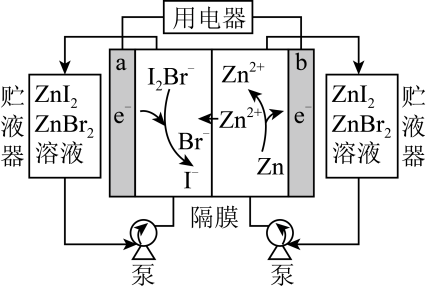

| A.放电时,b电极反应式为Zn2++2e-=Zn |
| B.放电时,a电极I-被氧化 |
| C.充电时,导线中每通过0.2mole-,b电极增重6.5g |
| D.充电时,a电极接外电源负极 |
您最近一年使用:0次
解题方法
2 . 全钒电池以惰性材料作电极,在电解质溶液中发生的原电池反应为 (黄色)
(黄色)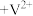 (绿色)
(绿色) (蓝色)
(蓝色)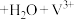 (紫色)。下列说法正确的是
(紫色)。下列说法正确的是

 (黄色)
(黄色)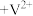 (绿色)
(绿色) (蓝色)
(蓝色)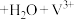 (紫色)。下列说法正确的是
(紫色)。下列说法正确的是
A.正极反应为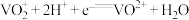 |
| B.正极附近的溶液由绿色逐渐变为紫色 |
C.反应每生成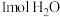 时转移电子的物质的量为 时转移电子的物质的量为 |
| D.电池使用过程中溶液的pH逐渐减小 |
您最近一年使用:0次
名校
解题方法
3 . 2019年诺贝尔化学奖颁给了三位锂电池领域有着杰出贡献的科学家,也使锂电池再一次受到世人关注。一种锂—空气电池直接使用金属锂作电极,从空气中获得 ,其工作装置如图所示,下列说法
,其工作装置如图所示,下列说法不正确 的是
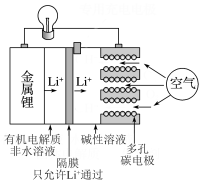
 ,其工作装置如图所示,下列说法
,其工作装置如图所示,下列说法
| A.若隔膜被腐蚀,会影响该电池正常使用 |
B.外电路有 电子通过时,通过膜的Li+的质量为 电子通过时,通过膜的Li+的质量为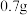 |
C.电池工作一段时间后,多孔碳电极附近的 变大 变大 |
D.和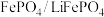 作电极的锂离子电池相比,锂—空气电池的能量密度(指标之一是单位质量电池所储存的能量)较小 作电极的锂离子电池相比,锂—空气电池的能量密度(指标之一是单位质量电池所储存的能量)较小 |
您最近一年使用:0次
解题方法
4 . Li-SO2Cl2电池可用于心脏起搏器。该电池的电极材料分别为Li和C,电解液是LiAlCl4-SO2Cl2,总反应为:2Li+SO2Cl2=2LiCl+SO2↑,其工作示意图如图所示。下列叙述中正确的是
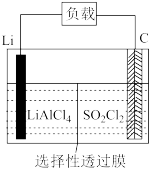

| A.电池工作时负极材料是Li,发生还原反应 |
| B.电池工作肘,电子流向:锂电极→负载→碳棒→电解液→锂电极 |
| C.外电路流过0.2mol电子,生成2.24L气体 |
| D.电池必须在无水、无氧的条件下进行工作 |
您最近一年使用:0次
2020-08-20更新
|
102次组卷
|
2卷引用:湖北省老河口市一中2020-2021学年高二12月阶段性考试化学试题
解题方法
5 . 元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的离子半径逐渐减小;化合物XN常温下为气体。据此回答:
(1)M在周期表的位置__________ ;X、Y、Z三种元素组成化合物的电子式为__________ ;
(2)N的最高价氧化物对应水化物的化学式为:__________ 。
(3)M与Fe与氢氧化钠溶液构成原电池,其负极反应式为:__________ ;
(4)Z的最高价氧化物的水化物和M的最高价氧化物反应的离子方程为__________
(1)M在周期表的位置
(2)N的最高价氧化物对应水化物的化学式为:
(3)M与Fe与氢氧化钠溶液构成原电池,其负极反应式为:
(4)Z的最高价氧化物的水化物和M的最高价氧化物反应的离子方程为
您最近一年使用:0次
名校
解题方法
6 . 金属燃料电池是一类重要的电池,其工作原理如图所示。下列说法正确的是


| A.正极上O2被氧化 |
| B.蔗糖可作为电解质 |
| C.电流由金属电极经导线流向空气电极 |
| D.消耗相同质量的Zn、Al、Mg时,通过导线转移的电子数最多的是Al |
您最近一年使用:0次
2020-08-08更新
|
224次组卷
|
4卷引用:湖北省十堰市2019-2020学年高一下学期期末考试化学试题
解题方法
7 . 熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为:2Na + x S Na2Sx (x = 5~3,难溶 于熔融硫)。下列说法错误的是
Na2Sx (x = 5~3,难溶 于熔融硫)。下列说法错误的是
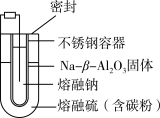
 Na2Sx (x = 5~3,难溶 于熔融硫)。下列说法错误的是
Na2Sx (x = 5~3,难溶 于熔融硫)。下列说法错误的是
A.Na2S4的电子式为: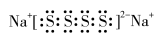 |
| B.放电时正极反应为:xS + 2Na+ + 2e- === Na2Sx |
| C.充电时的阴极反应:Na - e- === Na+ |
| D.Na和S分别为电池的负极和正极 |
您最近一年使用:0次
解题方法
8 . 某汽油(主要成分是丁烷)燃料电池,放电时反应的化学方程式为:2C4H10+ 13O2= 8CO2+ 10H2O,下列说法不正确的是
| A.其能量转换形式是将化学能直接转化为电能 |
| B.提炼汽油的原料是石油,石油是一种不可再生能源 |
| C.若负极上有32g O2参加反应,则反应过程中转移电子4mol e- |
D.若电池的电解质是固体氧化物(在高温下能传导O2-),其工作原理如图: |
您最近一年使用:0次
名校
解题方法
9 . 2019年诺贝尔化学奖授予对锂离子电池研究有突出贡献的科学家。一种“大气固碳”的锂离子电池工作原理如图所示,该电池在充电时,通过催化剂的选择性控制,只有Li2CO3被氧化,释放出CO2和O2。下列说法不正确的是
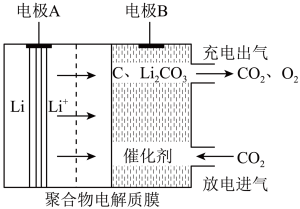

| A.该电池应选用无水电解质 |
| B.该电池放电时的正极反应为4Li++3CO2+4e-=C+2Li2CO3 |
| C.充电时若电极A质量增加14g,则聚合物电解质膜上通过电子2mol |
| D.该电池放电、充电各一次且都转移4mole−时,理论上能固定1molCO2 |
您最近一年使用:0次
2020-06-23更新
|
150次组卷
|
3卷引用:湖北省咸宁市嘉鱼县第一中学2019-2020学年高二下学期期末考试化学试题
名校
解题方法
10 . 如图所示是原电池的装置图。请回答:

(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为___ ;反应进行一段时间后溶液酸性将__ (填“增强”“减弱”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为___ ,B(负极)极材料为__ ,溶液C为___ 。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
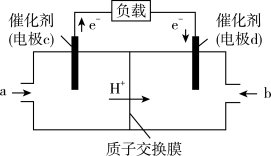
电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是__ (填“正极”或“负极”),c电极的反应方程式为__ 。若线路中转移1mol电子,则上述CH3OH燃料电池消耗的O2在标准状况下的体积为__ L。

(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是
您最近一年使用:0次
2020-06-23更新
|
555次组卷
|
3卷引用:湖北省黄冈市黄州区第一中学2019-2020学年高一下学期6月月考化学试题



