解题方法
1 . 下列说法不正确 的是
| A.镁条着火不能用干冰灭火 |
| B.ClO2是一种高效安全的灭菌消毒剂 |
| C.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀 |
| D.氯化铁、硫酸亚铁都是优良的净水剂,可用于自来水的消毒 |
您最近半年使用:0次
2 . 下列实验操作和现象及所得出的结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴加几滴K3[Fe(CN)6]溶液,无明显现象 | 该过程未发生氧化还原反应 |
| B | 在各盛5ml1mol/LNaOH溶液的两支试管中,分别滴入5滴1mol/LFeCl3溶液和1mol/LAlCl3溶液,前者有红褐色沉淀生成,后者无沉淀生成 | Ksp[Fe(OH)3]<Ksp[Al(OH)3] |
| C | 室温下,用pH试纸分别测定浓度为0.1mol·L−1NaClO溶液和0.1mol·L−1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| D | T℃时,向等体积的饱和AgCl、AgBr溶液中分别滴加足量AgNO3溶液,所得沉淀n(AgCl)>n(AgBr) | T℃时,Ksp:AgCl>AgBr |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚。某科研所在处理含苯酚废水的同时获得电能,原理如图所示。下列说法正确的是
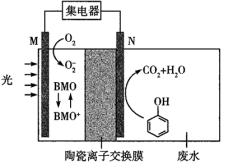

| A.此装置只将光能转化为电能 |
| B.每氧化1 mol C6H5OH需要156.8 L O2 |
| C.M为负极,N为正极 |
| D.N极的电极反应式是C6H5OH+7O2-7e-=6CO2↑+3H2O |
您最近半年使用:0次
名校
解题方法
4 . 快速充放电铝离子电池与锂离子电池相比,其充电速度更快,寿命更长。其原理如图所示。下列说法不正确 的是


A.电池放电时,负极反应式为: |
| B.电池放电时,有机阳离子EM+向石墨电极移动 |
C.电池充电时,石墨电极表面发生反应: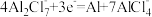 |
| D.电池充电时,Al与外电源的负极相连 |
您最近半年使用:0次
2021-02-03更新
|
177次组卷
|
2卷引用:北京市东城区2020-2021学年高二上学期期末考试化学试题
2018高三下·全国·专题练习
名校
解题方法
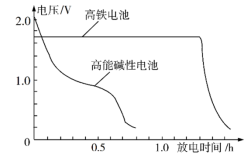
5 . 高铁电池是以高铁酸盐(K2FeO4、BaFeO4等)为材料的新型可充电电池,这种电池能量密度大、体积小、重量轻、污染低。这种电池的总反应为:3Zn+2 +8H2O
+8H2O 3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
 +8H2O
+8H2O 3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
3Zn(OH)2+2Fe(OH)3+4OH−。下图是高铁电池与普通的高能碱性电池的使用电压对比。下列有关高铁电池的判断不正确的是
| A.放电过程中正极区域电解液pH升高 |
| B.放电时负极反应式为:Zn+2H2O−2e−=Zn(OH)2+2H+ |
| C.充电时,每转移3 mol电子,则有1 mol Fe(OH)3被氧化 |
| D.高铁电池比高能碱性电池电压稳定,放电时间长 |
您最近半年使用:0次
2021-02-02更新
|
200次组卷
|
5卷引用:2018年3月2018届高三第一次全国大联考(新课标Ⅲ卷)-化学试题
(已下线)2018年3月2018届高三第一次全国大联考(新课标Ⅲ卷)-化学试题天津市南开中学2020届高三上学期第五次月考化学试题(已下线)专题4.2 化学电源-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)4.2 化学电源(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)天津市实验中学滨海学校2021届高三上学期期中考试化学试题
名校
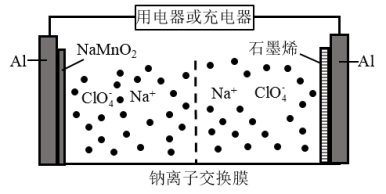
6 . 我国科研团队成功研究出高比能量、低成本的钠离子二次电池,其工作原理如图所示。已知电池反应:Na1-xMnO2 + NaxCn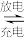 NaMnO2 + nC.下列说法错误的是
NaMnO2 + nC.下列说法错误的是
 NaMnO2 + nC.下列说法错误的是
NaMnO2 + nC.下列说法错误的是
| A.电池放电过程中,NaMnO2/Al 为正极 |
| B.电池放电时,正极发生反应 Na1-xMnO2 +xNa+ +xe- =NaMnO2 |
| C.电池充电时,外接电源的负极连接 NaMnO2/Al 电极 |
| D.电池充电时,Na+由 NaMnO2/Al 电极移向石墨烯/Al 电极 |
您最近半年使用:0次
7 . 如图是一种新型电池的工作原理图。下列关于该电池工作时的说法正确的是
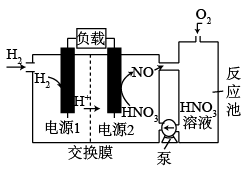

| A.电极1为负极,发生还原反应 |
B.电池总反应为 |
| C.电子由电极2经过负载流入电极1 |
D.电池工作时间越长,右侧反应池内溶液中 越高 越高 |
您最近半年使用:0次
解题方法
8 . 碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,则下列说法错误的是
已知电池总反应式:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)
已知电池总反应式:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)
| A.电池工作时,锌失去电子 |
| B.电池工作时,溶液中OH-向正极移动 |
| C.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq) |
| D.外电路中每通过0.2mole-,锌的质量理论上减小6.5g |
您最近半年使用:0次
9 . 甲烷是一种重要的化工原料和清洁能源,研究其相关反应并合理利用具有重要意义。请回答下列问题:
(1)已知:a.工业上甲烷可用于制造合成气,常温常压下其反应为 ;b.
;b. 、
、 的燃烧热依次为
的燃烧热依次为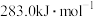 、
、 。常温常压下,
。常温常压下,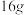 甲烷完全燃烧生成液态水放出的热量为
甲烷完全燃烧生成液态水放出的热量为___________ 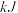 。
。
(2)将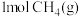 和
和 充入盛有催化剂的5L刚性密闭容器中发生反应:
充入盛有催化剂的5L刚性密闭容器中发生反应: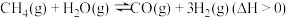 ,相同时间内测得
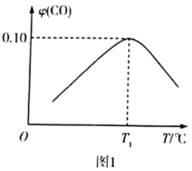
,相同时间内测得 的体积分数
的体积分数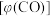 与温度(T)的关系如图1所示。
与温度(T)的关系如图1所示。
①既能提高甲烷的转化率又能提高反应速率的措施是___________ (填序号)。
A.在其他条件不变时,充入氮气
B.在其他条件不变时,再充入
C.在其他条件不变时,升高反应温度
D.在其他条件不变时,再充入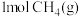 和
和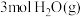
②温度大于 ℃时,随着温度的升高,
℃时,随着温度的升高, 的体积分数降低的可能原因是
的体积分数降低的可能原因是___________ (写一条即可)
③假设 ℃时反应达到平衡所需的时间为
℃时反应达到平衡所需的时间为 ,平衡时
,平衡时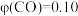 ,则从开始至达到平衡时间内用
,则从开始至达到平衡时间内用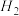 表示的化学反应速率为
表示的化学反应速率为___________ ,反应的平衡常数K为___________ 。
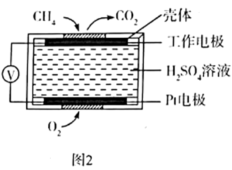
(3)甲烷属于易燃易爆气体,可用电化学原理测定空气中甲烷的含量防止爆炸事故的发生,其原理如图所示,则负极的电极反应式为___________ ;若测得标准状况下空气中甲烷的含量为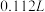 ,当甲烷完全被氧化时消耗的
,当甲烷完全被氧化时消耗的 为
为___________  。
。
(1)已知:a.工业上甲烷可用于制造合成气,常温常压下其反应为
 ;b.
;b. 、
、 的燃烧热依次为
的燃烧热依次为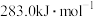 、
、 。常温常压下,
。常温常压下,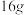 甲烷完全燃烧生成液态水放出的热量为
甲烷完全燃烧生成液态水放出的热量为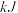 。
。(2)将
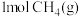 和
和 充入盛有催化剂的5L刚性密闭容器中发生反应:
充入盛有催化剂的5L刚性密闭容器中发生反应: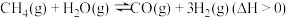 ,相同时间内测得
,相同时间内测得 的体积分数
的体积分数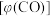 与温度(T)的关系如图1所示。
与温度(T)的关系如图1所示。

①既能提高甲烷的转化率又能提高反应速率的措施是
A.在其他条件不变时,充入氮气
B.在其他条件不变时,再充入

C.在其他条件不变时,升高反应温度
D.在其他条件不变时,再充入
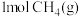 和
和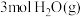
②温度大于
 ℃时,随着温度的升高,
℃时,随着温度的升高, 的体积分数降低的可能原因是
的体积分数降低的可能原因是③假设
 ℃时反应达到平衡所需的时间为
℃时反应达到平衡所需的时间为 ,平衡时
,平衡时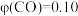 ,则从开始至达到平衡时间内用
,则从开始至达到平衡时间内用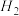 表示的化学反应速率为
表示的化学反应速率为(3)甲烷属于易燃易爆气体,可用电化学原理测定空气中甲烷的含量防止爆炸事故的发生,其原理如图所示,则负极的电极反应式为
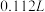 ,当甲烷完全被氧化时消耗的
,当甲烷完全被氧化时消耗的 为
为 。
。
您最近半年使用:0次
解题方法
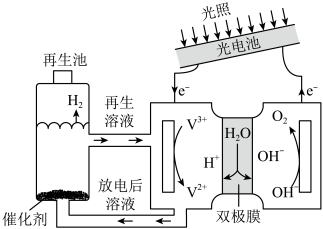
10 . 光电池在光照条件下可产生电压,如图所示装置可实现光能的充分利用。双极膜复合层间的 能解离为
能解离为 和
和 ,且双极膜能实现
,且双极膜能实现 和
和 的定向通过。下列说法正确的是
的定向通过。下列说法正确的是
 能解离为
能解离为 和
和 ,且双极膜能实现
,且双极膜能实现 和
和 的定向通过。下列说法正确的是
的定向通过。下列说法正确的是
| A.该装置将光能最终转化为电能 | B.当阳极生成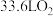 时,电路中转移电子数为 时,电路中转移电子数为 |
C.再生池中的反应为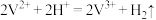 | D.光照过程中阳极区溶液中的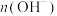 基本不变 基本不变 |
您最近半年使用:0次
2021-02-01更新
|
159次组卷
|
2卷引用:山东省临沂市2020-2021学年度高二上学期期末质量检测化学试题



