名校
解题方法
1 . 北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜。”回答下列问题:
(1)基态Cu原子的电子排布式为_______ ; 量子力学把电子在原子核外的一个空间运动状态称为一个原子轨道,基态Cu原子核外电子有_______ 个空间运动状态。
(2)胆矾的化学式为CuSO4·5H2O, 其中SO 的空间构型为
的空间构型为_______
(3)Cu2+能与乙二胺四乙酸根阴离子(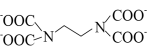 )形成配离子,组成该阴离子的H、C、N、O四种元素的电负性由大到小的顺序是
)形成配离子,组成该阴离子的H、C、N、O四种元素的电负性由大到小的顺序是_______ ,第一电离能最大的是______ ;C、N原子的轨道杂化类型分别为_____________ 。
(4)Cu的某种含结晶水的氯化物晶体的晶胞结构如图所示。
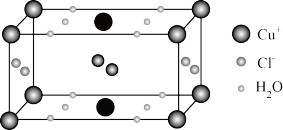
①该晶体的化学式为_____________ 。
②已知晶胞参数为: apm,bpm、 cpm,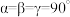 , 设NA为阿伏加德罗常数的值,则该晶体的密度为
, 设NA为阿伏加德罗常数的值,则该晶体的密度为__________ g·cm-3。
(1)基态Cu原子的电子排布式为
(2)胆矾的化学式为CuSO4·5H2O, 其中SO
 的空间构型为
的空间构型为(3)Cu2+能与乙二胺四乙酸根阴离子(
 )形成配离子,组成该阴离子的H、C、N、O四种元素的电负性由大到小的顺序是
)形成配离子,组成该阴离子的H、C、N、O四种元素的电负性由大到小的顺序是(4)Cu的某种含结晶水的氯化物晶体的晶胞结构如图所示。

①该晶体的化学式为
②已知晶胞参数为: apm,bpm、 cpm,
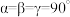 , 设NA为阿伏加德罗常数的值,则该晶体的密度为
, 设NA为阿伏加德罗常数的值,则该晶体的密度为
您最近一年使用:0次
名校
2 . 下列关于元素的“最”及其因果关系描述正确的是
| A.元素周期表的f区包括镧系、锕系元素,所以周期表中含元素种类最多的区为f区 |
| B.因为F元素的得电子能力最强,所以元素周期表中第一电离能最大的是F |
C.因为元素非金属性F>O,所以最简单氢化物的沸点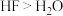 |
D.因为C原子易形成 杂化轨道,可以以四个价键进行不同方式的连接,所以形成化合物种类最多的元素在第ⅣA族 杂化轨道,可以以四个价键进行不同方式的连接,所以形成化合物种类最多的元素在第ⅣA族 |
您最近一年使用:0次
2021-07-13更新
|
142次组卷
|
3卷引用:云南省曲靖市第一中学2023-2024学年高二下学期3月月考化学试题
3 . 下列有关图示,能直观形象地展示化学知识。以下图示正确的是
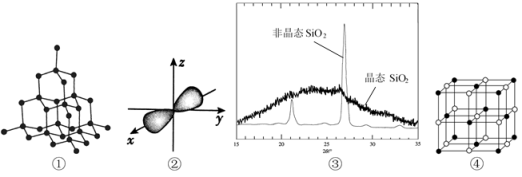
| A.①表示石墨的空间结构 |
| B.②表示2s电子云轮廓图 |
| C.③表示非晶态SiO2、晶态SiO2X-衍射粉末图谱 |
| D.④表示NaCl晶体的晶胞结构图 |
您最近一年使用:0次
2021-07-06更新
|
212次组卷
|
2卷引用:云南省曲靖市第一中学2023-2024学年高二下学期3月月考化学试题
名校
4 . (1)一个基态原子电子排布为1s22s22p63s23p1的元素最可能的价态是___________ ,某元素原子的3p原子轨道中有2个未成对电子,则该原子的价电子轨道式 可表示为___________ 。
(2)B、C、Al、Si四种原子中,第一电离能最大的是___________ ,价层电子排布式为4s1、2s22p3、3s23p4、3d64s2的四种元素,电负性最大的是___________ (填元素符号 )。
(3)元素周期表中能稳定存在且电负性相差最大的两种元素形成的化合物的化学式为___________ ,X、Y、Z三种短周期元素的原子序数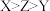 ,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子p电子数比Y原子多2个。Z、Y所形成的化合物的化学式为
,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子p电子数比Y原子多2个。Z、Y所形成的化合物的化学式为___________ 。
(2)B、C、Al、Si四种原子中,第一电离能最大的是
(3)元素周期表中能稳定存在且电负性相差最大的两种元素形成的化合物的化学式为
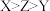 ,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子p电子数比Y原子多2个。Z、Y所形成的化合物的化学式为
,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子p电子数比Y原子多2个。Z、Y所形成的化合物的化学式为
您最近一年使用:0次
2021-07-06更新
|
323次组卷
|
3卷引用:云南省泸西县第一中学2021-2022学年高二下学期期中考试化学试题
云南省泸西县第一中学2021-2022学年高二下学期期中考试化学试题河南省2020-2021学年高二下学期领军考试7月联考化学试题(已下线)1.2.2 原子结构与元素周期律(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)
5 . 有A、B、C、D、E、F六种短周期元素,其原子序数依次增大,A元素基态原子的p能级上的电子数等于次外层电子数,C元素基态原子的s能级与p能级上的电子数相等,D是短周期中电负性最小的元素,E原子的第一电离能至第四电离能分别为578、1817、2745、11575(单位:kJ·mol-1),F原子的价电子构型与C原子的相同。请回答下列问题:
(1)推测B的电负性___________ (填“>”或“<”)F的电负性。
(2)写出D原子的电子排布图:___________ ,该原子的能层数为___________ 。
(3)写出元素E与D的最高价氧化物对应的水化物的水溶液反应的离子方程式:___________ 。
(1)推测B的电负性
(2)写出D原子的电子排布图:
(3)写出元素E与D的最高价氧化物对应的水化物的水溶液反应的离子方程式:
您最近一年使用:0次
解题方法
6 . 铑的配合物Rh(PPh3)Cl可催化丙烯与氢气的加成,反应过程为:CH3CH=CH2+H2 CH3CH2CH3,回答下列问题:
CH3CH2CH3,回答下列问题:
(1)基态Rh原子的价电子排布式为4d85s1,铑在周期表的位置是_______ ,其原子中的未成对电子数为_______ 。
(2) 1mol丙烯(CH3CH=CH2)中σ键的数目为_______ ,其结构简式中打点的C原子与H原子间的σ键可称为sp2-sσ键,则丙烯分子中C原子之间的所有σ键可称为_______ 。
(3)第一电离能P_______ Cl (填“大于”或“小于”),PPh3是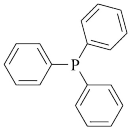 的缩写,该分子的立体构型是
的缩写,该分子的立体构型是_______ 。比较PPh3与PH3的沸点大小,并说明原因_______ 。
(4) RhCl3的晶胞结构中Rh3+的位置如图所示(Cl-未画出):
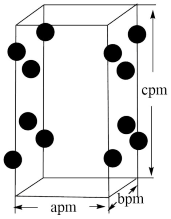
①晶胞中含有的Cl-数目为_______ ;
②若阿伏加德罗常数为NA,则晶体的密度为_______ g·cm-3.(列出计算式)
 CH3CH2CH3,回答下列问题:
CH3CH2CH3,回答下列问题:(1)基态Rh原子的价电子排布式为4d85s1,铑在周期表的位置是
(2) 1mol丙烯(CH3CH=CH2)中σ键的数目为
(3)第一电离能P
 的缩写,该分子的立体构型是
的缩写,该分子的立体构型是(4) RhCl3的晶胞结构中Rh3+的位置如图所示(Cl-未画出):

①晶胞中含有的Cl-数目为
②若阿伏加德罗常数为NA,则晶体的密度为
您最近一年使用:0次
2021-05-31更新
|
261次组卷
|
2卷引用:云南省昆明市2021届高三“三诊一模”模拟考试(三模)理科综合化学试题
解题方法
7 . 2021年,我国学者研究发现将FeNi层状双氢氧化物负载到g—C3N4纳米片上,可以有效提高光催化还原CO2生成CH3OH的产率。回答下列问题:
(1)基态Fe原子的价层电子排布式是______ 。
(2)CH3OH的沸点高于CO2的原因是______ 。
(3)C、N、O的第一电离能大小顺序为______ 。
(4)已知:孤电子对与成键电子对之间的排斥力大于成键电子对与成键电子对之间的排斥力。NH3可以与Ni2+形成配离子[Ni(NH3)4]2+,该离子中的H—N—H键角______ (填“大于”、“小于”或“等于”)NH3中的H—N—H键角。[Ni(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,则[Ni(NH3)4]2+的立体构型是______ 。
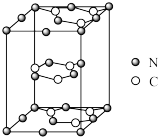
(5)一种石墨相g—C3N4的单层平面结构和晶体结构如图所示:
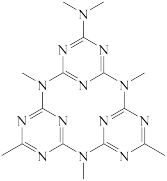
①石墨相g—C3N4中C的杂化方式是______ ,1molg—C3N4中的σ键的数目是______ ,g—C3N4______ (填“是”或“否”)具有导电性。
②已知:如图的中间层原子均在晶胞内部,晶胞的密度是ρg▪cm-3,晶胞的体积是Vpm3,则阿伏加德罗常数NA=______ 。
(1)基态Fe原子的价层电子排布式是
(2)CH3OH的沸点高于CO2的原因是
(3)C、N、O的第一电离能大小顺序为
(4)已知:孤电子对与成键电子对之间的排斥力大于成键电子对与成键电子对之间的排斥力。NH3可以与Ni2+形成配离子[Ni(NH3)4]2+,该离子中的H—N—H键角
(5)一种石墨相g—C3N4的单层平面结构和晶体结构如图所示:

①石墨相g—C3N4中C的杂化方式是
②已知:如图的中间层原子均在晶胞内部,晶胞的密度是ρg▪cm-3,晶胞的体积是Vpm3,则阿伏加德罗常数NA=

您最近一年使用:0次



