名校
解题方法
1 . 钛(Ti)及其化合物的应用研究是目前前沿科学之一,请回答下列问题;
(1)基态钛原子的电子排布式为___________ ,核外电子占据的轨道数为___________ 。
(2)与钛位于同一周期且基态原子不成对电子与钛相同的元素,第一电离能由大到小的顺序为___________ (用元素符号填空)。
(3)TiCl4常温下为无色液体,熔点250K,沸点409K,则TiCl4属于___________ 晶体。 TiCl4在水中或空气中极易水解,露置于空气中形成白色烟雾,烟雾中的固体成分可用TiO2·nH2O表示,请写出TiCl4在空气中产生烟雾的化学方程式:___________ 。
(4)TiO2作光催化剂可将甲醛、苯等有害气体转化为CO2和H2O。
①上述含碳原子的分子中,碳原子的杂化方式为sp2的是___________ (填名称)
②下列各组微粒互为等电子体的是___________ (填字母标号)。
A. H2O与SO2 B. CO2与N2O C. CH2O与BF3 D. C6H6与B3N3H6
(5)金红石(TiO2)的晶胞结构如图所示,设NA为阿伏加德罗常数的值,则该晶体的密度为___________ g·cm-3(用含相关字母和符号的代数式表示)。

(1)基态钛原子的电子排布式为
(2)与钛位于同一周期且基态原子不成对电子与钛相同的元素,第一电离能由大到小的顺序为
(3)TiCl4常温下为无色液体,熔点250K,沸点409K,则TiCl4属于
(4)TiO2作光催化剂可将甲醛、苯等有害气体转化为CO2和H2O。
①上述含碳原子的分子中,碳原子的杂化方式为sp2的是
②下列各组微粒互为等电子体的是
A. H2O与SO2 B. CO2与N2O C. CH2O与BF3 D. C6H6与B3N3H6
(5)金红石(TiO2)的晶胞结构如图所示,设NA为阿伏加德罗常数的值,则该晶体的密度为

您最近一年使用:0次
名校
2 . CdSnAs2是一种高迁移率的新型热电材料,回答下列问题:
(1)Sn为ⅣA族元素,Sn原子的价层电子排布图为___________ 。
(2)单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为___________ ,其固体的晶体类型为___________ 。
(3)第一电离能:Sn___________ As(填“大于”或“小于”)。
(4)NH3、PH3、AsH3的沸点由高到低的顺序为___________ (填化学式,下同),原因是___________ ;
NH3、PH3、AsH3的键角由大到小的顺序为___________ 。
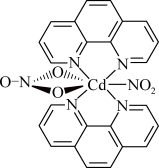
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示, 1mol该配合物中通过螯合作用形成的配位键有___________ mol,该螯合物中C的杂化方式为 ___________ 。
(6)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
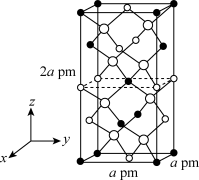
一个晶胞中有___________ 个Sn,CdSnAs2晶体中与单个Sn键合的As有___________ 个。
找出距离Cd(0,0,0)最近的Sn___________ (用分数坐标表示)。
(1)Sn为ⅣA族元素,Sn原子的价层电子排布图为
(2)单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为
(3)第一电离能:Sn
(4)NH3、PH3、AsH3的沸点由高到低的顺序为
NH3、PH3、AsH3的键角由大到小的顺序为
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示, 1mol该配合物中通过螯合作用形成的配位键有
(6)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标 原子 | x | y | z |
| Cd | 0 | 0 | 0 |
| Sn | 0 | 0 | 0.5 |
| As | 0.25 | 0.25 | 0.125 |

一个晶胞中有
找出距离Cd(0,0,0)最近的Sn
您最近一年使用:0次
3 . 自然界中有许多矿石,如闪锌矿主要成分为ZnS,硫铁矿主要成分为FeS2等,它们都是化工生产中重要的化工原料。回答下列问题:
(1)FeS2中Fe2+的价层电子排布图为___________
(2)在常温下ZnS与稀硫酸作用时,有气体产生。该气体的沸点比水低的主要原因是______
(3)高温加热闪锌矿生成SO2,SO2中共价键的类型有___________ (填“σ键”或“π键”),属于___________ (填“极性”或“非极性”)分子;SO2与SO3的键角相比,键角更大的是___________ ,氧和硫形成 的空间构型为
的空间构型为___________ ,中心原子S的杂化方式为___________ 。
(4)某矿石主要成分是由A(Fe)、B、C三种元素构成的化合物,其中B、C的价电子排布分别为3d104s1、3s23p4,其晶胞结构如下图所示,该晶胞上下底面为正方形,侧面与底面垂直。

①一个晶胞中有___________ 个B,晶体中与单个B键合的C有_______ 个。
②已知:NA为阿伏加德罗常数的值,根据如图中所示的数据可得该晶体的密度是________ g∙cm-3(列出计算式)。
(1)FeS2中Fe2+的价层电子排布图为
(2)在常温下ZnS与稀硫酸作用时,有气体产生。该气体的沸点比水低的主要原因是
(3)高温加热闪锌矿生成SO2,SO2中共价键的类型有
 的空间构型为
的空间构型为(4)某矿石主要成分是由A(Fe)、B、C三种元素构成的化合物,其中B、C的价电子排布分别为3d104s1、3s23p4,其晶胞结构如下图所示,该晶胞上下底面为正方形,侧面与底面垂直。

①一个晶胞中有
②已知:NA为阿伏加德罗常数的值,根据如图中所示的数据可得该晶体的密度是
您最近一年使用:0次
2022-01-03更新
|
187次组卷
|
2卷引用:广西玉林市、贵港市2021-2022学年高三上学期12月联合模拟考试理科综合化学试题
4 . 钇(Y)是第一种被发现的稀土元素,位于元素周期表的第 5 周期第 IIIB 族,其在电子、激光、超导等领域均有广泛应用。回答下列问题:
(1)基态 Y 原子的价电子排布式为___________ 。
(2)Y(NO3)3与水杨酸甲酯( )反应,可制得配合物同时生成 HNO3,其中配合物能用于捕获 NO。
)反应,可制得配合物同时生成 HNO3,其中配合物能用于捕获 NO。
①Y(NO3)3中所含三种元素的第一电离能由大到小的顺序为______ (用元素符号表示);NO 的立体构型为
的立体构型为___________ 。
②lmol HNO3中含有σ键的数目为______ ,HNO3的酸性强于HNO2的原因为___________ 。
③水杨酸甲酯中 C 的杂化类型为___________ ,水杨酸甲酯沸点高于水杨酸( )的主要原因为
)的主要原因为___________ 。
④NO 分子中,N、O 原子间形成共价键的电子云对称形式包括镜面对称和___________ 。
(3)Y、Cu、Ba、O 形成的一种具有超导性的材料的晶胞结构如图所示。若 NA表示阿伏加德罗常数的值, =
= =
= ,则该晶体的密度ρ=
,则该晶体的密度ρ=___________ g•cm-3 (用含a、c、N A的代数式表示)。

(1)基态 Y 原子的价电子排布式为
(2)Y(NO3)3与水杨酸甲酯(
 )反应,可制得配合物同时生成 HNO3,其中配合物能用于捕获 NO。
)反应,可制得配合物同时生成 HNO3,其中配合物能用于捕获 NO。①Y(NO3)3中所含三种元素的第一电离能由大到小的顺序为
 的立体构型为
的立体构型为②lmol HNO3中含有σ键的数目为
③水杨酸甲酯中 C 的杂化类型为
 )的主要原因为
)的主要原因为④NO 分子中,N、O 原子间形成共价键的电子云对称形式包括镜面对称和
(3)Y、Cu、Ba、O 形成的一种具有超导性的材料的晶胞结构如图所示。若 NA表示阿伏加德罗常数的值,
 =
= =
= ,则该晶体的密度ρ=
,则该晶体的密度ρ=
您最近一年使用:0次
5 . C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)科学家常利用___________ 区分晶体SiO2和非晶体SiO2.,基态Ge原子价电子排布图为___________ ,第四周期与基态Ge原子具有相同数目未成对电子数的元素有___________ (填元素符号)。
(2)SnCl2极易水解生成Sn(OH)Cl沉淀,Sn(OH)Cl中四种元素电负性由小到大的顺序为___________ 。SnO2是一种重要的半导体传感器材料,用来制备灵敏度高的气敏传感器,SnO2与熔融NaOH反应生成Na2SnO3,Na2SnO3中阴离子的空间构型为___________ 。
(3)灰锡的晶体结构与金刚石相似(如图所示),其中A处原子的原子分数坐标为(0,0,0)。
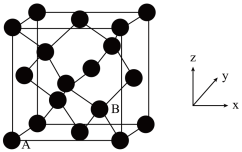
①B处原子的原子分数坐标为___________ 。
②已知灰锡的密度为ρg·m-3,设NA为阿伏加德罗常数的值,根据硬球接触模型,则Sn原子半径r(Sn)=___________ pm(可只列式不计算)。
(1)科学家常利用
(2)SnCl2极易水解生成Sn(OH)Cl沉淀,Sn(OH)Cl中四种元素电负性由小到大的顺序为
(3)灰锡的晶体结构与金刚石相似(如图所示),其中A处原子的原子分数坐标为(0,0,0)。

①B处原子的原子分数坐标为
②已知灰锡的密度为ρg·m-3,设NA为阿伏加德罗常数的值,根据硬球接触模型,则Sn原子半径r(Sn)=
您最近一年使用:0次
解题方法
6 . 元素H、N、O、S、Fe之间可形成多种化合物。请回答下列问题:
(1)基态Fe原子的价层电子排布式为___________ ;其最外层电子的电子云形状为___________ 。
(2)N、O、S三种元素的第一电离能由大到小的顺序为___________ 。
(3)写出一种与SO 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式___________ ,NH 的空间构型为
的空间构型为___________ 。
(4)NH OH-
OH- NH3H2O,NH
NH3H2O,NH 转化为NH3的过程中,没有发生变化的是
转化为NH3的过程中,没有发生变化的是___________ 。
A.键角 B.粒子的空间构型 C.中心原子的杂化轨道类型
(5)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①晶胞a的堆积方式为___________ 堆积;
②晶胞b中铁原子的配位数为___________ ,空间利用率为___________ ;
③若晶胞c的密度为gcm-3,则铁的原子半径r___________ cm。(用含、NA的式子表示,NA表示阿伏加德罗常数的值)。
(1)基态Fe原子的价层电子排布式为
(2)N、O、S三种元素的第一电离能由大到小的顺序为
(3)写出一种与SO
 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式 的空间构型为
的空间构型为(4)NH
 OH-
OH- NH3H2O,NH
NH3H2O,NH 转化为NH3的过程中,没有发生变化的是
转化为NH3的过程中,没有发生变化的是A.键角 B.粒子的空间构型 C.中心原子的杂化轨道类型
(5)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①晶胞a的堆积方式为
②晶胞b中铁原子的配位数为
③若晶胞c的密度为gcm-3,则铁的原子半径r
您最近一年使用:0次
名校
7 . 下列叙述正确的是
| A.[Ar]3d64s2是基态原子的电子排布 |
| B.铬原子的电子排布式是:1s22s22p63s23p64s13d5 |
| C.铜原子的外围电子排布式是:3d94s2 |
D.氮原子的轨道表示式是: |
您最近一年使用:0次
2021-05-24更新
|
720次组卷
|
21卷引用:广西平果市第二中学2020-2021学年高二下学期期中考试化学试题
广西平果市第二中学2020-2021学年高二下学期期中考试化学试题甘肃省天水市秦安县第一中学2020-2021学年高二上学期期末考试化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 B素养拓展区(已下线)第一章 原子结构与性质【过关测试基础卷】-2020-2021学年高二化学单元复习测试(新教材人教版选择性必修2)(已下线)模块同步卷01 原子结构和元素周期律-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)宁夏海原第一中学2020-2021学年高二下学期期中考试化学试题广东省东莞市新世纪英才学校2021-2022学年高二上学期第一次教学质量检测化学试题(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)第1章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修1)重庆市万州第二高级中学2020-2021学年高二上学期期末考试化学试题新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题海南省三亚华侨学校2019-2020学年高二上学期期中考试化学试题山西省朔州市怀仁县第一中学2018-2019学年高二下学期第三次月考化学试题山东省东营市广饶县第一中学2019-2020学年高二下学期3月线上考试化学试题第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(1卷)试题山西省临汾市尧都区山西师范大学实验中学2021-2022学年高二下学期第一次月考化学考试试题广东省清远市华侨中学2021-2022学年高二下学期6月月考化学试题广东省云浮市罗定中学2022-2023学年高二下学期第2周周测(分子结构与性质)化学试题广东省深圳市盐田高级中学2021-2022学年高二下学期4月考试化学试题(已下线)BBWYhjhx1112.pdf
8 . 下表为元素周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)表中属于d区的元素是________ (填编号),其原子结构示意图是 ________________ 。
(2)写出元素⑩的基态原子的简化电子排布式:________________________________ 。
(3)某元素的特征电子排布式为 ,该元素是
,该元素是 ________ (填名称),原子的最外层电子的成对电子为 ________ 对。
(4)③和④的简单气态氢化物最稳定的是________ (填化学式,下同),⑦的最强含氧酸为 ________ 。
(5)⑦和③形成的化合物的电子式是________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | |||||||||||||||
| ⑧ | ⑨ | ⑩ |
(1)表中属于d区的元素是
(2)写出元素⑩的基态原子的简化电子排布式:
(3)某元素的特征电子排布式为
 ,该元素是
,该元素是 (4)③和④的简单气态氢化物最稳定的是
(5)⑦和③形成的化合物的电子式是
您最近一年使用:0次
2021-04-13更新
|
84次组卷
|
2卷引用:广西钦州市浦北县浦北中学2020-2021学年高二3月月考化学试题
20-21高二·全国·单元测试
名校
解题方法
9 . 下表列出了某短周期元素 的各级电离能数据(用
的各级电离能数据(用 、
、 表示,单位为
表示,单位为 )。
)。
下列关于元素 的判断中一定正确的是
的判断中一定正确的是
 的各级电离能数据(用
的各级电离能数据(用 、
、 表示,单位为
表示,单位为 )。
)。 |  |  |  | …… | |
| R | 740 | 1500 | 7700 | 10500 | …… |
 的判断中一定正确的是
的判断中一定正确的是| A.R的最高正价为+3 |
| B.R元素位于元素周期表中第IIA族 |
| C.R元素的原子最外层共有4个电子 |
D.R元素基态原子的电子排布式为 |
您最近一年使用:0次
2021-04-13更新
|
2020次组卷
|
26卷引用:广西钦州市浦北县浦北中学2020-2021学年高二3月月考化学试题
广西钦州市浦北县浦北中学2020-2021学年高二3月月考化学试题(已下线)第一单元 原子结构(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)(已下线)模块同步卷11 综合检测卷(基础卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)1.3.1 电离能及其变化规律-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)甘肃省酒泉市青海油田第一中学2020-2021学年高二下学期期中考试化学试题宁夏海原第一中学2020-2021学年高二下学期期中考试化学试题河南省正阳高中2020-2021学年高二下学期第三次素质检测化学试题新疆乌鲁木齐市第四中学2020-2021学年高二下学期期末考试化学试题新疆新源县第二中学2020-2021学年高二下学期期末联考化学试题(已下线)考向36 原子结构与性质-备战2022年高考化学一轮复习考点微专题(已下线)1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)河南省汤阴县五一中学2019-2020学年高二下学期期中考试化学试题(已下线)第38练 原子结构与元素的性质-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省肇东市第四中学2021-2022学年高二下学期期中考试化学试题福建省三明市宁化第六中学2021-2022学年高二下学期第一次月考化学试题四川省内江市第六中学2022-2023学年高二上学期第一次月考化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二下学期期末考试化学试题黑龙江省大庆市第五十六中学2021-2022学年高二学年下学期期中考试化学试题新疆乌鲁木齐市第101中学2021-2022学年高二下学期期末考试化学试题湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题河北省保定市唐县第一中学2022-2023学年高二下学期5月月考化学试题安徽省滁州市实验中学等2校2022-2023学年高二上学期1月期末考试化学试题河北省沧州市2023-2024学年高二上学期12月月考化学试题黑龙江省哈尔滨市六校联考2023-2024学年高二上学期1月期末化学试题(已下线)热点02 原子结构与元素的性质福建省福州第二中学2023-2024学年高二下学期3月月考化学试题
10 . 2020年11月24日4时30分,我国在文昌航天发射场,用长征五号遥五运载火箭成功发射探月工程“嫦娥五号”探测器,顺利将探测器送入预定轨道,开启我国首次地外天体采样返回之旅。已知所用火箭推进剂为肼(N2H4)和过氧化氢(H2O2),火箭箭体一般采用钛合金材料。请回答下列问题:
(1)基态钛原子的电子排布式为_______
(2)N2H4、H2O2分子中,各元素的电负性由大到小的顺序为_______ ,第一电离能最大的是_______ 。
(3)一个N2H4分子中含有的σ键数目为_______ ;固态N2H4的晶体类型为_______ 。
(4)H2O2分子结构下图,其中心原子杂化轨道类型为_______ ,H2O2难溶于CS2,原因是_______ 。

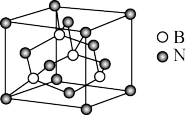
(5)氮化硼是航天航空常用的热屏蔽材料,立方氮化硼晶胞如下图所示,氨氮原子的配位数为_______ ,若该晶胞的密度为ρg•cm-3,阿伏加德罗常数为NA,则两个最近N原子核间的距离为_______ cm。
(1)基态钛原子的电子排布式为
(2)N2H4、H2O2分子中,各元素的电负性由大到小的顺序为
(3)一个N2H4分子中含有的σ键数目为
(4)H2O2分子结构下图,其中心原子杂化轨道类型为

(5)氮化硼是航天航空常用的热屏蔽材料,立方氮化硼晶胞如下图所示,氨氮原子的配位数为

您最近一年使用:0次
2021-03-04更新
|
392次组卷
|
3卷引用:广西河池市高级中学2021-2022学年高三上学期第四次月考化学试题



