解题方法
1 . 铝、锌、铁在人类生产和生活中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Fe2+电子排布式为___ ,Zn的基态原子能级最高的电子的电子云轮廓图形状为___ 。
(2)已知Al的第一电离能为578kJ·mol-1、Mg的第一电离能为740kJ·mol-1,请解释Mg的第一电离能比Al大的原因___ 。
(3)Zn2+可形成[Zn(NH3)6]SO4络合物,1mol[Zn(NH3)6]2+配离子中含σ键___ mol,其阴离子中心原子的杂化方式是___ ,NH3的沸点高于PH3的原因是___ 。
(4)已知Zn2+等过渡元素离子形成的水合离子的颜色如下表所示:
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因:___ 。
(5)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为___ ,其中Fe的配位数为___ 。
(6)Fe和N可组成一种过渡金属氮化物,其晶胞如图所示。六棱柱底边边长为xcm,高为ycm,NA为阿伏加 德罗常数的值,则晶胞的密度为___ g·cm-3(列出计算式即可)。

(1)Fe2+电子排布式为
(2)已知Al的第一电离能为578kJ·mol-1、Mg的第一电离能为740kJ·mol-1,请解释Mg的第一电离能比Al大的原因
(3)Zn2+可形成[Zn(NH3)6]SO4络合物,1mol[Zn(NH3)6]2+配离子中含σ键
(4)已知Zn2+等过渡元素离子形成的水合离子的颜色如下表所示:
| 离子 | Sc3+ | Cr3+ | Fe2+ | Zn2+ |
| 水合离子的颜色 | 无色 | 绿色 | 浅绿色 | 无色 |
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因:
(5)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(6)Fe和N可组成一种过渡金属氮化物,其晶胞如图所示。六棱柱底边边长为xcm,高为ycm,NA为阿伏加 德罗常数的值,则晶胞的密度为

您最近一年使用:0次
2020-06-28更新
|
1995次组卷
|
4卷引用:重庆市江津中学、实验中学等七校2020届高三下学期6月联考(三诊)理科综合化学试题
重庆市江津中学、实验中学等七校2020届高三下学期6月联考(三诊)理科综合化学试题(已下线)2021年高考化学押题预测卷(广东卷)(01)(已下线)2021年高考全国乙卷化学试题变式题2021年广东省高考化学试卷变式题11-21
真题
名校
2 . [化学——选修3:物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在______ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是_____________ 。
(3)CS2分子中,共价键的类型有_____________ ,C原子的杂化轨道类型是_______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______________ 。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____ 晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____ 个六元环,每个六元环占有___ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________ 个六元环,六元环中最多有________ 个C原子在同一平面。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
2016-12-09更新
|
5124次组卷
|
12卷引用:重庆市垫江县2018届高三上学期模底考试理综化学试题
重庆市垫江县2018届高三上学期模底考试理综化学试题2015年全国普通高等学校招生统一考试化学(新课标I卷)2016届广东省深圳第二外国语学校高三上学期第二次教学质检化学试卷2016届黑龙江省哈尔滨一中高三上学期12月月考化学试卷宁夏石嘴山市第三中学2018届高三9月月考化学试题百所名校联考-物质结构与性质云南省曲靖市第一中学2020届高三化学仿真模拟考试理科综合化学试题云南省曲靖一中2020届高考化学仿真试卷河北省石家庄市第二中学2020届高中毕业班四月份教学质量监测卷理科综合化学部分安徽省马鞍山市2020届高考第二次模拟理综化学试题辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题四川省宜宾市第四中学2021届高三上学期开学考试理综化学试题
名校
解题方法
3 . 氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。请回答下列问题:
(1)第一电离能介于B和N之间的第二周期的元素共有________ 种。
(2)基态K+离子电子占据最高能级的电子云轮廓图为_________ 形。
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下BeCl2以双聚分子存在,其结构式为________ ,其中Be原子的电子排布图为_________ 。
(4)四氟硼酸钠(NaBF4)是纺织工业的催化剂。其阴离子的中心原子的杂化轨道类型为_________ 。四氟硼酸钠中存在_______ (填序号):
a. 氢键 b. 范德华力 c. 离子键 d. 配位键 e. σ键 f. π键
(1)第一电离能介于B和N之间的第二周期的元素共有
(2)基态K+离子电子占据最高能级的电子云轮廓图为
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下BeCl2以双聚分子存在,其结构式为
(4)四氟硼酸钠(NaBF4)是纺织工业的催化剂。其阴离子的中心原子的杂化轨道类型为
a. 氢键 b. 范德华力 c. 离子键 d. 配位键 e. σ键 f. π键
您最近一年使用:0次
2020-01-24更新
|
1096次组卷
|
5卷引用:重庆市2022-2023学年高二下学期3月月考化学试题
名校
4 . 离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
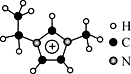
(1)碳原子价层电子的轨道表达式为__________ ,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_________ 形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_______ 。NH3比PH3的沸点高,原因是_________ 。
(3)氮元素的第一电离能比同周期相邻元素都大的原因是____________ 。
(4)EMIM+离子中,碳原子的杂化轨道类型为______ 。分子中的大π键可用符号 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为 ),则EMIM+离子中的大π键应表示为
),则EMIM+离子中的大π键应表示为________ 。
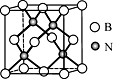
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于_______ 晶体,其中硼原子的配位数为_______ 。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏伽德罗常数的值为NA,则该晶胞中原子的空间利用率为________ (列出化简后的计算式)。

(1)碳原子价层电子的轨道表达式为
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是
(3)氮元素的第一电离能比同周期相邻元素都大的原因是
(4)EMIM+离子中,碳原子的杂化轨道类型为
 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为 ),则EMIM+离子中的大π键应表示为
),则EMIM+离子中的大π键应表示为
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于
您最近一年使用:0次
2019-01-14更新
|
1543次组卷
|
5卷引用:【全国百强校】重庆南开中学高2019届高三下学期4月考试理科综合化学试题
5 . Ⅰ.有机金属化合物的应用研究是目前科学研究的前沿之一,二茂铁[ ]的发现在有机金属化合物研究中具有里程碑意义,它开辟了有机金属化合物研究的新领域。二茂铁分子是一种金属有机配合物,熔点173℃,沸点249℃,100℃以上能升华;不溶于水,易溶于苯、乙醚、汽油等有机溶剂。环戊二烯和二茂铁的结构如下图所示。回答下列问题。
]的发现在有机金属化合物研究中具有里程碑意义,它开辟了有机金属化合物研究的新领域。二茂铁分子是一种金属有机配合物,熔点173℃,沸点249℃,100℃以上能升华;不溶于水,易溶于苯、乙醚、汽油等有机溶剂。环戊二烯和二茂铁的结构如下图所示。回答下列问题。
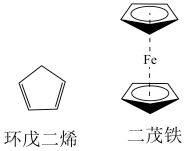
(1)环戊二烯分子中σ键和π键的个数比为_______ 。
(2)下列关于环戊二烯和二茂铁的说法正确的是_______(填字母序号)
(3)环戊二烯能使溴的四氯化碳溶液褪色。写出环戊二烯与足量溴的四氯化碳溶液反应的化学方程式_______ 。
(4)分子或离子团中的大π键可表示为 ,其中m表示参与形成大π键的原子数,n表示参与形成大π键的电子数。已知环戊二烯阴离子(
,其中m表示参与形成大π键的原子数,n表示参与形成大π键的电子数。已知环戊二烯阴离子(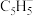 )的结构与苯分子相似,具有芳香性。苯分子中大π键可表示为
)的结构与苯分子相似,具有芳香性。苯分子中大π键可表示为 ,则
,则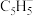 中大π键应表示为
中大π键应表示为_______ 。
Ⅱ.完成下列填空。
(5)有机物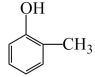 的命名为:
的命名为:_______ 。
(6)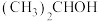 与氧气在铜催化作用下加热的化学方程式是
与氧气在铜催化作用下加热的化学方程式是_______ 。
(7)乙二醇与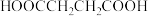 可发生缩聚反应,得到的产物结构简式为
可发生缩聚反应,得到的产物结构简式为_______ 。
 ]的发现在有机金属化合物研究中具有里程碑意义,它开辟了有机金属化合物研究的新领域。二茂铁分子是一种金属有机配合物,熔点173℃,沸点249℃,100℃以上能升华;不溶于水,易溶于苯、乙醚、汽油等有机溶剂。环戊二烯和二茂铁的结构如下图所示。回答下列问题。
]的发现在有机金属化合物研究中具有里程碑意义,它开辟了有机金属化合物研究的新领域。二茂铁分子是一种金属有机配合物,熔点173℃,沸点249℃,100℃以上能升华;不溶于水,易溶于苯、乙醚、汽油等有机溶剂。环戊二烯和二茂铁的结构如下图所示。回答下列问题。
(1)环戊二烯分子中σ键和π键的个数比为
(2)下列关于环戊二烯和二茂铁的说法正确的是_______(填字母序号)
| A.二茂铁晶体是分子晶体 |
| B.环戊烷中含有环戊二烯,可用与氢气反应除去 |
| C.环戊二烯分子中所有原子均在同一个平面上 |
| D.环戊二烯的同分异构体可能是含两个碳碳三键的炔烃 |
(4)分子或离子团中的大π键可表示为
 ,其中m表示参与形成大π键的原子数,n表示参与形成大π键的电子数。已知环戊二烯阴离子(
,其中m表示参与形成大π键的原子数,n表示参与形成大π键的电子数。已知环戊二烯阴离子(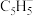 )的结构与苯分子相似,具有芳香性。苯分子中大π键可表示为
)的结构与苯分子相似,具有芳香性。苯分子中大π键可表示为 ,则
,则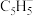 中大π键应表示为
中大π键应表示为Ⅱ.完成下列填空。
(5)有机物
 的命名为:
的命名为:(6)
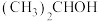 与氧气在铜催化作用下加热的化学方程式是
与氧气在铜催化作用下加热的化学方程式是(7)乙二醇与
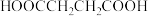 可发生缩聚反应,得到的产物结构简式为
可发生缩聚反应,得到的产物结构简式为
您最近一年使用:0次
名校
6 . 硫和碳及其化合物广泛存在于自然界中,并被人们广泛利用。回答下列问题:
(1)当基态原子的电子吸收能量后,电子会发生____ ,某处于激发态的S原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为__________ 。硫所在周期中,第一电离能最大的元素是___________ 。(填元素符号)
(2)写出一个与CO2具有相同空间结构和键合形式的分子的电子式__________________ 。
(3)H2S中S原子的杂化类型是__________ ;H2S的VSEPR模型名称为_________ ;H2S的键角约为94°,H2O的键角为105°,其原因是___________________________ 。
(4)科学家通过X射线推测胆矾结构示意图1如下:


其中含有________ 个配位键,___________ 个氢键。
(5)已知Zn和Hg同属IIB族元素,火山喷出的岩浆是一种复杂的混合物,冷却时,许多矿物相继析出,其中所含的ZnS矿物先于HgS矿物析出,原因是_________________________________ 。
(6)碳的另一种同素异形体—石墨,其晶体结构如上图2所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为____ 个,已知石墨的密度为pg·cm-1,C-C键长为rcm,阿伏伽德罗常数的值为NA,计算石墨晶体的层间距为____ cm。
(1)当基态原子的电子吸收能量后,电子会发生
(2)写出一个与CO2具有相同空间结构和键合形式的分子的电子式
(3)H2S中S原子的杂化类型是
(4)科学家通过X射线推测胆矾结构示意图1如下:


其中含有
(5)已知Zn和Hg同属IIB族元素,火山喷出的岩浆是一种复杂的混合物,冷却时,许多矿物相继析出,其中所含的ZnS矿物先于HgS矿物析出,原因是
(6)碳的另一种同素异形体—石墨,其晶体结构如上图2所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为
您最近一年使用:0次
2017-05-10更新
|
1410次组卷
|
3卷引用:重庆市巴蜀中学2017届高三下学期期中(三模)考试理科综合化学试题
名校
7 . 近年来我国科学家发现了一系列意义重大的铁系、铜系超导材料,其中一类为Fe-Sm-As-F-O组成的化合物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为______ ,杂化类型为______ ,其沸点比 的
的______ (填“高”或“低”),其判断理由是____________ 。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成,第一电离能:
______ (填“大于”或“小于”) ,原因是
,原因是____________ 。
(3)研究发现,阳离子的颜色与未成对电子数有关。例如: 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是____ 。
(1)元素As与N同族。预测As的氢化物分子的立体结构为
 的
的(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成,第一电离能:

 ,原因是
,原因是(3)研究发现,阳离子的颜色与未成对电子数有关。例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是
您最近一年使用:0次
2023-04-03更新
|
125次组卷
|
2卷引用:重庆市璧山来凤中学校2023-2024学年高二下学期3月月考化学试题
名校
解题方法
8 . 钛、铁、砷、硒、锌等元素的单质及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为_______ ,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有________ 种。
(2)铁的第三电离能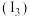 、第四电离能
、第四电离能 分别为
分别为 和
和 ,
, 远大于
远大于 的原因是
的原因是______________________ 。
(3) 离子可用于
离子可用于 的检验,其对应的酸有两种,分别为硫氰酸
的检验,其对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸 。
。
①写出与 互为等电子体的一种微粒
互为等电子体的一种微粒_________  分子或离子
分子或离子 ;
;
②异硫氰酸的沸点比硫氰酸沸点高的原因是_______________ 。
(4)成语“信口雌黄”中的雌黄分子式为 ,分子结构如图1所示,As原子的杂化方式为
,分子结构如图1所示,As原子的杂化方式为_______________ 。

(5)离子化合物 的晶胞结构如图2所示。一个晶胞含有的
的晶胞结构如图2所示。一个晶胞含有的 键有
键有__________ 个。

(6)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为____________  填元素符号
填元素符号 ;该晶胞中硒原子所处空隙类型为
;该晶胞中硒原子所处空隙类型为____________  填“立方体”、“正四面体”或“正八面体”
填“立方体”、“正四面体”或“正八面体” ,该种空隙的填充率为
,该种空隙的填充率为____________ ;若该晶胞密度为 ,硒化锌的摩尔质量为
,硒化锌的摩尔质量为 。用
。用 代表阿伏加 德罗常数的数值,则晶胞参数a为
代表阿伏加 德罗常数的数值,则晶胞参数a为____________ nm。

(1)基态Ti原子中,最高能层电子的电子云轮廓形状为
(2)铁的第三电离能
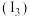 、第四电离能
、第四电离能 分别为
分别为 和
和 ,
, 远大于
远大于 的原因是
的原因是(3)
 离子可用于
离子可用于 的检验,其对应的酸有两种,分别为硫氰酸
的检验,其对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸 。
。①写出与
 互为等电子体的一种微粒
互为等电子体的一种微粒 分子或离子
分子或离子 ;
;②异硫氰酸的沸点比硫氰酸沸点高的原因是
(4)成语“信口雌黄”中的雌黄分子式为
 ,分子结构如图1所示,As原子的杂化方式为
,分子结构如图1所示,As原子的杂化方式为
(5)离子化合物
 的晶胞结构如图2所示。一个晶胞含有的
的晶胞结构如图2所示。一个晶胞含有的 键有
键有
(6)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为
 填元素符号
填元素符号 ;该晶胞中硒原子所处空隙类型为
;该晶胞中硒原子所处空隙类型为 填“立方体”、“正四面体”或“正八面体”
填“立方体”、“正四面体”或“正八面体” ,该种空隙的填充率为
,该种空隙的填充率为 ,硒化锌的摩尔质量为
,硒化锌的摩尔质量为 。用
。用 代表阿伏加 德罗常数的数值,则晶胞参数a为
代表阿伏加 德罗常数的数值,则晶胞参数a为
您最近一年使用:0次
名校
解题方法
9 . 钢化玻璃因其优良的性能广泛应用于日常生活,但由于制作玻璃时里面含有极少量硫化镍,使得钢化玻璃在极限条件下的使用受到限制。
(1)基态硫原子价层电子的轨道表达式 电子排布图
电子排布图 为
为__ ,基态镍原子中核外电子占据最高能层的符号为__ 。
(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为__ 晶体,Ni(CO)4空间构型与甲烷相同,中心原子的杂化轨道类型为__ ,写出与配体互为等电子体的阴离子__  任写一种
任写一种 。
。
(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱__ >__  填化学式
填化学式 ,理由是
,理由是__ 。
(4)H2S的键角__ 填“大于”“小于”“等于”)H2O的键角,请从电负性的角度说明理由__ 。
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的__ 空隙中,已知Ni2+半径为69nm,O2-半径为140nm,阿伏加 德罗常数为NA,NiO晶体的密度为__ g/cm3(只列出计算式 。
。

(1)基态硫原子价层电子的轨道表达式
 电子排布图
电子排布图 为
为(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为
 任写一种
任写一种 。
。(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱
 填化学式
填化学式 ,理由是
,理由是(4)H2S的键角
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的
 。
。
您最近一年使用:0次
10 . 钒(V)固氮酶种类众多,其中种结构如图所示:

(1)基态钒原子的核外电子排布式为________ ,该元素位于元素周期表的第___ 族。
(2)钒固氮酶中钒的配位原子有___ (写元素符号)。
(3)配体CH3CN中碳的杂化类型为____ 所含σ键与π键数目之比为___ 。
(4)配体CH3CN中所涉及元素的电负性由强到弱依次排序为__________ (用元素符号表示)。
(5)写出证明非金属性Cl >S的一个常见离子方程式:__________ 。

(1)基态钒原子的核外电子排布式为
(2)钒固氮酶中钒的配位原子有
(3)配体CH3CN中碳的杂化类型为
(4)配体CH3CN中所涉及元素的电负性由强到弱依次排序为
(5)写出证明非金属性Cl >S的一个常见离子方程式:
您最近一年使用:0次
2020-09-04更新
|
227次组卷
|
2卷引用:重庆市第八中学2018-2019学年高二下学期期中考试化学试题



