名校
解题方法
1 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。请用相关的化学术语回答下列问题:
(1) 在这些元素中,最不活泼的是 ,非金属性最强的是___________,金属性最强的是___________;(填元素符号或化学式,下同。)
(2) 这些元素形成的最高价氧化物对应的水化物中碱性最强的 ,酸性最强的__________;
(3) ①、②、③、④、⑤这五种元素的原子半径由大到小的顺序为 ;
(4) ⑥的氢化物的电子式为 ,① 在空气中燃烧后生成产物的电子式 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA[ | 0 |
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ① | ③ | ④ | ⑧ | ⑨ | |||
| 4 | ② |
(2) 这些元素形成的最高价氧化物对应的水化物中碱性最强的 ,酸性最强的__________;
(3) ①、②、③、④、⑤这五种元素的原子半径由大到小的顺序为 ;
(4) ⑥的氢化物的电子式为 ,① 在空气中燃烧后生成产物的电子式 。
您最近一年使用:0次
解题方法
2 . R元素的单质4.5g,跟足量的硫酸反应生成R2(SO4)3,并放出5.6L的H2(标准状况下).试求:
(1)R的相对原子质量为_____
(2)若R原子中质子数比中子数少1,则R是(填元素符号)_____ ,它在元素周期表的位置为第_____ 周期第_____ 族.
(1)R的相对原子质量为
(2)若R原子中质子数比中子数少1,则R是(填元素符号)
您最近一年使用:0次
解题方法
3 . 表中所列字母分别代表一种元素。
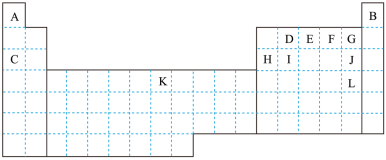
(1)G的气态氢化物比J的气态氢化物_______ (填“稳定”或“不稳定”)。
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为_______ ;该物质溶于水后的溶液呈_______ 性(填“酸”、“碱”或“中”)。
(3)元素C和H的最高价氧化物对应的水化物相互反应的离子方程式为:_______ 。
(4)元素G和L的原子序数相差:_______ ,它们的氢化物的水溶液酸性相对强的是:_______ (填化学式)
(5)表中A和F两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为:_______
(6)K为生产、生活中应用最广泛的金属,通常采用的冶炼方法为:_______

(1)G的气态氢化物比J的气态氢化物
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为
(3)元素C和H的最高价氧化物对应的水化物相互反应的离子方程式为:
(4)元素G和L的原子序数相差:
(5)表中A和F两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为:_______
| A.MnO2 | B.Na2SO4 | C.FeCl3 | D.KMnO4 |
| A.电解法 | B.热分解法 | C.热还原法 |
您最近一年使用:0次
解题方法
4 . 下表为周期表的一部分,其中的编号代表对应的元素.

请回答下列问题:
(1)表中属于d区的元素是_____________ (填编号)。
(2)写出元素⑨的基态原子的电子排布式_____________ ;
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为_____________ 对,其单质的电子式为_____________ ;
(4)元素④的氢化物的分子构型为_____________ ,中心原子的杂化方式为_____________ ;
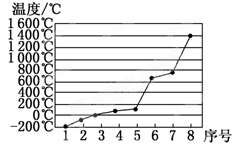
(5)第3周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表_____________ (填元素符号);其中电负性最大的是_____________ (填图中的序号)。

请回答下列问题:
(1)表中属于d区的元素是
(2)写出元素⑨的基态原子的电子排布式
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为
(4)元素④的氢化物的分子构型为
(5)第3周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表

您最近一年使用:0次
解题方法
5 . 现有10种元素的性质、数据如下表所列,它们均为短周期元素.
回答下列问题:
(1)D的元素名称是_______ ,H的元素符号是_______ ,B在元素周期表中的位置是(周期、族)_______ 。
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是_______ .化合物F2A2的电子式是:_______ ,构成该物质的化学键类型为_______ 。
(3)用电子式表示A的简单氢化物的形成过程如下:_______ ;G的氢化物的结构式为_______ 。
(4)一定条件下,IA2气体与足量的A单质充分反应生成20 g气态化合物,放出24.6 kJ热量,写出其热化学方程式_______ 。
(5)用J元素的单质与A元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的惰性电极甲和乙浸入KOH溶液,在甲极通入J的单质,乙极通入A的单质,则甲极的电极反应式为:_______ 。
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10﹣10m) | 0.74 | 1.60 | 1.52 | 1.10[ | 0.99 | 1.86 | 0.75 | 0.82 | 0.102 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5[ | +7 | +1 | +5 | +3 | +6 | +1 | |
| ﹣2 | ﹣3 | ﹣1 | ﹣3 | ﹣2 |
(1)D的元素名称是
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)用电子式表示A的简单氢化物的形成过程如下:
(4)一定条件下,IA2气体与足量的A单质充分反应生成20 g气态化合物,放出24.6 kJ热量,写出其热化学方程式
(5)用J元素的单质与A元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的惰性电极甲和乙浸入KOH溶液,在甲极通入J的单质,乙极通入A的单质,则甲极的电极反应式为:
您最近一年使用:0次
解题方法
6 . 五种短周期元素A、B、C、D、E的原子序数依次增大,其中只有C为金属元素。A和C同主族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是__________ ,非金属性最强的是__________ (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是__________ (用化学式表示);
(3)D在周期表的位置为__________
(4)A和B形成的化合物与A和E形成的化合物反应,产物的化学式为__________ ,该化合物溶于水,显__________ 性(填“酸”、“碱”、“中”)原因是__________ (用离子方程式表示);
(5)D和E可形成一种所有原子都满足8电子结构的化合物,其化学式为__________ 。
(1)五种元素中,原子半径最大的是
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)D在周期表的位置为
(4)A和B形成的化合物与A和E形成的化合物反应,产物的化学式为
(5)D和E可形成一种所有原子都满足8电子结构的化合物,其化学式为
您最近一年使用:0次
解题方法
7 . 如表所示为元素周期表的一部分,参照元素①~⑨在表中的位置,请回答下列问题:
(1)周期表中元素最高正价与最低价代数和为零的是______________ 族(用族序号表示)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_______________ (用酸的化学式表示)。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式______________________ ;
(4)已知周期表中存在对角相似规则,如铍(Be)与铝化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式__________________ 。
(5)已知W+X=Y+Z(反应需要加热,),W、X、Y、Z分别是由①②⑨三种元素形成的四种十电子粒子(W、X为离子,Y、Z为分子),写出该化学方程式_______________________ 。
(6)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
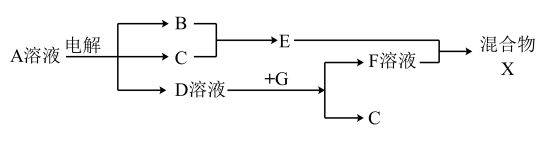
①写出D溶液与G反应的化学方程式_______________________ 。
②写出检验A溶液中溶质的阴离子的方法___________________________ 。
(1)周期表中元素最高正价与最低价代数和为零的是
(2)⑥和⑦的最高价含氧酸的酸性强弱为
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑧ | ⑨ | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(5)已知W+X=Y+Z(反应需要加热,),W、X、Y、Z分别是由①②⑨三种元素形成的四种十电子粒子(W、X为离子,Y、Z为分子),写出该化学方程式
(6)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出D溶液与G反应的化学方程式
②写出检验A溶液中溶质的阴离子的方法
您最近一年使用:0次
解题方法
8 . 已知两种相邻周期、相邻主族的短周期非金属元素X、Y,其最高价氧化物对应的水化物均为强酸。根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
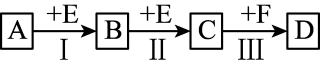
(1)若A、B、C、D均为含X元素的化合物,且A和F的分子均为10电子微粒,则:
①F属于________ (填“离子化合物”或“共价化合物”)。
②反应Ⅰ的化学方程式为______________________________ 。
③将1.92 g铜粉与一定量的D的浓溶液反应,当铜完全反应时收集到气体1.12 L(标准状况),则反应耗的D的物质的量为________ mol。
(2)若A、B、C、D均为含Y元素的化合物,其中A由两种元素组成,且A的摩尔质量为34 g·mol-1,则:①将铜粉与D的浓溶液反应所得溶液加热蒸干,得的白色固体物质为________ (填化学式)。
②将少量Na2Y溶液滴加到次氯酸钠溶液中发生应,无沉淀生成,请写出该反应的离子方程式__________________ 。在该反中若有74.5 g NaClO被还原,则转移电子的物质量为________ mol。
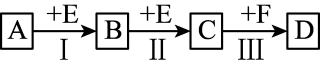
(1)若A、B、C、D均为含X元素的化合物,且A和F的分子均为10电子微粒,则:
①F属于
②反应Ⅰ的化学方程式为
③将1.92 g铜粉与一定量的D的浓溶液反应,当铜完全反应时收集到气体1.12 L(标准状况),则反应耗的D的物质的量为
(2)若A、B、C、D均为含Y元素的化合物,其中A由两种元素组成,且A的摩尔质量为34 g·mol-1,则:①将铜粉与D的浓溶液反应所得溶液加热蒸干,得的白色固体物质为
②将少量Na2Y溶液滴加到次氯酸钠溶液中发生应,无沉淀生成,请写出该反应的离子方程式
您最近一年使用:0次
解题方法
9 . A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的离子不含电子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与 E同周期;E元素原子的最外层电子数是其次外层电子数的 3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
(1)E元素在元素周期表中的位置是_______________ 。
(2)由A、B、C三种元素形成的离子化合物的化学式为_________________ 。
(3)A可分别与C、E形成甲、乙两种三原子分子,且甲有18个电子、乙有10个电子,甲与乙比较,沸点较高的是(填化学式)_______________ 。
(4)F含有的化学键类型是___________ 和_____________ ,其水溶液呈酸性,请用相关的离子方程式解释其原因___________ 。
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为______ 。
(1)E元素在元素周期表中的位置是
(2)由A、B、C三种元素形成的离子化合物的化学式为
(3)A可分别与C、E形成甲、乙两种三原子分子,且甲有18个电子、乙有10个电子,甲与乙比较,沸点较高的是(填化学式)
(4)F含有的化学键类型是
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为
您最近一年使用:0次
解题方法
10 . 已知A、B、C、D四种元素分别为短周期元素,表示中三个不同短周期的主族元素,且原子序数依次增
大。D原子的质子数是B原子质子数的2倍,A原子与D原子的最外层电子数之和是B原子与C原子质子
数之和的1/3。A与B可形成BA3型化合物,该化合物与C的单质在一定条件下反应,能生成化合物BC,请按要求填写下列空白:
(1)D元素的名称____________ ,C元素在元素周期表中的位置_____________ 。
(2)写出BA3的电子式____________ ,BA3跟C的单质在一定条件下反应,能生成化合物BC的化学方程式________________________________ 。
(3)D单质在工业上最重要的用途是_________ ,写出工业上制取D单质的化学方程式__________ 。
(4)在实验室中B的最高价氧化物的水化物的浓溶液应如何保存__________________ ,用化学方程
式说明理由____________________________________ 。
大。D原子的质子数是B原子质子数的2倍,A原子与D原子的最外层电子数之和是B原子与C原子质子
数之和的1/3。A与B可形成BA3型化合物,该化合物与C的单质在一定条件下反应,能生成化合物BC,请按要求填写下列空白:
(1)D元素的名称
(2)写出BA3的电子式
(3)D单质在工业上最重要的用途是
(4)在实验室中B的最高价氧化物的水化物的浓溶液应如何保存
式说明理由
您最近一年使用:0次



