解题方法
1 . 硫元素有多种化合价,如图表示了含硫物质(甲~辛)与硫的化合价及相应物质类别物质类别之间的关系。
回答下列问题:
(1)物质甲的分子式为_______ 。
(2)物质丙排入空气中是形成酸雨的主要原因之一,工业上要除去废气中的丙,下列物质中最适宜的是_________ (填标号)。
A.烧碱 B.生石灰 C.活性炭 D.明矾
(3)从图中选择一种物质将乙转化为丙,写出反应的化学方程式:______ 。
| 物质类别 | ||||||
| 盐 | 戊 | 辛 | ||||
| 含氧酸 | 丁 | 庚 | ||||
| 氧化物 | 丙 | 己 | ||||
| 单质 | 乙 | |||||
| 氢化物 | 甲 | |||||
| -2 | 0 | +2 | +4 | +6 | 化合价 |
(1)物质甲的分子式为
(2)物质丙排入空气中是形成酸雨的主要原因之一,工业上要除去废气中的丙,下列物质中最适宜的是
A.烧碱 B.生石灰 C.活性炭 D.明矾
(3)从图中选择一种物质将乙转化为丙,写出反应的化学方程式:
您最近一年使用:0次
名校
解题方法
2 . 完成下列问题。
(1)指出溴在周期表中的位置:_ ,属于_ 区。
(2)用二氧化碳生产化工产品,有利于二氧化碳的大量回收。二氧化碳和乙二醇在ZnO或锌盐催化下可合成碳酸乙烯酯。
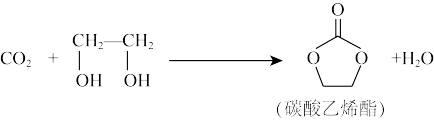
碳酸乙烯酯中碳原子杂化轨道类型为____ ;1mol碳酸乙烯酯中含有的 键数目为
键数目为____ 。
(3)苯胺( )与甲苯(
)与甲苯(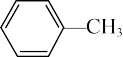 )的相对分子质量相近,但苯胺的熔点、沸点分别高于甲苯的熔点、沸点,原因是
)的相对分子质量相近,但苯胺的熔点、沸点分别高于甲苯的熔点、沸点,原因是_____ 。
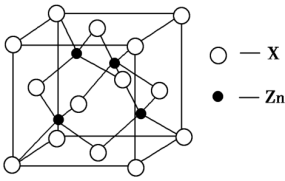
(4)下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为__ 。
(1)指出溴在周期表中的位置:
(2)用二氧化碳生产化工产品,有利于二氧化碳的大量回收。二氧化碳和乙二醇在ZnO或锌盐催化下可合成碳酸乙烯酯。

碳酸乙烯酯中碳原子杂化轨道类型为
 键数目为
键数目为(3)苯胺(
 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的熔点、沸点分别高于甲苯的熔点、沸点,原因是
)的相对分子质量相近,但苯胺的熔点、沸点分别高于甲苯的熔点、沸点,原因是(4)下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为

您最近一年使用:0次
名校
解题方法
3 . 元素周期表是学习和研究化学的重要工具。
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
①Al原子的核电荷数为____ 。②钠离子的结构示意图为____ 。
③周期表中磷元素的有关信息为 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是____ 。
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。
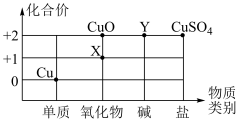
①写出物质 X 的化学式:________________ 。
②写出由物质 Y 转化为 CuSO4的化学反应方程式:_______________ 。
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是_________________ 。
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
| 第1周期 | H | He | ||||||
| 第2周期 | Li | Be | B | C | N | O | F | Ne |
| 第3周期 | Na | Mg | Al | Si | P | S | Cl | Ar |
①Al原子的核电荷数为
③周期表中磷元素的有关信息为
 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。

①写出物质 X 的化学式:
②写出由物质 Y 转化为 CuSO4的化学反应方程式:
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
您最近一年使用:0次
名校
解题方法
4 . 短周期中的三种元素X、Y、Z的原子序数依次减小,三种元素原子核外电子层数之和是5,X元素原子的最外层电子数是Y和Z两元素原子的最外层电子数的总和;Y元素原子的最外层电子数是它的电子层数的2倍,且Y元素最高正价与最低负价的绝对值相等,X和Z可以形成XZ3的化合物。请回答:
(1)X、Y、Z三种元素的元素符号分别为X_____ ,Y_____ ,Z______ ;
(2)元素X的原子得电子能力__ (填"强于"或"弱于")元素Y的原子,用最简单的实验验证(用化学方程式表示)__
(3)XZ3的电子式是_______ ;
(4)写出向XZ3的水溶液中通入过量Y的最高价氧化物反应的化学方程式______ 。
(1)X、Y、Z三种元素的元素符号分别为X
(2)元素X的原子得电子能力
(3)XZ3的电子式是
(4)写出向XZ3的水溶液中通入过量Y的最高价氧化物反应的化学方程式
您最近一年使用:0次
5 . 某元素原子的电子排布式为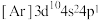 ,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
(1)该元素处于元素周期表的第______ 周期,该周期的元素种数是______ ;
(2)该元素处于元素周期表的第______ 族,该族的非金属元素种数是______ 。
(3)试推测该元素处于元素周期表的______ 区,该区包含族的种类是______ 。
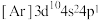 ,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:(1)该元素处于元素周期表的第
(2)该元素处于元素周期表的第
(3)试推测该元素处于元素周期表的
您最近一年使用:0次
名校
6 . 如图是元素周期表的另一种画法——塔式周期表,在上面标有部分族及部分元素。请回答下列问题:

(1)请在图上把过渡元素涂黑。_______
(2)已知A、B、C、D、E、F、G为元素周期表中短周期主族元素,且原于序数依次增大。A与E、D与F分别同主族,E、F、G同周期;A与D形成的化合物常温下为液态;B原子最外层电子数是次外层电子数的两倍。请回答下列问题:
①在如图塔式周期表相应位置标出上述属于碱金属和卤族元素的元素符号。____
②写出E与D形成含有非极性键化合物的电子式______ 。
③这些元素形成的最简单氢化物中,属于18电子的分子有____ (写化学式)
④A、D的单质和A、D、E形成的离子化合物的水溶液,在一定条件下可构成原电池,其中D的单质在___ 极发生反应,原电池反应中,A单质发生反应的电极反应式为_______ 这种电池相对于其它电池的优点是________ 。

(1)请在图上把过渡元素涂黑。
(2)已知A、B、C、D、E、F、G为元素周期表中短周期主族元素,且原于序数依次增大。A与E、D与F分别同主族,E、F、G同周期;A与D形成的化合物常温下为液态;B原子最外层电子数是次外层电子数的两倍。请回答下列问题:
①在如图塔式周期表相应位置标出上述属于碱金属和卤族元素的元素符号。
②写出E与D形成含有非极性键化合物的电子式
③这些元素形成的最简单氢化物中,属于18电子的分子有
④A、D的单质和A、D、E形成的离子化合物的水溶液,在一定条件下可构成原电池,其中D的单质在
您最近一年使用:0次
9-10高一下·浙江金华·期中
解题方法
7 . 前20号元素A、B、C、D,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)D元素的名称____________ ; B元素的原子结构示意图________________ ;
(2)C在周期表中的位置___________ ;
(3)化合物D2C的电子式_____________ ;
(4)B的氢化物的水溶液加入B的最高价氧化物对应水化物的稀溶液,反应的离子方程式为:_____ ;
(5)有人认为,A单质是一种优质能源,你认为它作为能源的优点是:____ 。
(1)D元素的名称
(2)C在周期表中的位置
(3)化合物D2C的电子式
(4)B的氢化物的水溶液加入B的最高价氧化物对应水化物的稀溶液,反应的离子方程式为:
(5)有人认为,A单质是一种优质能源,你认为它作为能源的优点是:
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X的单质是一种理想能源,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为__________ 。
(2)上述元素中,非金属气态氢化物还原性最强的是_________ (写化学式);Y和Z形成的含有共价键的化合物的电子式为_________ 。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有_________ 。(写出其中两种物质的化学式)
(4)ZX与水剧烈反应产生X的单质,其化学方程式为_________ 。
(1)Y在元素周期表中的位置为
(2)上述元素中,非金属气态氢化物还原性最强的是
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有
(4)ZX与水剧烈反应产生X的单质,其化学方程式为
您最近一年使用:0次
名校
9 . 下表中的实线表示元素周期表的部分边界,a-1分别表示周期表中对应位置的元素。
(1)请在上表中用实线补全元素周期表边界____ 。
(2)表中所列元素,不属于短周期元素有____ ,不属于主族元素的有___ (填相应的元素符号)
(3)指出下列元素在周期表中的位置:
①b元素位于第___ 周期___ 族;
②g元素位于第___ 周期___ 族;
③l元素位于第___ 周期___ 族;
(4)①写出b与c的化合物(温室气体)电子式:___________ ;
②用电子式表示k与h化合物形成过程:__________ 。
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | f | g | h | ||||||||||||||
| k | l | ||||||||||||||||
(2)表中所列元素,不属于短周期元素有
(3)指出下列元素在周期表中的位置:
①b元素位于第
②g元素位于第
③l元素位于第
(4)①写出b与c的化合物(温室气体)电子式:
②用电子式表示k与h化合物形成过程:
您最近一年使用:0次
10-11高二下·河北邢台·期中
解题方法
10 . 化合物YX2、ZX2中,X、Y、Z都是短周期元素,X与Y为同周期元素,Y与Z为同族元素,Y原子的最外层p能级电子数等于前一电子层电子总数。X原子最外层p能级中只有一个轨道填充了2个电子,则X的电子排布式为___________ ;Y的简化电子排布式为___________ ;Z的电子排布式为____________ ;YX2的化学式是________ ,电子式是________ ;ZX2的化学式是________ 。
您最近一年使用:0次



