名校
1 . 如表为长式周期表的一部分,其中的编号代表对应的元素。
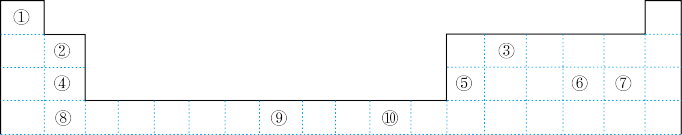
请回答下列问题:
(1)表中属于d区的元素是_______ (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为_______ 。
(3)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为_______ ;该元素与元素①形成的分子X的立体构型为_______ ,与⑧在同一周期的元素中的未成对电子数目最多的元素的价电子排布式是_______ 。
(5)某些不同族元素的性质也有一定的相似性,如表中元素⑤与元素②的氢氧化物有相似的性质,请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_______ 。

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为
(5)某些不同族元素的性质也有一定的相似性,如表中元素⑤与元素②的氢氧化物有相似的性质,请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
名校
2 . 元素周期表是重要的化学学习工具。随着原子序数变化,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
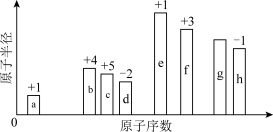
(1)b在元素周期表中的位置是_______ 周期_______ 族。
(2)8种元素中金属性最强的是_______ (用元素符号表示),b和c的最高价氧化物的水化物中,酸性较强的是_______ (用化学式表示)。
(3)c、h两种元素电负性相近,在不同的电负性标度下其大小关系不同,写出由两者组成的化合物按照c:h=1:3形成的化合物的电子式:_______ 。
(4)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,Be及其化合物与f单质及其化合物的性质相似,写出Be的最高价氧化物对应的水化物与e的最高价氧化物对应的水化物反应的离子方程式:_______ 。

(1)b在元素周期表中的位置是
(2)8种元素中金属性最强的是
(3)c、h两种元素电负性相近,在不同的电负性标度下其大小关系不同,写出由两者组成的化合物按照c:h=1:3形成的化合物的电子式:
(4)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,Be及其化合物与f单质及其化合物的性质相似,写出Be的最高价氧化物对应的水化物与e的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
2022-11-11更新
|
135次组卷
|
2卷引用:安徽省安庆市第二中学2022-2023学年高三上学期11月月考化学试题
3 . 下列8种化学符号: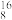 O2、
O2、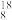 O2、
O2、 H、
H、 C、
C、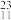 Na、
Na、 N、
N、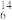 C、
C、 Mg。
Mg。
(1)表示核素的符号共_______ 种。
(2)互为同位素的是_______ 。
(3)质量相同的H216O和D216O所含中子数之比为_______ 。
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:Be(OH)2与Mg(OH)2可用_______ 试剂鉴别。
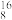 O2、
O2、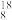 O2、
O2、 H、
H、 C、
C、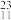 Na、
Na、 N、
N、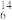 C、
C、 Mg。
Mg。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:Be(OH)2与Mg(OH)2可用
您最近一年使用:0次
名校
解题方法
4 . 我国科学家曾通过测量石英中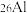 和
和 两种核素的比例确定“北京人”年龄,这种测量方法叫“铝铍埋藏测年法”。下列说法正确的是
两种核素的比例确定“北京人”年龄,这种测量方法叫“铝铍埋藏测年法”。下列说法正确的是
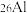 和
和 两种核素的比例确定“北京人”年龄,这种测量方法叫“铝铍埋藏测年法”。下列说法正确的是
两种核素的比例确定“北京人”年龄,这种测量方法叫“铝铍埋藏测年法”。下列说法正确的是| A.工业上常采用电解熔融氯化铝的方法获得金属铝 |
B. 和 和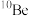 具有相同的化学性质,因此可用 具有相同的化学性质,因此可用 代替 代替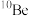 完成“铝铍埋藏测年法” 完成“铝铍埋藏测年法” |
| C.世界卫生组织国际癌症研究机构公布的致癌物清单中铝制品属一类致癌物,因此日常生活中要严禁使用铝制品 |
| D.铍和铝在元素周期表中的位置特点决定了它们具有相似的化学性质,故氢氧化铍也为两性氢氧化物 |
您最近一年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
5 . 下列各组离子中,可能能在所处环境中大量共存的是
A.在室温环境下c(OH-)=1×10-11的溶液中:Cr2+,SO ,NO ,NO ,Na+ ,Na+ |
B.在4℃的水溶液中:Be2+,K+,PO ,OH- ,OH- |
C.在漂白液中:OH-,Rb+,SO ,CO ,CO |
| D.在水玻璃中:H+,SCN-,Cl-,Cs+ |
您最近一年使用:0次
解题方法
6 . 下列关于原子结构和性质的叙述中,正确的为
①2p、3p、4p能级的轨道数依次增多
②ds区全部是金属元素
③在一个原子轨道中最多能容纳2个电子且自旋相反,称为洪特规则
④Be和Al在化学性质上具有一定的相似性
⑤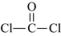 中的σ键与π键个数比为1:3
中的σ键与π键个数比为1:3
①2p、3p、4p能级的轨道数依次增多
②ds区全部是金属元素
③在一个原子轨道中最多能容纳2个电子且自旋相反,称为洪特规则
④Be和Al在化学性质上具有一定的相似性
⑤
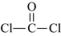 中的σ键与π键个数比为1:3
中的σ键与π键个数比为1:3| A.②④ | B.①②④ | C.②④⑤ | D.③④⑤ |
您最近一年使用:0次
22-23高二上·浙江·期末
解题方法
7 . 下列“类比”结果正确的是
| A.H2S晶体中一个H2S分子周围有12个H2S紧邻,则冰中一个水分子周围也有12个紧邻分子 |
| B.AlCl3中Al原子是sp2杂化,则Al2Cl6中Al原子也是sp2杂化 |
| C.Mg在过量氧气中燃烧生成MgO,则锂在过量氧气燃烧也生成Li2O |
| D.乙醇CH3CH2OH能与水互溶,则戊醇CH3CH2CH2CH2CH2OH也能与水互溶 |
您最近一年使用:0次
8 . 下列说法错误的是
A.BF3和BF 的中心原子杂化方式不同 的中心原子杂化方式不同 |
B. 和 和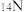 的质量数相等,它们互为同位素 的质量数相等,它们互为同位素 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
D.根据对角线规则, 是弱酸 是弱酸 |
您最近一年使用:0次
2022-09-26更新
|
53次组卷
|
2卷引用:河南省商城县观庙高级中学2021-2022学年高二下学期第一次月考化学试题
9 . 元素周期表中,B与Si处于对角线位置,性质相似。下列推断不合理的是
| A.硅酸为弱酸,可推断硼酸为弱酸 |
B. ,可推断 ,可推断 |
C. 还原能力强,空气中自燃,可推断 还原能力强,空气中自燃,可推断 还原能力强,空气中自燃 还原能力强,空气中自燃 |
| D.Si原子最外层有4个电子,可推断B原子最外层有4个电子 |
您最近一年使用:0次
2022-09-21更新
|
145次组卷
|
3卷引用:湖北省黄冈市2022-2023学年高三上学期9月调研考试化学试题
湖北省黄冈市2022-2023学年高三上学期9月调研考试化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题6-10)陕西省西安市2023-2024学年高二下学期4月期中联考化学试题
名校
10 . W、X、Y、Z、M、R、Q均为短周期主族元素,其原子序数与原子半径关系如图所示。

请回答下列问题:
(1)R在元素周期表中的位置是_______ ;X的质量数分别为16和18的两种核素互为_______ 。
(2)Z与X形成的原子个数比为1:1的化合物与水反应的化学方程式为_______ 。
(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,W单质及其化合物与M单质及其化合物的性质相似,写出W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式_______ 。
(4)用电子式表示 形成过程
形成过程_______ , 与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式_______ 。

请回答下列问题:
(1)R在元素周期表中的位置是
(2)Z与X形成的原子个数比为1:1的化合物与水反应的化学方程式为
(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,W单质及其化合物与M单质及其化合物的性质相似,写出W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式
(4)用电子式表示
 形成过程
形成过程 与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
您最近一年使用:0次



