1 . 在元素周期表中,某些主族元素与其右下方的主族元素的有些性质是相似的,这称为“对角线规则”。根据“对角线规则”,下列有关推断错误的是
| A.BeO是两性氧化物 |
B.Li在空气中燃烧可生成 和 和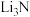 |
C.B的最高价氧化物对应的水化物为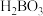 |
D.碱性: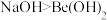 |
您最近一年使用:0次
名校
2 . 运用元素周期律分析下面的推断,其中正确的是
| A.硒化氢是无色、有毒、比硫化氢稳定的气体 |
| B.LiOH是极易溶于水的强碱 |
| C.硫酸镭是易溶于水的白色固体 |
| D.锗单质是一种优良的半导体材料 |
您最近一年使用:0次
解题方法
3 . 元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是


A. 是离子化合物 是离子化合物 | B.Li在空气中燃烧生成 、 、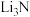 |
C. 是两性氢氧化物 是两性氢氧化物 | D.硼酸是弱酸 |
您最近一年使用:0次
名校
解题方法
4 . 硼是第IIIA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题:
(1)B的第一电离能比Be低,原因是_______ ,按照“对角线规则”,硼的性质应该和_______ (填元素符号)相似,因此晶体硼的晶体类型是_______ 。
(2)氢气的安全贮存和运输是氢能应用的关键,氨硼烷(H3NBH3)是目前颇具潜力的储氢材料之一
①氨硼烷能溶于水,其主要原因是_______ 。
②氨硼烷热分解放氢,能生成一种环状的平面分子(B3N3H6),该分子的结构式为_______ 。
③分子之间除范德华力外,还有可能形成氢键,处于不同环境中氢原子也有可能显不同的电性,此时带相反电性的两个氢原子会形成一种新的作用力,叫双氢键,氨硼烷分子间既能形成氢键又能形成双氢键。下列选项中表示氨硼烷分子间的氢键的是_______ (填标号,下同),表示氨硼烷分子间的双氢键的是_______ 。
a.H-B…H-B b.B-H…H-B c.N-H…H-N d.H-N…H-N
e.H-N…H-B f.B-H…H-N g.H-B…H-N
(3)硼氢化钠(NaBH4)是一种常用的还原剂,其晶胞结构如图所示。
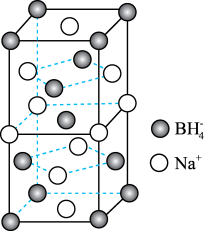
①Na+的配位数是_______ 。
②若晶胞的上、下底面心处的Na+被Li+取代,得到晶体的化学式为_______ 。
③已知硼氢化钠晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值,则Na+与BH 之间的最近距离为
之间的最近距离为_______ (用含ρ、NA的代数式表示)nm。
(1)B的第一电离能比Be低,原因是
(2)氢气的安全贮存和运输是氢能应用的关键,氨硼烷(H3NBH3)是目前颇具潜力的储氢材料之一
①氨硼烷能溶于水,其主要原因是
②氨硼烷热分解放氢,能生成一种环状的平面分子(B3N3H6),该分子的结构式为
③分子之间除范德华力外,还有可能形成氢键,处于不同环境中氢原子也有可能显不同的电性,此时带相反电性的两个氢原子会形成一种新的作用力,叫双氢键,氨硼烷分子间既能形成氢键又能形成双氢键。下列选项中表示氨硼烷分子间的氢键的是
a.H-B…H-B b.B-H…H-B c.N-H…H-N d.H-N…H-N
e.H-N…H-B f.B-H…H-N g.H-B…H-N
(3)硼氢化钠(NaBH4)是一种常用的还原剂,其晶胞结构如图所示。

①Na+的配位数是
②若晶胞的上、下底面心处的Na+被Li+取代,得到晶体的化学式为
③已知硼氢化钠晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值,则Na+与BH
 之间的最近距离为
之间的最近距离为
您最近一年使用:0次
2022-04-27更新
|
112次组卷
|
3卷引用:山西省临汾市部分学校2021-2022学年高二下学期期中联考化学试题
名校
解题方法
5 . “类推”是一种重要的学习方法。下列类推的结论与事实不相符的是
A.由 微溶于水,推知 微溶于水,推知 微溶于水 微溶于水 |
B.由 有两性,推知 有两性,推知 有两性 有两性 |
C.由 与水反应生成HCl和HClO,推知 与水反应生成HCl和HClO,推知 与水反应生成HF和HFO 与水反应生成HF和HFO |
| D.由N元素的最高正价是+5,推知P元素的最高正价是+5 |
您最近一年使用:0次
2022-04-27更新
|
413次组卷
|
4卷引用:四川省成都市蓉城名校联盟2021-2022学年高一下学期期中联考化学试题
名校
解题方法
6 . 我国科学家合成单核钬复合物 ,即
,即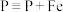 (单原子)→
(单原子)→ 。
。 类似
类似 。下列说法错误的是
。下列说法错误的是
 ,即
,即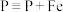 (单原子)→
(单原子)→ 。
。 类似
类似 。下列说法错误的是
。下列说法错误的是A. 类似 类似 能体现周期表中磷和碳的对角关系 能体现周期表中磷和碳的对角关系 |
B. 含 含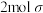 键和 键和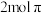 键 键 |
C. 中 中 键键能小于 键键能小于 中 中 键键能 键键能 |
D. 中Fe提供的空轨道和P提供的孤电子对形成配位键 中Fe提供的空轨道和P提供的孤电子对形成配位键 |
您最近一年使用:0次
2022-04-25更新
|
158次组卷
|
2卷引用:湖南省长沙市长郡中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
7 . 铍(4Be)的右下角元素是铝,根据“对角线规则”,下列描述不正确的
| A.BeO是两性氧化物 |
| B.Be(OH)2既能与H2SO4溶液反应也能与NaOH溶液反应 |
| C.Be(OH)2与NaOH溶液反应后生成Na2BeO2和H2O |
| D.BeCl2是离子化合物 |
您最近一年使用:0次
名校
8 . 磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用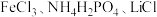 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是_______ ,该元素基态原子核外M层电子的自旋状态_______ (填“相同”或“相反”)。
(2) 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的
中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的 的结构式为
的结构式为_______ ,其中Fe的配位数为_______ 。
(3)苯胺(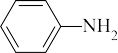 )的晶体类型是
)的晶体类型是_______ 。
(4) 中,电负性最高的元素是
中,电负性最高的元素是_______ ;P的_______ 杂化轨道与O的2p轨道形成_______ 键。
(5) 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:

这类磷酸根离子的化学式可用通式表示为_______ (用n代表P原子数)。
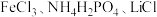 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:(1)在周期表中,与Li的化学性质最相似的邻族元素是
(2)
 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的
中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的 的结构式为
的结构式为(3)苯胺(
 )的晶体类型是
)的晶体类型是(4)
 中,电负性最高的元素是
中,电负性最高的元素是(5)
 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
这类磷酸根离子的化学式可用通式表示为
您最近一年使用:0次
2022-04-22更新
|
135次组卷
|
2卷引用:福建省德化第一中学2021-2022学年高二下学期第一次质检化学试题
9 . 在元素周期表中的某些元素之间存在着特殊的“对角线规则”,如Li和Mg、Be和Al、B和Si的一些性质相似。下列说法不正确的是
| A.氢氧化铍是两性氢氧化物 | B.B和Si的电负性数值相近 |
| C.Li在N2中燃烧生成Li3N | D.Li和Mg的原子半径相近,且核外电子排布相同 |
您最近一年使用:0次
10 . 类推是学习化学的一种重要方法,下列类推正确的是
| A.碳酸钠易溶于水,故碳酸锂也易溶于水 |
| B.H2CO3可以溶于水,故H2SiO3也可以溶于水 |
| C.金属Li通常保存在石蜡里,故金属钠也能保存在石蜡里 |
| D.Cu在室温下以固态的形式存在,故Hg在室温下也以固态的形式存在 |
您最近一年使用:0次
2022-04-19更新
|
133次组卷
|
2卷引用:河南省豫北名校2021-2022学年高二年级下学期联考(三)化学试卷



