名校
解题方法
1 . 化合物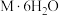 可用作洗涤粉,M的结构如下,其中X、Y、Z、W是原子序数依次增大的短周期主族元素,下列说法
可用作洗涤粉,M的结构如下,其中X、Y、Z、W是原子序数依次增大的短周期主族元素,下列说法错误 的是
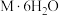 可用作洗涤粉,M的结构如下,其中X、Y、Z、W是原子序数依次增大的短周期主族元素,下列说法
可用作洗涤粉,M的结构如下,其中X、Y、Z、W是原子序数依次增大的短周期主族元素,下列说法
| A.Y的基态原子核外电子排布中有1个未成对电子 |
| B.X、Y、Z、W元素中电负性最大的是Z |
| C.Z、W形成的化合物中可能含有共价键 |
D.X、Z形成的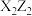 分子的空间构型是直线形 分子的空间构型是直线形 |
您最近半年使用:0次
2024-03-21更新
|
251次组卷
|
2卷引用:安徽省合肥市第一中学2023-2024学年高二下学期素质拓展(2)化学试题
名校
解题方法
2 . 化合物A可应用于清洁剂、化妆品、杀虫剂,结构简式如图所示,W、X、Y、Z分属三个短周期的主族元素且原子序数依次增大,X最高价氧化物对应的水化物为弱酸,Y是地壳中含量最多的元素,下列说法错误的是
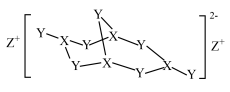

| A.Y与Z形成的两种化合物阴阳离子比均为1:2 |
| B.电负性大小关系为:Y>W>X>Z |
| C.Y基态原子核外电子有5种空间运动 |
| D.化合物A的阴离子中所有原子均满足8电子稳定结构 |
您最近半年使用:0次
解题方法
3 . 已知A为淡黄色固体,T、R为日常生活中两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M。
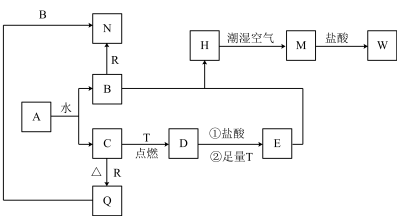
(1)写出下列物质的化学式:A:___________ ,D:___________ ,W:___________ 。
(2)按要求写出下列方程式:
①B和Q反应的离子方程式:___________ 。
②D和稀盐酸反应后的溶液与足量T反应的离子方程式:___________ 。
③H在潮湿空气中变成M的化学方程式:___________ 。
④检验W中阴离子的方法:___________ 。

(1)写出下列物质的化学式:A:
(2)按要求写出下列方程式:
①B和Q反应的离子方程式:
②D和稀盐酸反应后的溶液与足量T反应的离子方程式:
③H在潮湿空气中变成M的化学方程式:
④检验W中阴离子的方法:
您最近半年使用:0次
名校
解题方法
4 . W、X、Y、Z是原子序数依次增大的短周期主族元素,焰色试验中X呈黄色,Y是地壳中含量最多的金属元素,W、Z原子最外层电子数相同,Z的核电荷数是W的2倍。下列叙述正确的是
| A.简单离子半径大小:X>Y>Z>W |
B.化合物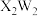 中阴阳离子的个数比为 中阴阳离子的个数比为 |
| C.X、Y、Z最高价氧化物的水化物两两间能发生反应 |
| D.简单氢化物的沸点:Z>W |
您最近半年使用:0次
2023-02-12更新
|
1070次组卷
|
7卷引用:安徽省合肥市2023届高三第一次教学质量检测 化学试题
安徽省合肥市2023届高三第一次教学质量检测 化学试题(已下线)2022年重庆高考真题化学试题变式题(选择题6-10)(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题1-16)江苏省南京市中华中学2022-2023学年高一下学期3月月考化学试题(已下线)专题06 原子结构与元素周期律(已下线)专题卷09 根据原子结构和物质结构特点叙述型元素推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)宁夏石嘴山市光明中学2024届高三第一次模拟考试理综化学试题
名校
解题方法
5 . W、X、Y、Z为原子序数增大的短周期不同主族元素,W的简单氢化物可用作制冷剂。Y单质既能溶于强酸也能溶于强碱。Z的最外层电子数是W和X的最外层电子数之和。下列叙述不正确的是
| A.简单氢化物的沸点:W>Z |
| B.Z分别与X、Y组成的二元化合物中,化学键均为离子键 |
| C.简单离子的半径大小为:Z>W>X>Y |
| D.工业上常用电解熔融盐的方法制备X |
您最近半年使用:0次
名校
解题方法
6 . X、Y、Z、W是原子序数依次增大的四种短周期元素,X氢化物的水溶液可用于刻蚀玻璃,Y是地壳中含量最高的金属元素,Z原子的核外电子数是X最外层电子数的2倍,W的单质是制作黑火药的原料之一。下列结论正确的是( )
| A.工业上通过电解法获取Y的单质 |
| B.简单氢化物的沸点:X<W |
| C.简单离子半径大小:X>Y>W |
| D.最高价氧化物水化物的酸性:Z>W |
您最近半年使用:0次
2022-04-11更新
|
765次组卷
|
5卷引用:安徽省合肥市2022届高三第二次教学质量检测理综化学试题
安徽省合肥市2022届高三第二次教学质量检测理综化学试题(已下线)押全国卷理综第10题 元素周期表 元素周期律-备战2022年高考化学临考题号押题(课标全国卷)四川省南充市2022届高三适应性考试(三诊)理综化学试题四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题2024届四川省南充市高三下学期适应性考试(二诊)理综试题-高中化学
解题方法
7 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的核外电子数是其内层电子数的3倍,X元素与Y、W元素相邻,且与W元素同主族;工业上通过电解熔融Z的氧化物来制备单质。下列说法正确的是
| A.X的单质与W的氧化物反应可制备W的单质 |
| B.Y最高价氧化物对应的水化物是离子化合物 |
| C.工业上制备Z单质时可加一种Z的化合物使Z的氧化物熔点降低 |
| D.W的最简单氢化物的稳定性强于X的最简单氢化物的稳定性 |
您最近半年使用:0次
2022-03-19更新
|
193次组卷
|
4卷引用:安徽省合肥市肥东县综合高中2021-2022学年高三下学期期中考试理科综合化学试题
名校
8 . 已知a、b、d、e、 f、g、 h为原子序数依次增大的六种短周期主族元素, 非金属元素a最外层电子数与其周期数相同,b原子的最外层电子数是其所在周期数的2倍。d的一种单质可杀菌消毒,g的最高正价与最低负价代数和为4, f的最高价氧化物可分别与e和h的最高价氧化物的水化物反应,a单质在h单质中燃烧,产物溶于水得到一种强酸甲。请用化学用语回答下列问题:
(1)f在元素周期表中的位置___ 画出与h同族的第四周期元素的原子结构示意图____________ 。
(2)d、e、f、h的简单离子的半径由大到小的顺序_________ 。
(3)下列说法正确的是 。
(4)设计一个简单的实验证明d和g的非金属性强弱: _________ (用化学方程式表示)。
(5)为降低水源中NO 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为______________ 。
(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积_______ L。最终获得溶液的物质的量浓度为_____ mol∙L−1。
(1)f在元素周期表中的位置
(2)d、e、f、h的简单离子的半径由大到小的顺序
(3)下列说法正确的是 。
| A.氢化物的稳定性d>b |
| B.含氧酸的酸性h>g>b>f |
| C.bg2中b为+4价;g为−2价可说明g的非金属性强于b |
| D.g阴离子能与Fe3+反应而h的阴离子不能,可说明g的非金属性弱于h |
(5)为降低水源中NO
 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积
您最近半年使用:0次
名校
9 . 现有部分短周期元素的性质或原子结构如下表:
请用化学用语回答下列问题:
(1)Y元素符号是___________ ,W在周期表中的位置是___________ 。
(2)元素X与元素Z相比,非金属性较强的是___________ (填元素符号),写出一个能表示X、Z非金属性强弱关系的化学反应方程式:___________ 。
(3)写出实验室制取Y的最高价氧化物对应水化物的离子方程式:___________ 。
(4)ZX2和W2按照体积比1:1充分混合后,再通入品红溶液中,观察到的实验现象是___________ ,其原因是___________ (用离子方程式表示)。
| X | X原子的L层电子数是K层电子数的3倍 |
| Y | Y存在质量数为27,中子数为14的核素 |
| Z | Z原子的L层电子数是K层和M层电子数之和 |
| W | 常温下,W的单质为黄绿色气体 |
(1)Y元素符号是
(2)元素X与元素Z相比,非金属性较强的是
(3)写出实验室制取Y的最高价氧化物对应水化物的离子方程式:
(4)ZX2和W2按照体积比1:1充分混合后,再通入品红溶液中,观察到的实验现象是
您最近半年使用:0次
2021-09-19更新
|
81次组卷
|
2卷引用:安徽省合肥艺术中学2020-2021学年高一下学期第一次调研考试化学试题
解题方法
10 . 锂电池的电解液在很大程度上制约着锂电池的发展,某种商业化锂电池的电解质的结构如图所示。已知短周期主族元素X、Y、Z、M、W的原子序数依次增大,且0.1 mol·L—1 XW的水溶液呈酸性且pH>1。下列说法正确的是
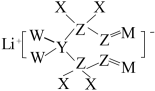

| A.简单氢化物的稳定性:W>M>Z | B.W的单质与水反应可生成两种酸 |
| C.简单离子半径:W>M | D.元素的非金属性:X>Z |
您最近半年使用:0次
2021-08-05更新
|
166次组卷
|
2卷引用:安徽省合肥市肥东县综合高中2021-2022学年高二下学期期中考试化学试题



