1 . D、E、W、R、X、Y均为元素周期表前20号主族元素。根据所学知识,回答下列问题:
(1)化合物 是一种常见的干燥剂,其阳离子和阴离子的电子层结构相同,且
是一种常见的干燥剂,其阳离子和阴离子的电子层结构相同,且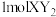 含有
含有 电子。则
电子。则 的化学式是
的化学式是_______ 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是_______ ;D与E能形成一种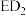 的三原子分子,且每个原子均达到了
的三原子分子,且每个原子均达到了 稳定结构,该分子的结构式为
稳定结构,该分子的结构式为_______ ,化学键类型为_______ (填“离子键”或“共价键”)。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:加热时生成_______ ,其化学键类型为_______ ,电子式为_______ 。元素R是地壳中含量最多的金属元素,写出R的单质与Z的最高价氧化物对应水化物反应的离子方程式:_______ 。
(1)化合物
 是一种常见的干燥剂,其阳离子和阴离子的电子层结构相同,且
是一种常见的干燥剂,其阳离子和阴离子的电子层结构相同,且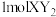 含有
含有 电子。则
电子。则 的化学式是
的化学式是(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
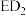 的三原子分子,且每个原子均达到了
的三原子分子,且每个原子均达到了 稳定结构,该分子的结构式为
稳定结构,该分子的结构式为(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:加热时生成
您最近半年使用:0次
2 . 甲~丁均为短周期元素,在元素周期表中的位置如图所示,甲元素原子的最外层电子数是次外层的 ,下列说法中正确的是
,下列说法中正确的是
 ,下列说法中正确的是
,下列说法中正确的是| 甲 | 乙 |
| 丙 | 丁 |
| A.简单离子半径:甲>丙 |
| B.单质丙可保存在煤油中 |
| C.最高价氧化物对应水化物的碱性:丁>乙 |
| D.甲、乙、丙、丁四种元素在自然界中主要以游离态形式存在 |
您最近半年使用:0次
3 . R、W、X、Y、Z是原子序数依次增大的前四周期元素,其中R与W位于同一周期,且R元素的第一电离能大于氧,W的单质在暗处与 能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
(1)基态Z原子的价层电子排布式为__________ ,该元素位于元素周期表中的__________ 区。
(2)基态R原子中有__________ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为__________ 形。
(3)R、W、X三种元素中第一电离能由大到小的顺序为____ (用元素符号表示),原因是________ 。
(4)R、W、X、Y、Z中非金属元素形成的最简单气态氢化物的稳定性由强到弱的顺序是__________ (填化学式)。
(5)X、Y两种元素组成的化合物 的电子式为
的电子式为__________ ,其中含有的化学键类型为__________ 。
 能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:
能剧烈化合,常温下X的单质为淡黄色固体,含Y元素的物质灼烧时焰色为紫色,基态Z原子有5个未成对电子。请回答下列问题:(1)基态Z原子的价层电子排布式为
(2)基态R原子中有
(3)R、W、X三种元素中第一电离能由大到小的顺序为
(4)R、W、X、Y、Z中非金属元素形成的最简单气态氢化物的稳定性由强到弱的顺序是
(5)X、Y两种元素组成的化合物
 的电子式为
的电子式为
您最近半年使用:0次
2023-02-15更新
|
169次组卷
|
2卷引用:河北省邢台市2022-2023学年高二上学期教学质量检测(期末)化学试题
解题方法
4 . 短周期主族元素X、Y、Z、M、Q原子序数依次增大,X、Q的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,Z在同周期主族元素中原子半径最大,M是地壳中含量最多的金属元素。
(1)Y在周期表中的位置是_______ ;Q的元素名称是_______ 。
(2)Z、M、Q的简单离子半径由小到大的顺序为_______ (用离子符号表示)。
(3)将含有M的简单离子的盐溶液与足量Z的最高价氢氧化物的溶液混合,反应的离子方程式为_______ ;
(4)可以比较Z、M两元素金属性强弱的实验是____________。
(5)R是第四周期与Q同主族的元素,下列说法正确的是____________。
(1)Y在周期表中的位置是
(2)Z、M、Q的简单离子半径由小到大的顺序为
(3)将含有M的简单离子的盐溶液与足量Z的最高价氢氧化物的溶液混合,反应的离子方程式为
(4)可以比较Z、M两元素金属性强弱的实验是____________。
| A.比较这两种元素最高价氧化物的水化物的碱性 |
| B.将Z的单质投入到M的硫酸盐溶液中 |
| C.将这两种元素单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
| A.R的最高化合价为+7 |
| B.简单气态氢化物稳定性:R>Q |
| C.简单离子的还原性:R<Q |
| D.R的单质在常温下可与氢气化合 |
您最近半年使用:0次
2023-02-14更新
|
403次组卷
|
3卷引用:山东省聊城市2022-2023学年高一上学期期末考试化学试题
山东省聊城市2022-2023学年高一上学期期末考试化学试题山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题(已下线)专题08 元素周期表与元素周期律-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
2023·安徽合肥·一模
名校
解题方法
5 . W、X、Y、Z是原子序数依次增大的短周期主族元素,焰色试验中X呈黄色,Y是地壳中含量最多的金属元素,W、Z原子最外层电子数相同,Z的核电荷数是W的2倍。下列叙述正确的是
| A.简单离子半径大小:X>Y>Z>W |
B.化合物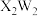 中阴阳离子的个数比为 中阴阳离子的个数比为 |
| C.X、Y、Z最高价氧化物的水化物两两间能发生反应 |
| D.简单氢化物的沸点:Z>W |
您最近半年使用:0次
2023-02-12更新
|
1070次组卷
|
7卷引用:2022年重庆高考真题化学试题变式题(选择题6-10)
(已下线)2022年重庆高考真题化学试题变式题(选择题6-10)安徽省合肥市2023届高三第一次教学质量检测 化学试题(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题1-16)江苏省南京市中华中学2022-2023学年高一下学期3月月考化学试题(已下线)专题06 原子结构与元素周期律(已下线)专题卷09 根据原子结构和物质结构特点叙述型元素推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)宁夏石嘴山市光明中学2024届高三第一次模拟考试理综化学试题
名校
解题方法
6 . A、B、C、D、E均为18电子分子,且均为前三周期主族元素的氢化物。A有臭鸡蛋气味;B和C均为四原子分子,B的水溶液常用于医用消毒;D为火箭推进器常用燃料,C和D中除氢外的另一种元素位于同一主族;E为烃。下列判断错误的是
| A.A分子中的化学键为σ键,有轴对称性,可以旋转 |
| B.B和E中均含有极性键和非极性键,两者均为非极性分子 |
| C.已知D可以和氢离子通过配位键形成阳离子,则反应前后中心原子杂化方式不变 |
| D.C分子中原子序数较大的元素可形成正四面体结构的单质分子,键角为109°28′ |
您最近半年使用:0次
7 . 甲~戊均为短周期主族元素,在周期表中的位置如图所示,基态丙原子与基态戊原子的p轨道电子数之和为9,下列说法错误的是
| 甲 | |||
| 乙 | 丙 | ||
| 丁 | 戊 |
A.基态乙原子的核外电子排布式为 |
| B.仅由甲和丙形成的化合物均具有还原性 |
| C.第一电离能:戊>丁 |
| D.戊的最高价氧化物对应的水化物能与氨水反应 |
您最近半年使用:0次
2023-02-08更新
|
57次组卷
|
2卷引用:广东省2023届高三8月大联考化学试题(二)
8 . 下表显示了元素周期装中短周期主族元素的一部分,①~⑦代表7种短周期元素。
已知:④与⑦组成的化合物是生活中最常见的调味品。请填写下列空白。
(1)与④同族的下一周期元素的原子结构示意图为:______________ 。
(2)①②③的原子半径由大到小的排列顺序:______________ (用元素符号表示)。
(3)④在氧气中燃烧的产物含有的化学键是:____________________ 。
(4)⑤的氧化物与KOH溶液反应的离子方程式是:____________________ 。
(5)③、⑥的简单气态氢化物,更稳定的是:____________________ 。(填化学式)
(6)简述溶液中含⑦简单离子的检验方法:____________________ 。
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
(1)与④同族的下一周期元素的原子结构示意图为:
(2)①②③的原子半径由大到小的排列顺序:
(3)④在氧气中燃烧的产物含有的化学键是:
(4)⑤的氧化物与KOH溶液反应的离子方程式是:
(5)③、⑥的简单气态氢化物,更稳定的是:
(6)简述溶液中含⑦简单离子的检验方法:
您最近半年使用:0次
名校
9 . 根据①~⑩元素的编号所在周期表中的位置,用相应的元素符号回答有关问题:
(1)其单质与氧气反应生成淡黄色固体化合物,该化合物的化学式是_______ ,该化合物与二氧化碳反应的化学方程式是_______ 。
(2)通常显+1价的非金属元素是_______ (填化学式,下同)。
(3)最难形成简单离子的元素是_______ 。
(4)其中一种金属单质能和冷水剧烈反应的反应方程式:_______ 。
(5)其中气态氢化物稳定性最强的是_______ (填氢化物化学式)。
(6)气态氢化物可与其最高价含氧酸反应,该元素是_______ (填化学式)。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 3 | ⑧ | ⑨ | ⑩ |
(2)通常显+1价的非金属元素是
(3)最难形成简单离子的元素是
(4)其中一种金属单质能和冷水剧烈反应的反应方程式:
(5)其中气态氢化物稳定性最强的是
(6)气态氢化物可与其最高价含氧酸反应,该元素是
您最近半年使用:0次
名校
解题方法
10 . 现有部分短周期元素的性质或原子结构如下表:
(1)元素X的一种核素可用于测定文物年代,这种核素的符号是___________ 。
(2)元素Y与氢元素形成一种离子YH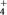 ,写出某溶液中含该微粒的检验方法:
,写出某溶液中含该微粒的检验方法:___________ 。
(3)元素Z与元素T相比,原子得电子能力较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ (填序号)。
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
④Z单质、T单质与铁反应,产物中铁元素价态
⑤Z氢化物的还原性比T的氢化物强
⑥Z单质能置换出T单质
(4)T、Z、M对应的离子半径有小到大的顺序是___________ (用化学式填写)
(5)探寻物质的性质差异性是学习的重要方法之一,T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是___________ (填化学式),理由是___________ 。
| 元素编号 | 元素的性质或原子结构 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 元素的最高正化合价是+7价 |
| M | 短周期主族原子半径最大 |
(2)元素Y与氢元素形成一种离子YH
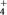 ,写出某溶液中含该微粒的检验方法:
,写出某溶液中含该微粒的检验方法:(3)元素Z与元素T相比,原子得电子能力较强的是
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
④Z单质、T单质与铁反应,产物中铁元素价态
⑤Z氢化物的还原性比T的氢化物强
⑥Z单质能置换出T单质
(4)T、Z、M对应的离子半径有小到大的顺序是
(5)探寻物质的性质差异性是学习的重要方法之一,T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是
您最近半年使用:0次



