解题方法
1 . 锰、铬、铜、铁四种元素的基态原子中,有五个未成对电子的原子核外电子排布式为___________ 。
您最近一年使用:0次
名校
解题方法
2 . 下图为“点击化学”的一种反应
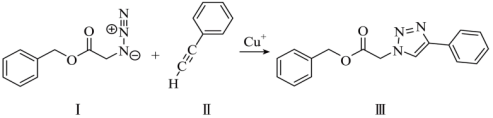
(1)基态 的价层电子排布式为
的价层电子排布式为___________ 。
(2)写出I中C、N、O的原子半径大小(按从小到大排列)___________ ;
(3)画出基态N原子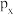 轨道的电子云轮廓图
轨道的电子云轮廓图___________ ;
(4)从绿色化学角度分析,该反应的优点在于(写出一点即可)___________ 。

(1)基态
 的价层电子排布式为
的价层电子排布式为(2)写出I中C、N、O的原子半径大小(按从小到大排列)
(3)画出基态N原子
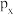 轨道的电子云轮廓图
轨道的电子云轮廓图(4)从绿色化学角度分析,该反应的优点在于(写出一点即可)
您最近一年使用:0次
2023高三·全国·专题练习
3 . 谷氨酸[HOOC—CH(NH2)—CH2—CH2—COOH]的钠盐——谷氨酸钠(C5H8NO4Na)是味精的主要成分,谷氨酸分子中C原子的杂化方式为___________ ,C原子与O原子所形成的化学键中σ键与π键的数目比N(σ)∶N(π)=___________ ,π键的特征是两块电子云呈___________ 对称。
您最近一年使用:0次
名校
4 . 铋(83Bi)为第V A族元素,常见化合价为+3和+5。化合物NaBiO3为黄色固体,常温下微溶于水,在空气中逐渐分解产生Bi2O3、NaOH等物质。
(1)铋元素最外层电子分布在_____ 种能级中,共有_____ 种运动状态。
(2)铋酸钠NaBiO3中属于短周期元素的离子半径大小关系为_________ 。
(3)元素Na、Bi、O的金属性依次减弱,非金属性依次增强,请列举判断依据:_______ 。
(4)铋酸钠NaBiO3在空气中分解所得到产物中,化学键类型是______ 。
A.金属键 B.离子键 C.极性键 D.非极性键
(5)将NaBiO3加入MnSO4和H2SO4的混合溶液里加热,发生如下反应:
[ ]NaBiO3+[ ]MnSO4+[ ]H2SO4→[ ]Na2SO4+[ ]Bi2(SO4)3+[ ]NaMnO4+[ ]H2O
①配平该化学方程式,将系数填写在对应位置上。
______ NaBiO3+______ MnSO4+______ H2SO4→______ Na2SO4+______ Bi2(SO4)3+______ NaMnO4+______ H2O
②若有2mol氧化剂在该反应中被还原,则生成的MnO 被还原为Mn2+时,能将
被还原为Mn2+时,能将____ mol HCl氧化成Cl2。
(6)写出NaBiO3固体溶于HCl时发生反应的离子方程式:_________ 。
(1)铋元素最外层电子分布在
(2)铋酸钠NaBiO3中属于短周期元素的离子半径大小关系为
(3)元素Na、Bi、O的金属性依次减弱,非金属性依次增强,请列举判断依据:
(4)铋酸钠NaBiO3在空气中分解所得到产物中,化学键类型是
A.金属键 B.离子键 C.极性键 D.非极性键
(5)将NaBiO3加入MnSO4和H2SO4的混合溶液里加热,发生如下反应:
[ ]NaBiO3+[ ]MnSO4+[ ]H2SO4→[ ]Na2SO4+[ ]Bi2(SO4)3+[ ]NaMnO4+[ ]H2O
①配平该化学方程式,将系数填写在对应位置上。
②若有2mol氧化剂在该反应中被还原,则生成的MnO
 被还原为Mn2+时,能将
被还原为Mn2+时,能将(6)写出NaBiO3固体溶于HCl时发生反应的离子方程式:
您最近一年使用:0次
11-12高三上·上海奉贤·期末
解题方法
5 . 工业制玻璃主要原料有石英、纯碱和石灰石.在玻璃窑中发生主要反应的化学方程式为:Na2CO3+SiO2 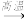 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2  CaSiO3+CO2↑
CaSiO3+CO2↑
(1)普通玻璃的成分是Na2CaSi6O14,它的氧化物形式为________ ,则原料中SiO2、Na2CO3、CaCO3的物质的量之比为_________________________ 。
(2)在上述反应的反应物和生成物中,属于非极性分子的电子式___________________ ,有_____________ 种不同类型的晶体(填数字)
(3)在上述普通玻璃的组成元素中某元素与铝元素同周期且原子半径比铝原子半径大,该元素离子半径比铝离子半径___________ (填“大”或“小”),该元素与铝元素两者的最高价氧化物的水化物之间发生反应的离子方程式为__________________________ 。
(4)在上述普通玻璃的组成元素中,与铝元素同周期的另一元素的原子最外层共有________ 种不同运动状态的电子、________ 种不同能级的电子。
 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2  CaSiO3+CO2↑
CaSiO3+CO2↑(1)普通玻璃的成分是Na2CaSi6O14,它的氧化物形式为
(2)在上述反应的反应物和生成物中,属于非极性分子的电子式
(3)在上述普通玻璃的组成元素中某元素与铝元素同周期且原子半径比铝原子半径大,该元素离子半径比铝离子半径
(4)在上述普通玻璃的组成元素中,与铝元素同周期的另一元素的原子最外层共有
您最近一年使用:0次
6 . 铅是一种金属元素,可用作耐酸腐蚀、蓄电池等的材料。其合金可作铅字、轴承、电缆包皮之用,还可做体育运动器材铅球等。
(1)铅元素位于元素周期表第六周期IVA。IVA中原子序数最小的元素的原子有_______ 种能量不同的电子,其次外层的电子云有_______ 种不同的伸展方向。
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是______ (填化学式),气态氢化物沸点最低的是_____________ (填化学式)。
(3)配平下列化学反应方程式,把系数以及相关物质(写化学式)填写在空格上, 并标出电子转移的方向和数目。
__ PbO2+___ MnSO4+___ HNO3 →___ HMnO4+___ Pb(NO3)2+___ PbSO4↓+____ ____
(4)把反应后的溶液稀释到1 L,测出其中的Pb2+的浓度为0.6 mol·L-1,则反应中转移的电子数为_______ 个。
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是_______
A. PbO2+4HCl→PbCl4+2H2O B. PbO2+4HCl→PbCl2+ Cl2↑+2H2O
C. PbO2+2HCl+2H+→PbCl2+2H2O D. PbO2+4HCl→PbCl2+2OH-
(1)铅元素位于元素周期表第六周期IVA。IVA中原子序数最小的元素的原子有
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是
(3)配平下列化学反应方程式,把系数以及相关物质(写化学式)填写在空格上, 并标出电子转移的方向和数目。
(4)把反应后的溶液稀释到1 L,测出其中的Pb2+的浓度为0.6 mol·L-1,则反应中转移的电子数为
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是
A. PbO2+4HCl→PbCl4+2H2O B. PbO2+4HCl→PbCl2+ Cl2↑+2H2O
C. PbO2+2HCl+2H+→PbCl2+2H2O D. PbO2+4HCl→PbCl2+2OH-
您最近一年使用:0次
名校
解题方法
7 . 大型客机燃油用四乙基铅[Pb(CH2CH3)4])做抗震添加剂,但皮肤长期接触四乙基铅对身体健康有害,可用硫基乙胺(HSCH2CH2NH2)和KMnO4清除四乙基铅。
(1)碳原子核外电子的空间运动状态有______ 种,基态锰原子的外围电子排布式为___ ,该原子能量最高的电子的电子云轮廓图形状为________ 。
(2)N、C和Mn电负性由大到小的顺序为____________ 。
(3)HSCH2CH2NH2中C的杂化方式为_____ ,其中NH2-空间构型为____ ;N和P的价电子相同,但磷酸的组成为H3PO4,而硝酸的组成不是H3NO4,其原因是_______ 。
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于_____ 晶体。已知Pb(CH2CH3)4晶体的堆积方式如下。
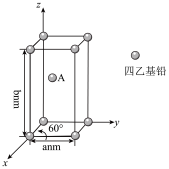
Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是___ ,A分子的坐标参数为_____ ;设阿伏加 德罗常数为NA/mol,Pb(CH2CH3)4]的摩尔质量为Mg/mol,则Pb(CH2CH3)4]晶体的密度是_____ g/cm3 (列出计算式即可)。
(1)碳原子核外电子的空间运动状态有
(2)N、C和Mn电负性由大到小的顺序为
(3)HSCH2CH2NH2中C的杂化方式为
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于

Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是
您最近一年使用:0次
2020-02-24更新
|
654次组卷
|
3卷引用:四川省遂宁市第二中学2020届高三上学期第二次高考模拟理综化学试题
四川省遂宁市第二中学2020届高三上学期第二次高考模拟理综化学试题(已下线)专题6.4 物质结构与性质(选考)(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升北京专家2020届高三高考模拟试卷(二)化学试题
8 . 氯原子核外有___ 种不同运动状态的电子,它的最外层电子排布式是___ 。
您最近一年使用:0次
12-13高三上·上海闵行·期末
解题方法
9 . 黑火药是中国古代四大发明之一,它的爆炸反应为:
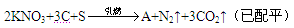
(1)生成物中除了氮气与二氧化碳外,还有一种物质A生成,则A的电子式为____________ ,A属于________ 晶体。
(2)黑火药中位于元素周期表短周期的元素有_________ 种。其中一种元素的单质可用于制药,其氧化物可用于漂白织物和防腐剂,该元素在周期表中的位置是___________________ ,该元素的原子核外有______ 种不同运动状态的电子。
(3)黑火药中所含元素的原子半径从大到小的顺序是________________ (用元素符号表示);
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有___________ 。
A.同条件同浓度溶液pH:Na2CO3>Na2SO4
B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
D.分解温度:CH4>H2S
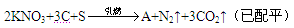
(1)生成物中除了氮气与二氧化碳外,还有一种物质A生成,则A的电子式为
(2)黑火药中位于元素周期表短周期的元素有
(3)黑火药中所含元素的原子半径从大到小的顺序是
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有
A.同条件同浓度溶液pH:Na2CO3>Na2SO4
B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
D.分解温度:CH4>H2S
您最近一年使用:0次



