名校
解题方法
1 . 2023年6月,科学家首次合成含铍-铍能的固态化合物,相关成果发表于《科学》杂质。该分子入选2023年最“炫”分子榜单,其结构如图所示,回答下列问题: 原子最外层电子的电子云轮廓图为
原子最外层电子的电子云轮廓图为_____ (填序号)。
A.球形 B.哑铃形
(2)下列电子排布式分别代表铍微粒,其中失去1个电子所需能量最多的是_____。
(3)“固态双铍化合物的化学式为_____ ,它不含_____ (填标号)。
A.极性键 B.非极性键 C.金属键 D. 键
键
(4)卤化铍的熔点如表所示:
① 中
中 原子的杂化方式为
原子的杂化方式为_____ ;
②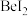
_____ (填“能”或“不能)溶于四氯化碳:
③ 、
、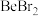 、
、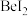 的熔点依次升高的原因是
的熔点依次升高的原因是_____ 。
(5) 易形成配离子
易形成配离子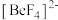 ,其中心阳离子的配位数为
,其中心阳离子的配位数为_____ ,配体是_____ (填化学符号),配离子的空间构型为_____ 。
(6)离子晶体中稳定配位多面体的理论半径比如表所示:
已知铍离子、氧离子的半径分别为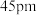 、
、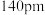 ,
, 的配位多面体是
的配位多面体是_____ 。
(7)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。这种氧化物的化学式为_____ ;设晶胞参数为 ,用
,用 表示阿伏加德罗参数的值,则
表示阿伏加德罗参数的值,则 晶体的密度为
晶体的密度为_____  (用含a和
(用含a和 的式子表示)。
的式子表示)。
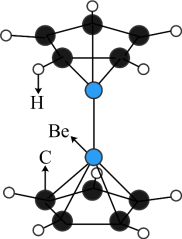
 原子最外层电子的电子云轮廓图为
原子最外层电子的电子云轮廓图为A.球形 B.哑铃形
(2)下列电子排布式分别代表铍微粒,其中失去1个电子所需能量最多的是_____。
A.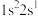 | B. | C.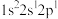 | D. |
(3)“固态双铍化合物的化学式为
A.极性键 B.非极性键 C.金属键 D.
 键
键(4)卤化铍的熔点如表所示:
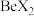 | 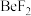 |  | 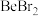 | 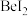 |
熔点/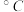 | 552 | 399 | 488 | 510 |
 中
中 原子的杂化方式为
原子的杂化方式为②
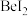
③
 、
、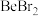 、
、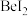 的熔点依次升高的原因是
的熔点依次升高的原因是(5)
 易形成配离子
易形成配离子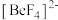 ,其中心阳离子的配位数为
,其中心阳离子的配位数为(6)离子晶体中稳定配位多面体的理论半径比如表所示:
| 配位多面体 | 配位数 | 半径比(r+/r-) |
| 平面三角形 | 3 | 0.15~0.225 |
| 四面体 | 4 | 0.225~0.414 |
| 八面体 | 6 | 0.414~0.732 |
| 立方体 | 8 | 0.732~1.000 |
| 立方八面体 | 12 | 1.000 |
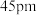 、
、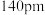 ,
, 的配位多面体是
的配位多面体是(7)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。这种氧化物的化学式为
 ,用
,用 表示阿伏加德罗参数的值,则
表示阿伏加德罗参数的值,则 晶体的密度为
晶体的密度为 (用含a和
(用含a和 的式子表示)。
的式子表示)。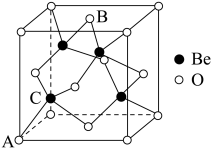
您最近一年使用:0次
2 . 按要求回答下列问题。
(1)基态硅原子核外电子的运动状态有___________ 种,价层电子轨道表示式为___________ 。
(2)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
(3)①钴位于元素周期表中___________ (填“s”、“p”、“d”或“ds”)区,与钴位于同一周期且含有相同未成对电子数的元素有___________ 种。
②钴元素可形成配合物[Co(NH3)6]Cl3,1mol该配合物含有σ键的数目为___________ 。该配合物中存在的化学键有___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D.氢键 E.配位键
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
比较两元素的 、
、 可知,气态Mn2+再失去1个电子比气态
可知,气态Mn2+再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是___________ 。
(5)第四周期主族元素中,第一电离能介于Ga、As之间的元素有___________ 种。
(6)氯化铝熔点为194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成为Al2Cl6,其结构式为___________ (已知Al2Cl6中原子均满足8e-稳定结构)。
(1)基态硅原子核外电子的运动状态有
(2)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
| A.1s22s22p43s1 | B.1s22s22p43d2 | C.1s22s22p5 | D.1s22s22p6 |
②钴元素可形成配合物[Co(NH3)6]Cl3,1mol该配合物含有σ键的数目为
A.离子键 B.极性键 C.非极性键 D.氢键 E.配位键
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
电离能/ | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
 、
、 可知,气态Mn2+再失去1个电子比气态
可知,气态Mn2+再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是(5)第四周期主族元素中,第一电离能介于Ga、As之间的元素有
(6)氯化铝熔点为194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成为Al2Cl6,其结构式为
您最近一年使用:0次
名校
3 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。①~⑥表示元素在周期表中的位置,回答下列问题。
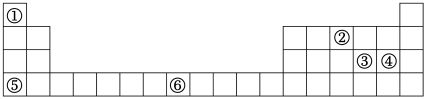
(1)①和④形成的化合物的化学式为_______ 。
(2)②的基态原子的轨道表示式为_______ ,其电子占据的最高能级的电子云轮廓是_______ 。
(3)⑤的基态原子占据的最高能层的符号是_______ ,其基态正一价离子占据的最高能级共有_______ 个原子轨道。
(4)⑥的基态正三价离子的价层电子排布式为_______ 。
(5)下列说法不正确 的是_______ 。
a.②的2px、2py、2pZ轨道互相垂直,但能量相等
b.④的p能级能量一定比s能级的能量高
c.⑥的2s、3s、4s能级的轨道数依次增多
(6)③和⑤形成的化合物的水溶液pH>7,结合离子方程式解释原因_______ 。

(1)①和④形成的化合物的化学式为
(2)②的基态原子的轨道表示式为
(3)⑤的基态原子占据的最高能层的符号是
(4)⑥的基态正三价离子的价层电子排布式为
(5)下列说法
a.②的2px、2py、2pZ轨道互相垂直,但能量相等
b.④的p能级能量一定比s能级的能量高
c.⑥的2s、3s、4s能级的轨道数依次增多
(6)③和⑤形成的化合物的水溶液pH>7,结合离子方程式解释原因
您最近一年使用:0次
解题方法
4 . JohnB.Goodenough等三位科学家因在发展锂离子电池方面做出的贡献而获得了诺贝尔化学奖。回答下列问题:
(1)锰酸锂(LiMn2O4)电池具有原料成本低合成工艺简单等优点。原子中运动的电子有两种相反的身旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为___________ 。基态Mn原子核外价层电子的运动状态有___________ 种。
(2)锂离子电池的电解液一般为溶有LiPF6的碳酸酯类有机溶剂,LiPF6遇水反应生成PF3和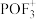 ,
,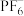 中心原子的价层电子对数为
中心原子的价层电子对数为___________ ,POF3的空间构型为___________ 。
(3)已知第三电离能数据:I3(Mn)=3246kJ·mol-1,I3(Fe)=2957kJ·mol-1.锰的第三电离能大于铁的第三电离能,其主要原因是___________ 。
(4)铋化锂被认为是很有潜力的正极材料,晶胞结构如图所示。
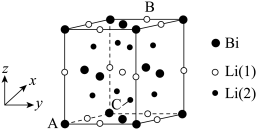
①晶胞可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体的化学式为___________ 。
②图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为___________ ,Bi与Li(1)和Li(2)之间的最短距离的比为___________ 。
(1)锰酸锂(LiMn2O4)电池具有原料成本低合成工艺简单等优点。原子中运动的电子有两种相反的身旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为(2)锂离子电池的电解液一般为溶有LiPF6的碳酸酯类有机溶剂,LiPF6遇水反应生成PF3和
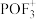 ,
,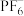 中心原子的价层电子对数为
中心原子的价层电子对数为(3)已知第三电离能数据:I3(Mn)=3246kJ·mol-1,I3(Fe)=2957kJ·mol-1.锰的第三电离能大于铁的第三电离能,其主要原因是
(4)铋化锂被认为是很有潜力的正极材料,晶胞结构如图所示。

①晶胞可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体的化学式为
②图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为
您最近一年使用:0次
解题方法
5 . 主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,从该矿渣中回收六水合硫酸镍晶体的工艺流程如图:

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。
(1)28Ni位于元素周期表_____ 区(填“s”“p”“d”或“ds”),其基态原子核外电子的空间运动状态有_____ 种。
(2)“焙烧”中,SiO2几乎不发生反应,NiO、CaO、FeO转化为相应的硫酸盐。NiFe2O4生成NiSO4、Fe2(SO4)3,发生该反应的化学方程式为______ 。
(3)“浸渣”的成分除Fe2O3、FeO(OH)外还含有______ (填化学式),为检验浸出液中是否含有Fe3+,可选用的化学试剂是______ 。
(4)“浸出液”中c(Ca2+)=1.0×10-3mol•L-1,加NaF固体时,忽略溶液体积变化,当除钙率达到99%时,除钙后的溶液中c(F-)=______ 。[已知Ksp(CaF2)=4.0×10-11]
(5)“萃取”时发生反应Mn+(水相)+nRH(有机相) MRn(有机相)+nH+(水相)(Mn+为金属离子,RH为萃取剂),萃取率与
MRn(有机相)+nH+(水相)(Mn+为金属离子,RH为萃取剂),萃取率与 的关系如图所示,V0/VA的最佳取值为
的关系如图所示,V0/VA的最佳取值为______ ;“反萃取”能使有机相再生而循环使用,可在有机相中加入______ ,待充分反应后再分液。

(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
从NiSO4溶液获得稳定的NiSO4•H2O晶体的操作是:______ 、______ 、过滤、洗涤、干燥等多步操作。

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。
(1)28Ni位于元素周期表
(2)“焙烧”中,SiO2几乎不发生反应,NiO、CaO、FeO转化为相应的硫酸盐。NiFe2O4生成NiSO4、Fe2(SO4)3,发生该反应的化学方程式为
(3)“浸渣”的成分除Fe2O3、FeO(OH)外还含有
(4)“浸出液”中c(Ca2+)=1.0×10-3mol•L-1,加NaF固体时,忽略溶液体积变化,当除钙率达到99%时,除钙后的溶液中c(F-)=
(5)“萃取”时发生反应Mn+(水相)+nRH(有机相)
 MRn(有机相)+nH+(水相)(Mn+为金属离子,RH为萃取剂),萃取率与
MRn(有机相)+nH+(水相)(Mn+为金属离子,RH为萃取剂),萃取率与 的关系如图所示,V0/VA的最佳取值为
的关系如图所示,V0/VA的最佳取值为
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
| 温度 | 低于30.8℃ | 30.8~53.8℃ | 53.8~280℃ | 高于280℃ |
| 晶体形态 | NiSO4•7H2O | NiSO4•H2O | 多种结晶水合物 | NiSO4 |
您最近一年使用:0次
解题方法
6 . 碱金属(Li、Na、K、Rb、Cs)及其化合物在生产、生活中有着重要的应用。
请回答:
(1)基态K原子核外有___________ 种不同的电子运动状态。
(2)卤化物CsICl2受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。解释X的熔点比Y高的原因:___________
(3)已知RbH2PO2是次磷酸的正盐,H3PO2的结构式为___________ ,其中P原子采取___________ 杂化方式。
(4)Al、B、H电负性分别为1.5、2.0、2.1,简要说明LiAlH4还原性比NaBH4强的原因:___________
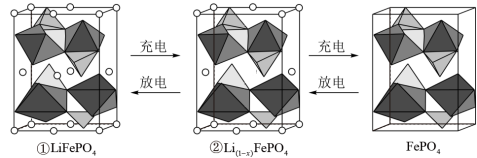
(5)锂离子电池电极材料是LiFePO4,其晶胞结构示意图如①所示。其中O围绕Fe和P分别形成4个正八面体和4个正四面体。电池充电时,LiFePO4脱出部分Li+形成Li(1-x)FePO4,其结构示意图如②所示,则Li(1-x)FePO4晶胞中n(Fe2+):n(Fe3+)=_________ 。
请回答:
(1)基态K原子核外有
(2)卤化物CsICl2受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。解释X的熔点比Y高的原因:
(3)已知RbH2PO2是次磷酸的正盐,H3PO2的结构式为
(4)Al、B、H电负性分别为1.5、2.0、2.1,简要说明LiAlH4还原性比NaBH4强的原因:
(5)锂离子电池电极材料是LiFePO4,其晶胞结构示意图如①所示。其中O围绕Fe和P分别形成4个正八面体和4个正四面体。电池充电时,LiFePO4脱出部分Li+形成Li(1-x)FePO4,其结构示意图如②所示,则Li(1-x)FePO4晶胞中n(Fe2+):n(Fe3+)=

您最近一年使用:0次
2023-03-12更新
|
408次组卷
|
2卷引用:浙江省浙里卷天下2022-2023学年高三百校联考3月测试化学试题
解题方法
7 . 元素H、N、O、S、Ni、Fe之间可形成多种化合物。请回答下列问题:
(1)基态Fe2+原子的价电子排布式为____________ ;Fe原子最外层电子的电子云形状为__________ 。
(2)N、O、S三种元素的第一电离能由大到小的顺序为___________ ;下列状态的O中,最容易失去最外层电子的是___________ (填字母)。
A.1s22s22p3 B.1s22s22p4 C.1s22s22p33s1 D.1s22s22p23s1
(3)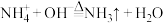 ,
, 转化为NH3的过程中,没有发生变化的有
转化为NH3的过程中,没有发生变化的有________ (填字母)。
A.键角 B.粒子的空间构型 C.杂化轨道类型
(4)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①若晶胞a中Fe原子直径为d pm,设该晶胞边长x,则x=_________ cm。(用含d的代数式表示)。
②晶胞b中与一个Fe原子最邻近的Fe原子共有_________ 个。
③若晶胞c的密度为ρ g/cm3,则铁的原子半径r=_________ cm。(NA表示阿伏加德罗常数的值,用含ρ、NA的式子表示)。
(1)基态Fe2+原子的价电子排布式为
(2)N、O、S三种元素的第一电离能由大到小的顺序为
A.1s22s22p3 B.1s22s22p4 C.1s22s22p33s1 D.1s22s22p23s1
(3)
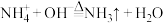 ,
, 转化为NH3的过程中,没有发生变化的有
转化为NH3的过程中,没有发生变化的有A.键角 B.粒子的空间构型 C.杂化轨道类型
(4)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①若晶胞a中Fe原子直径为d pm,设该晶胞边长x,则x=
②晶胞b中与一个Fe原子最邻近的Fe原子共有
③若晶胞c的密度为ρ g/cm3,则铁的原子半径r=
您最近一年使用:0次
解题方法
8 . John B.Goodenough等三位科学家因在发展锂离子电池方面做出的贡献而获得了诺贝尔化学奖。回答下列问题:
(1)锰酸锂( LiMn2O4)电池具有原料成本低合成工艺简单等优点。原子中运动的电子有两种相反的身旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为_______ 。基态 Mn原子核外价层电子的运动状态有_______ 种。
(2)锂离子电池的电解液一般为溶有LiPF6的碳酸酯类有机溶剂,LiPF6遇水反应生成PF3和POF , PF
, PF 中心原子的价层电子对数为
中心原子的价层电子对数为_______ ,POF3的空间构型为_______ 。 下列对PF5中心原子杂化方式的推断合理的是_______ (填字母)。
A. sp2 B. sp3 C. sp3d D. sp3d2
(3)三元正极材料LiC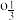 N
N jMnO2掺杂Al3+可使其性能更优,第三电离能:Fe
jMnO2掺杂Al3+可使其性能更优,第三电离能:Fe_______ (填“大于”或“小于”)Mn,原因是_______ 。
(4)链化锂被认为是很有潜力的正极材料,晶胞结构如图所示。
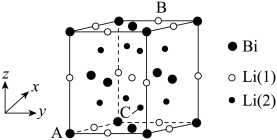
①晶施可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体的化学式为_______ 。
②图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为_______ ,Bi与Li(1)和Li(2)之间的最短距离的比值为_______ 。
(1)锰酸锂( LiMn2O4)电池具有原料成本低合成工艺简单等优点。原子中运动的电子有两种相反的身旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为(2)锂离子电池的电解液一般为溶有LiPF6的碳酸酯类有机溶剂,LiPF6遇水反应生成PF3和POF
 , PF
, PF 中心原子的价层电子对数为
中心原子的价层电子对数为A. sp2 B. sp3 C. sp3d D. sp3d2
(3)三元正极材料LiC
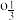 N
N jMnO2掺杂Al3+可使其性能更优,第三电离能:Fe
jMnO2掺杂Al3+可使其性能更优,第三电离能:Fe(4)链化锂被认为是很有潜力的正极材料,晶胞结构如图所示。

①晶施可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体的化学式为
②图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为
您最近一年使用:0次
名校
解题方法
9 . 锗、锡、铅均属于ⅣA族元素,它们的单质与化合物广泛应用于生活的各个领域。
Ⅰ.完成下列填空:
(1)锗元素原子核外能量最高的电子有_______ 个,它们运动所形成的电子云形状为_______ 形。
(2)氢化锗(GeH4)结构与甲烷类似,在常温常压下是具有刺激性气味的无色有毒气体。从结构角度比较GeH4与CH4沸点高低并说明理由_______ 。氢化锗的液氨溶液具有较好的导电性,主要是因为GeH4与NH3反应生成了 和
和_______ (填化学式)两种离子。
Ⅱ.三水锡酸钠(Na2SnO3·3H2O)是一种易溶于水的无色晶体,露置在空气中会逐渐转化成Na2CO3和Sn(OH)4。
(3)常温下,相同物质的量浓度的Na2SnO3溶液与Na2CO3溶液,前者pH_______ (填“大于”“小于”或“等于”)后者。
(4)写出三水锡酸钠露置在空气中发生反应的化学方程式_______ 。
Ⅲ.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、 、
、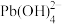 。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。

(5)Pb(NO3)2溶液中,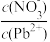
_______ 2(填“>”“=”或“<”);往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液中存在的阳离子除Na+外,还有_______ (填微粒符号)。
(6)科学家发现一种新型脱铅剂DH,能有效除去水中的痕量铅。已知DH脱铅过程中主要发生反应为:2DH(s)+Pb2+(aq) D2Pb(s)+2H+。则脱铅时最合适的pH约为
D2Pb(s)+2H+。则脱铅时最合适的pH约为_______ (选填编号)。
a.4~5 b.6~7 c.8~10 d.12~14
Ⅰ.完成下列填空:
(1)锗元素原子核外能量最高的电子有
(2)氢化锗(GeH4)结构与甲烷类似,在常温常压下是具有刺激性气味的无色有毒气体。从结构角度比较GeH4与CH4沸点高低并说明理由
 和
和Ⅱ.三水锡酸钠(Na2SnO3·3H2O)是一种易溶于水的无色晶体,露置在空气中会逐渐转化成Na2CO3和Sn(OH)4。
(3)常温下,相同物质的量浓度的Na2SnO3溶液与Na2CO3溶液,前者pH
(4)写出三水锡酸钠露置在空气中发生反应的化学方程式
Ⅲ.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、
 、
、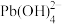 。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
(5)Pb(NO3)2溶液中,
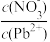
(6)科学家发现一种新型脱铅剂DH,能有效除去水中的痕量铅。已知DH脱铅过程中主要发生反应为:2DH(s)+Pb2+(aq)
 D2Pb(s)+2H+。则脱铅时最合适的pH约为
D2Pb(s)+2H+。则脱铅时最合适的pH约为a.4~5 b.6~7 c.8~10 d.12~14
您最近一年使用:0次
2022-05-29更新
|
272次组卷
|
4卷引用:上海市虹口区2022届高三下学期第二次模拟考试化学试题
上海市虹口区2022届高三下学期第二次模拟考试化学试题(已下线)2022年北京高考真题变式题1-14(已下线)2022年北京高考真题化学试题变式题(结构与性质)江西省吉安市永丰县永丰中学2022-2023学年高二上学期1月期末化学(B班)试题
名校
解题方法
10 . KZnF3是一种良好的光学材料,可由K2CO3、ZnF2、NH4HF2制备,掺杂Co、Ni等过渡金属可得到不同的荧光材料,回答下列问题:
(1)基态F原子的价电子轨道表达式为___ ;基态Zn原子核外占据最高能层电子的电子云轮廓图形状为___ 。
(2)K2CO3中阴离子的立体构型为___ ,NH4HF2中N原子的杂化方式为___ 。
(3)某镍配合物结构如图所示。
①分子内含有的化学键有___ (填序号)。
②配合物中元素原子的第一电离能N___ O(填“>”“<”或“=”),从原子结构角度解释原因是___ 。
(4)KZnF3具有钙钛矿型立方结构,其晶胞结构如图所示:___ 。
②已知晶胞边长为a pm,NA表示阿伏加德罗常数的值,则KZnF3晶体的密度为___ g·cm-3(用含a、NA的代数式表示)。
(1)基态F原子的价电子轨道表达式为
(2)K2CO3中阴离子的立体构型为
(3)某镍配合物结构如图所示。
①分子内含有的化学键有
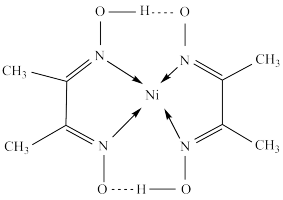
②配合物中元素原子的第一电离能N
(4)KZnF3具有钙钛矿型立方结构,其晶胞结构如图所示:
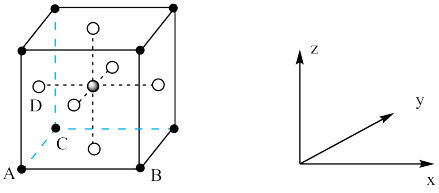
②已知晶胞边长为a pm,NA表示阿伏加德罗常数的值,则KZnF3晶体的密度为
您最近一年使用:0次
2021-09-04更新
|
761次组卷
|
5卷引用:安徽省蚌埠市2022届高三上学期第一次教学质量检查化学试题



