1 . 如图是s能级和p能级的原子轨道图。
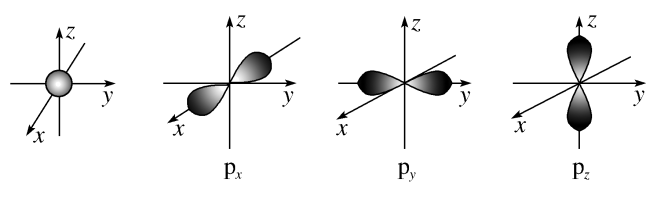
试回答下列问题:
(1)s电子的原子轨道呈________ 形,每个s能级有________ 个原子轨道;p电子的原子轨道呈________ 形,每个p能级有________ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是________ 电子,其电子云在空间有3个互相________ (填“垂直”或“平行”)的伸展方向。元素X的名称是________ ,它的最低价氢化物的电子式是________ 。
(3)元素Y的原子最外层电子排布式为nsn-1npn+1,Y的元素符号为________ ,原子的核外电子排布式为______________ 。

试回答下列问题:
(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是
(3)元素Y的原子最外层电子排布式为nsn-1npn+1,Y的元素符号为
您最近半年使用:0次
2020-07-07更新
|
613次组卷
|
3卷引用:陕西省咸阳百灵学校2019-2020学年高二下学期第二次月考化学试题
2 . 下列关于电子云的叙述中不正确的是
| A.电子云是用小黑点的疏密程度来表示电子在核外空间出现的概率密度 |
| B.电子云实际上是电子运动形成的类似云一样的图形 |
| C.1s电子云图表明离核越远,电子出现概率密度越小 |
| D.能级不同,电子云的轮廓也不一样 |
您最近半年使用:0次
2020-07-07更新
|
138次组卷
|
4卷引用:陕西省咸阳百灵学校2019-2020学年高二下学期第二次月考化学试题
陕西省咸阳百灵学校2019-2020学年高二下学期第二次月考化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第一节 原子结构(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)四川省绵阳市盐亭中学2022-2023学年高二上学期第一次月考教学质量检测化学试题
3 . 下列说法正确的是
| A.因为p轨道是哑铃形的,所以p轨道上的电子也是哑铃形的 |
| B.能层序数为3时,有3s、3p、3d、3f四个轨道 |
| C.氢原子中只有一个电子,故氢原子核外只有一个轨道 |
| D.原子轨道与电子云都是用来形象描述电子运动状态的 |
您最近半年使用:0次
4 . 电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述。下列有关电子云的说法正确的是
| A.概率密度的大小体现了电子数目的多少 |
| B.概率密度的大小体现了空间某处电子出现概率的大小 |
| C.基态C原子的1s电子的电子云和2s电子的电子云完全相同 |
| D.基态Li原子的1s电子的电子云和2s电子的电子云形状不同 |
您最近半年使用:0次
2020-07-07更新
|
311次组卷
|
4卷引用:陕西省咸阳百灵学校2019-2020学年高二下学期第二次月考化学试题
5 . 下列说法不正确 的是
| A.同一主族中,随着核电荷数的增加,元素的原子半径逐渐增大 |
| B.同一周期中,ⅡA与ⅢA族元素原子的核电荷数可能相差11 |
| C.原子核外电子排布,先排满K层再排L层、先排满L层再排M层 |
| D.同一原子中,在离核较近的区域运动的电子能量较高 |
您最近半年使用:0次
解题方法
6 . 已知反应3NaH+Fe2O3 2Fe+3NaOH。
2Fe+3NaOH。
(1)基态Fe原子核外共有__ 种运动状态不相同的电子;Fe3+的价电子排布图为__ 。
(2)1molNaOH含有σ键数目为__ ;Fe3+可以和SCN-形成配合物,该反应是典型的可逆反应,说明配位原子配位能力__ (填“强”或“弱”)。
(3)上述反应中含Na的化合物晶体类型均为__ 晶体。
 2Fe+3NaOH。
2Fe+3NaOH。(1)基态Fe原子核外共有
(2)1molNaOH含有σ键数目为
(3)上述反应中含Na的化合物晶体类型均为
您最近半年使用:0次
解题方法
7 . 根据题目要求,回答下列问题:
(1)下列现象和应用与电子跃迁无关的是___ 。
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用__ 形象化描述。
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)__ I1(Cu)(填“大于”或“小于”)。原因是__ 。
(4)ZnF2具有较高的熔点(872℃),其化学键类型是___ ;
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为___ , 原子的杂化形式为
原子的杂化形式为__ 。
(6)与H2O分子互为等电子体的阴离子为__ 。
(7)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为__ 。
(8)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) ΔH=-313kJ/mol,F—F键的键能为159kJ/mol,Cl—Cl键的键能为242kJ/mol,则ClF3中Cl—F键的平均键能为__ kJ/mol。ClF3的熔、沸点比BrF3的__ (填“高”或“低”)。
(1)下列现象和应用与电子跃迁无关的是
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)
(4)ZnF2具有较高的熔点(872℃),其化学键类型是
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
 原子的杂化形式为
原子的杂化形式为(6)与H2O分子互为等电子体的阴离子为
(7)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
(8)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) ΔH=-313kJ/mol,F—F键的键能为159kJ/mol,Cl—Cl键的键能为242kJ/mol,则ClF3中Cl—F键的平均键能为
您最近半年使用:0次
8 . m、n、x、y四种主族元素在周期表的相对位置如图所示。已知它们的原子序数总和为46,则:

(1)元素n的气态氢化物的电子式为___ ,基态n原子的核外共有__ 种不同运动状态的电子。
(2)m与y所形成的化合物含___ 键,属___ 分子。(填“极性”或“非极性”)
(3)x位于周期表的第___ 周期第___ 族;其简单离子的离子结构示意图为___ 。

(1)元素n的气态氢化物的电子式为
(2)m与y所形成的化合物含
(3)x位于周期表的第
您最近半年使用:0次
解题方法
9 . 下列说法中正确的是( )
| A.1s电子云呈球形,表示电子绕原子核做圆周运动 | B.基态氢原子的电子云是圆形的 |
C.ns能级的原子轨道图可表示为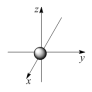 | D.3d3表示3d能级有3个原子轨道 |
您最近半年使用:0次
名校
解题方法
10 . 下列说法或化学用语表达正确的是

| A.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动 |
| B.p能级的原子轨道呈哑铃形,随着能层的增加,p能级原子轨道也在增多 |
C.某原子的电子排布式为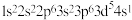 属于激发态 属于激发态 |
D. 的电子排布式为 的电子排布式为  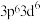 |
您最近半年使用:0次
2020-06-20更新
|
70次组卷
|
2卷引用:河北省邯郸市大名县第一中学2019-2020学年高二下学期第四次半月考化学试题(清北班)



