解题方法
1 . 下列描述中正确的是
| A.节日燃放的焰火与电子跃迁有关 |
| B.氢原子电子云的一个小黑点表示一个电子 |
| C.CS2是空间构型为V形的极性分子 |
D.HCN、SiF4和 的中心原子均为sp3杂化 的中心原子均为sp3杂化 |
您最近半年使用:0次
2020-08-21更新
|
232次组卷
|
2卷引用:河南省驻马店市2018-2019学年高二上学期期末考试化学试题
解题方法
2 . 元素的原子结构决定其性质和在元素周期表中的位置。下列说法正确的是
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.元素P、S、Cl的最高价氧化物对应的水化物的酸性依次增强 |
| D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
您最近半年使用:0次
3 . 中科院宁波研究所的“固态锂电池”即将量产,其技术世界领先。请完成下列问题:
(1)基态锂原子的电子排布式:______ ;基态锂原子中有_____ 种运动状态不同的电子。
(2)LiAlH4是重要的还原剂与储氢材料。其合成方法如下:① Na+Al+2H2 NaAlH4,②NaAlH4+LiCl
NaAlH4,②NaAlH4+LiCl LiAlH4+NaCl。
LiAlH4+NaCl。
①上述反应中涉及的元素的原子半径最大的是______ (填元素名称)。
②LiAlH4与水剧烈反应产生一种盐与 H2,写出反应的化学方程式:_______ 。
③LiAlH4中 H元素表现为-1价,Li元素为+1价,解释H表现出负价的理由:_______ 。
(3)Mg与 Al的电离能如下(kJ·mol-1):
第一电离能 Mg大于 Al,但第二电离能 Mg小于 Al,解释原因:_________ 。
(4)上述物质的元素中电负性最大的元素与电负性最小的元素形成的化合物的电子式为__________ 。
(1)基态锂原子的电子排布式:
(2)LiAlH4是重要的还原剂与储氢材料。其合成方法如下:① Na+Al+2H2
 NaAlH4,②NaAlH4+LiCl
NaAlH4,②NaAlH4+LiCl LiAlH4+NaCl。
LiAlH4+NaCl。①上述反应中涉及的元素的原子半径最大的是
②LiAlH4与水剧烈反应产生一种盐与 H2,写出反应的化学方程式:
③LiAlH4中 H元素表现为-1价,Li元素为+1价,解释H表现出负价的理由:
(3)Mg与 Al的电离能如下(kJ·mol-1):
| Mg | 737.7 | 1450.7 | … |
| Al | 577.5 | 1816.7 | … |
(4)上述物质的元素中电负性最大的元素与电负性最小的元素形成的化合物的电子式为
您最近半年使用:0次
2020-08-21更新
|
164次组卷
|
3卷引用:吉林省松原市扶余市第一中学2019-2020学年高二下学期期中考试化学试题
吉林省松原市扶余市第一中学2019-2020学年高二下学期期中考试化学试题山西省运城市2019-2020学年高二下学期期末测试化学试题(已下线)第01章 原子结构与元素性质(A卷基础强化篇)-2020-2021学年高二化学选择性必修2同步单元AB卷(新教材鲁科版)
4 . 下面关于多电子原子的核外电子的运动规律的叙述正确的是( )
①核外电子是分层运动的
②所有电子在同一区域里运动
③能量高的电子在离核近的区域内运动
④能量低的电子在离核近的区域内运动
①核外电子是分层运动的
②所有电子在同一区域里运动
③能量高的电子在离核近的区域内运动
④能量低的电子在离核近的区域内运动
| A.①④ | B.②③ | C.①③ | D.②④ |
您最近半年使用:0次
2020-08-12更新
|
488次组卷
|
5卷引用:4.1.1 原子结构 元素周期表 核素练习(2)——《高中新教材同步备课》(人教版 必修第一册)
(已下线)4.1.1 原子结构 元素周期表 核素练习(2)——《高中新教材同步备课》(人教版 必修第一册)(已下线)第04章 物质结构 元素周期律(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)黑龙江省伊春市伊美区第二中学2020-2021学年高一上学期期末考试化学试题新疆阿克苏市实验中学2022-2023学年高一上学期第二次月考(12月)化学试题内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高一上学期期末考试化学试题
5 . 某高效制氨剂的结构如下图,下列说法正确的是
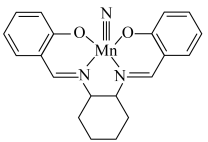

A. 元素电离能 元素电离能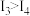 |
B.叁键键能: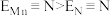 |
C.该化合物中的苯分子中含有大Ⅱ键 ,吡啶( ,吡啶(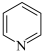 )中也含有大Ⅱ键 )中也含有大Ⅱ键 |
| D.该化合物中基态氧原子最高能级的电子云形状为球形 |
您最近半年使用:0次
解题方法
6 . 钾和碘的相关化合物在化工、医药、材料等领域有广泛的应用。回答下列问题:
(1)钾元素的焰色为紫色,该过程中其原子光谱属于______ 光谱(选填“吸收”或“发射”)。
(2)碘原子中,占据最高能级的电子的电子云轮廓图形状为______ 。
(3)请写出基态钾原子的核外电子排布式______ 。
(4)请比较KI与KCl晶体的熔点高低______ ,并说明理由:______ 。
(5)KIO3常用作食盐添加剂,其晶胞如图所示。

① 离子的立体构型为
离子的立体构型为______ 。
②已知KIO3晶胞的边长为apm,晶胞中K、I、O原子分别处于顶角、体心、面心位置。则每个K原子周围距离最短的O原子有______ 个。该晶胞的密度为______ g/cm3。
(1)钾元素的焰色为紫色,该过程中其原子光谱属于
(2)碘原子中,占据最高能级的电子的电子云轮廓图形状为
(3)请写出基态钾原子的核外电子排布式
(4)请比较KI与KCl晶体的熔点高低
(5)KIO3常用作食盐添加剂,其晶胞如图所示。

①
 离子的立体构型为
离子的立体构型为②已知KIO3晶胞的边长为apm,晶胞中K、I、O原子分别处于顶角、体心、面心位置。则每个K原子周围距离最短的O原子有
您最近半年使用:0次
7 . 下列各项叙述中,正确的是
| A.所有原子任一能层的s电子云轮廓图都是球形,且球的半径大小相同 |
| B.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| C.Cr原子的电子排布式是1s22s22p63s23p63d44s2 |
D.基态Ni原子的价电子排布图: |
您最近半年使用:0次
8 . 下列叙述中,不正确 的是
| A.在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析 |
| B.p轨道电子云形状是纺锤形 |
| C.电子的运动状态可从能层、能级、轨道、自旋方向4个方面进行描述 |
| D.3p能级上只有一个空轨道的原子和3p能级上有两个未成对电子的原子,对应为同一元素 |
您最近半年使用:0次
解题方法
9 . 下列有关说法不正确的是
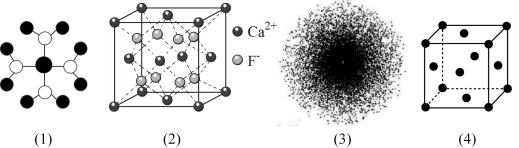

| A.水合铜离子的模型如图(1)所示,1个水合铜离子中有4个配位键 |
| B.CaF2晶体的晶胞如图(2)所示,与每个Ca2+ 等距离F- 有4个 |
| C.H原子的电子云图如图(3)所示,电子在原子核附近运动出现的概率大 |
| D.金属Cu中Cu原子晶胞模型如图(4),立方最密堆积,每个Cu原子的配位数均为8 |
您最近半年使用:0次
10 . 下列说法正确的是
| A.所有原子任一能层的s电子云轮廓图均为大小相同的球形 |
| B.对于排布在2s轨道上的电子,不能确定电子的自旋方向 |
| C.电子在同一能级的不同轨道排布时,尽可能分占不同的轨道,且自旋方向相反 |
| D.充有氖气的霓虹灯管通电时会发出红色光的主要原因,是电子由基态向激发态跃迁时吸收除红光以外的光线 |
您最近半年使用:0次



