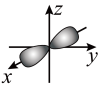
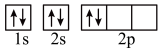
1 . 氮是生命物质的重要组成元素之一,含氮物质与人类的生活密切相关。氮原子最外层电子轨道表示式为:_____________ ;N4分子的空间结构如图: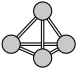 ,它是一种
,它是一种___________ 分子(填“极性”或“非极性”)。
 ,它是一种
,它是一种
您最近半年使用:0次
2 . 下列关于氢元素的说法中不正确的是
| A.氢元素是宇宙中最丰富的元素 |
| B.氢原子核外电子的电子云轮廓图是球形 |
| C.氢元素与其他元素形成的化合物都是共价化合物 |
| D.氢原子光谱是氢原子的电子跃迁产生的 |
您最近半年使用:0次
3 . 按原子核外电子排布,可把周期表里的元素划分成5个区。以下元素中属于ds区的是
| A.钙 | B.镍 | C.锌 | D.硒 |
您最近半年使用:0次
2020-10-13更新
|
243次组卷
|
4卷引用:湖北省武汉市五校联合体2019-2020学年高二下学期期中考试化学试题
湖北省武汉市五校联合体2019-2020学年高二下学期期中考试化学试题(已下线)1.1 原子结构(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)福建省莆田第七中学2020-2021学年高二下学期期中考试化学(A卷)试题河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题
名校
4 . 铋(83Bi)为第V A族元素,常见化合价为+3和+5。化合物NaBiO3为黄色固体,常温下微溶于水,在空气中逐渐分解产生Bi2O3、NaOH等物质。
(1)铋元素最外层电子分布在_____ 种能级中,共有_____ 种运动状态。
(2)铋酸钠NaBiO3中属于短周期元素的离子半径大小关系为_________ 。
(3)元素Na、Bi、O的金属性依次减弱,非金属性依次增强,请列举判断依据:_______ 。
(4)铋酸钠NaBiO3在空气中分解所得到产物中,化学键类型是______ 。
A.金属键 B.离子键 C.极性键 D.非极性键
(5)将NaBiO3加入MnSO4和H2SO4的混合溶液里加热,发生如下反应:
[ ]NaBiO3+[ ]MnSO4+[ ]H2SO4→[ ]Na2SO4+[ ]Bi2(SO4)3+[ ]NaMnO4+[ ]H2O
①配平该化学方程式,将系数填写在对应位置上。
______ NaBiO3+______ MnSO4+______ H2SO4→______ Na2SO4+______ Bi2(SO4)3+______ NaMnO4+______ H2O
②若有2mol氧化剂在该反应中被还原,则生成的MnO 被还原为Mn2+时,能将
被还原为Mn2+时,能将____ mol HCl氧化成Cl2。
(6)写出NaBiO3固体溶于HCl时发生反应的离子方程式:_________ 。
(1)铋元素最外层电子分布在
(2)铋酸钠NaBiO3中属于短周期元素的离子半径大小关系为
(3)元素Na、Bi、O的金属性依次减弱,非金属性依次增强,请列举判断依据:
(4)铋酸钠NaBiO3在空气中分解所得到产物中,化学键类型是
A.金属键 B.离子键 C.极性键 D.非极性键
(5)将NaBiO3加入MnSO4和H2SO4的混合溶液里加热,发生如下反应:
[ ]NaBiO3+[ ]MnSO4+[ ]H2SO4→[ ]Na2SO4+[ ]Bi2(SO4)3+[ ]NaMnO4+[ ]H2O
①配平该化学方程式,将系数填写在对应位置上。
②若有2mol氧化剂在该反应中被还原,则生成的MnO
 被还原为Mn2+时,能将
被还原为Mn2+时,能将(6)写出NaBiO3固体溶于HCl时发生反应的离子方程式:
您最近半年使用:0次
名校
5 . 下列说法错误的是( )
| A.原子结构模型的主要演变过程:道尔顿的原子结构模型→汤姆生的“葡萄干面包式”的原子结构模型→卢瑟福的带核的原子结构模型→玻尔的原子结构模型 |
| B.人类对原子结构的认识过程,说明了微观结构也要通过实验验证,同时要付出很大心血 |
| C.在原子结构分层排布中,M层容纳电子数最多为18,最少为8 |
| D.在化学反应过程中,原子核不发生变化,但原子最外层电子数可能发生变化 |
您最近半年使用:0次
2020-10-08更新
|
272次组卷
|
2卷引用:高一必修第一册(苏教2019)专题2 第三单元 人类对原子结构的认识
6 . 下列关于物质结构的说法错误的是
| A.晶格能:NaF>NaCl>NaBr |
| B.基态碳原子有三种能量不同的电子 |
C.CH4和 都是正四面体结构,键角均为109°28′ 都是正四面体结构,键角均为109°28′ |
| D.甲醛(HCHO)的键角约为120°,分子之间存在氢键 |
您最近半年使用:0次
2020-10-05更新
|
399次组卷
|
3卷引用:卓越联盟新高考省份2021届高三9月份检测化学试题
名校
解题方法
7 . 下列说法正确的是( )
| A.在多电子的原子里,能量高的电子通常在离核近的区域内运动 |
| B.核外电子总是先排在能量低的电子层上,例如只有M层排满后才排N层 |
| C.某原子M层电子数为L层电子数的4倍 |
| D.某离子的核电荷数与最外层电子数相等 |
您最近半年使用:0次
2020-09-24更新
|
663次组卷
|
7卷引用:鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律第1节 原子结构与元素性质 教材帮
鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律第1节 原子结构与元素性质 教材帮人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第一节 原子结构与元素周期表 教材帮高一必修第一册(苏教2019)专题2 第三单元 人类对原子结构的认识(已下线)4.1.1 原子结构-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)4.1.1 原子结构(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)福建省连城县第一中学2020-2021学年高一下学期第一次月考化学试题(已下线)4.1.1 原子结构-2021-2022学年高一化学10分钟课前预习练(人教版2019必修第一册)
8 . 下列表达方式或说法正确的是
A.CO2的分子模型示意图: |
B.p-p-π键电子云模型: |
C.某元素原子的电子排布图: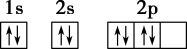 |
D.乙烯分子的比例模型: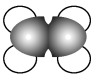 |
您最近半年使用:0次
2020-09-15更新
|
143次组卷
|
2卷引用:河北省唐山市玉田县第一中学2019-2020学年高二第二次阶段性考试化学试题
名校
9 . 下列说法中,正确的是( )
| A.在多电子的原子里,能量高的电子通常在离核近的区域内运动 |
| B.互为同素异形体的两科物质,其理化性质均相似 |
| C.两种微粒,若核外电子排布完全相同、则其化学性质一定相司 |
D.每个电子层最多客纳的电子数是 个(n分别对应1、2、3、……) 个(n分别对应1、2、3、……) |
您最近半年使用:0次