解题方法
1 . 下列化学用语的描述正确的是
A. 的 的 模型 模型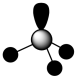 | B.锂原子最外层原子轨道示意图: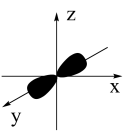 |
C.铬原子价电子排布式: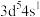 | D. 违反了洪特规则 违反了洪特规则 |
您最近一年使用:0次
2 . 下列对电子排布式或轨道表示式书写的评价错误的是
| 选项 | 电子排布式或轨道表示式 | 评价 |
| A | Br-的电子排布式:[Ar]3dl0 4s2 4p6 | 错误;违反能量最低原理 |
| B | O原子的轨道表示式: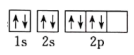 | 错误;违反洪特规则 |
| C | K原子的电子排布式:1s22s2 2p6 3s323p6 3d1 | 错误;违反能量最低原理 |
| D | F原子的轨道表示式: | 错误;违反泡利不相容原理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 镍在人类物质文明发展过程中起着重要作用,在现代合成工业中常用作催化剂。下列关于基态镍原子的价层电子描述错误的是
| A.价层电子数为10 | B.未成对电子的自旋方向均相同 |
| C.能量相同的电子有10个 | D.未成对电子数为2 |
您最近一年使用:0次
名校
解题方法
4 . 5-氨基四唑硝酸盐受热迅速生成以 为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是
为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是

 为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是
为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是 
| A.基态N原子核外电子的运动状态有3种 |
| B.阴离子的空间构型为三角锥形 |
| C.该化合物中五元环上的5个原子的杂化方式都相同 |
D.该化合物因存在类似于苯分子的大 键,所以非常稳定 键,所以非常稳定 |
您最近一年使用:0次
2022-04-29更新
|
981次组卷
|
7卷引用:山东省济宁市2022届高三第二次模拟考试化学试题
5 . 原子核外的某一能层最多能容纳的电子数目为18,则该能层是
| A.K能层 | B.L能层 | C.O能层 | D.M能层 |
您最近一年使用:0次
6 . 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元它们的原子序数依次增大。请根据下列相关信息,回答问题:
(1)写出A的元素符号____ ,D的元素名称____ 。
(2)B基态原子中能量最高的电子,其电子云在空间有____ 个方向,原子轨道呈____ 形。
(3)某同学根据上述信息,推断C基态原子的核外轨道表示式为 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了____ 。
(4)E元素原子核外有____ 种运动状态不同的电子。
(5)G位于____ 族____ 区,价电子排布式为____ 。
(6)检验F元素的方法是____ ,请用原子结构的知识解释产生此现象的原因是____ 。
| A元素原子半径在元素周期表中最小,也是宇宙中最丰富的元素 |
| B元素原子的核外p能级总电子数比s能级总电子数少1个 |
| C元素原子的第一至第四电离能分别是I1=738kJ·mol-1;I2=l451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4,原子半径同周期最小 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(4)E元素原子核外有
(5)G位于
(6)检验F元素的方法是
您最近一年使用:0次
名校
解题方法
7 . 铜及其化合物在生产生活中有着广泛的应用。请回答下列问题:
(1)铜元素在元素周期表中的位置为____ ,基态Cu原子核外有___ 种不同运动状态的电子。
(2)铜合金可用于制造航母螺旋桨。制造过程中产生的含铜废液可利用铜萃取剂M,通过如图反应实现铜离子的富集回收。

①M所含元素的电负性由大到小的顺序为____ (用元素符号表示)。
②X中采用sp3杂化的非金属原子有___ (填元素名称)。
③分子中的大Π键可用符号Π 表示,其中m为参与形成大Π键的原子数,n代表参与形成大Π键的电子数,则苯分子中的大π键表示为
表示,其中m为参与形成大Π键的原子数,n代表参与形成大Π键的电子数,则苯分子中的大π键表示为____ 。
(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体Y产生。Y分子的立体构型是___ ,Y的沸点比水低的主要原因是____ 。
(4)向蓝色[Cu(H2O)4]2+硫酸铜溶液中加入稍过量的氨水,溶液变为深蓝色[Cu(NH3)4]2+。通过上述实验现象可知,与Cu2+的配位能力:H2O____ NH3(填“大于”或“小于”)。
(1)铜元素在元素周期表中的位置为
(2)铜合金可用于制造航母螺旋桨。制造过程中产生的含铜废液可利用铜萃取剂M,通过如图反应实现铜离子的富集回收。

①M所含元素的电负性由大到小的顺序为
②X中采用sp3杂化的非金属原子有
③分子中的大Π键可用符号Π
 表示,其中m为参与形成大Π键的原子数,n代表参与形成大Π键的电子数,则苯分子中的大π键表示为
表示,其中m为参与形成大Π键的原子数,n代表参与形成大Π键的电子数,则苯分子中的大π键表示为(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体Y产生。Y分子的立体构型是
(4)向蓝色[Cu(H2O)4]2+硫酸铜溶液中加入稍过量的氨水,溶液变为深蓝色[Cu(NH3)4]2+。通过上述实验现象可知,与Cu2+的配位能力:H2O
您最近一年使用:0次
8 . 下列说法正确的是
| A.态Fe3+的最外层电子排布式为: 3s23p63d5 |
B.基态碳原子价电子轨道表示式: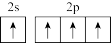 |
C.轨道表示式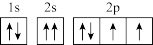 违背了洪特规则 违背了洪特规则 |
D.价层电子轨道表示式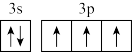 违背了泡利原理 违背了泡利原理 |
您最近一年使用:0次
2022-03-17更新
|
735次组卷
|
4卷引用:河北省石家庄市第二中学2022年高二寒假考试化学试题
9 . 下列轨道表示式中哪个是氧的基态原子______ ?为什么?______
A. B.
B.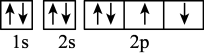 C.
C.
A.
 B.
B. C.
C.
您最近一年使用:0次
解题方法
10 . 泡利原理
(1)自旋:电子自旋有顺时针和逆时针两种状态,常用_______ 表示自旋状态相反的电子。
(2)泡利原理:在一个原子轨道里,最多只能容纳_______ 个电子,而且它们的自旋状态_______ 。
(1)自旋:电子自旋有顺时针和逆时针两种状态,常用
(2)泡利原理:在一个原子轨道里,最多只能容纳
您最近一年使用:0次
2022-02-16更新
|
163次组卷
|
2卷引用:课前-1.1.3 泡利原理、洪特规则、能量最低原理-人教版2019选择性必修2



