1 . 现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的1/6 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)G的元素名称为____________ 。
(2)A、B、C三种元素电负性由大到小的顺序为_____________ (用元素符号表示),第一电离能D______ Al(填“>”“<”或“=”),其原因是______________________ 。
(3)E3+的离子符号为________________ 。
(4)F元素基态原子的电子排布式为________________ 。
(5)G元素可能的性质_______________ 。
A.其单质可作为半导体材料 B.其电负性大于磷
C.最高价氧化物对应的水化物是强酸 D.其第一电离能小
(1)G的元素名称为
(2)A、B、C三种元素电负性由大到小的顺序为
(3)E3+的离子符号为
(4)F元素基态原子的电子排布式为
(5)G元素可能的性质
A.其单质可作为半导体材料 B.其电负性大于磷
C.最高价氧化物对应的水化物是强酸 D.其第一电离能小
您最近一年使用:0次
2020-08-08更新
|
126次组卷
|
2卷引用:福建省福州市四校联盟2021-2022学年高二下学期期中联考化学试题
名校
解题方法
2 . 不能说明X的电负性比Y的大的是
| A.X原子的最外层电子数比Y原子的最外层电子数多 |
| B.X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
| C.与H2化合时X单质比Y单质容易 |
| D.X单质可以把Y从其氢化物中置换出来 |
您最近一年使用:0次
2020-08-08更新
|
98次组卷
|
2卷引用:福建省福州教育学院附属中学2021-2022学年高二下学期3月月考化学试题
3 . 短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法正确的是
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | H3ZO4 | |||
 溶液对应的pH(25℃) 溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
| A.元素电负性:Z<W | B.简单离子半径:W<Y |
| C.元素第一电离能:Z<W | D.简单氢化物的沸点:X<Z |
您最近一年使用:0次
2020-07-11更新
|
8523次组卷
|
45卷引用:福建省福州第一中学2021-2022学年高二下学期期中考试化学试题
福建省福州第一中学2021-2022学年高二下学期期中考试化学试题2020年天津卷化学高考试题(已下线)专题06 物质结构 元素周期律-2020年高考真题和模拟题化学分项汇编(已下线)第8单元 原子结构 元素周期律(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷山东省潍坊市诸城一中2021届高三11月份模拟化学试题(已下线)小题必刷22 元素周期表(律)及其应用——2021年高考化学一轮复习小题必刷(通用版)(人教版2019)选择性必修2 第一章 原子结构与性质 章末综合检测卷(已下线)热点6 物质结构与元素周期律-2021年高考化学专练【热点·重点·难点】(新高考)(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)专题04 物质结构和元素周期律——备战2021年高考化学纠错笔记(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练甘肃省兰州市第一中学2020-2021学年高二下学期4月月考化学试题湖北省沙市第五中学2020-2021学年高二下学期3月月考化学试题(已下线)小题15 元素周期表、律(根据物质性质角度的元素推断)——备战2021年高考化学经典小题考前必刷(全国通用)山东省济南大学城实验高级中学2021届高三4月阶段性测试化学试题河南省开封市铁路中学2020-2021学年高二下学期期中考试化学试题(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第36讲 原子结构与性质(精练)-2022年一轮复习讲练测(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题04 物质结构与元素周期律—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)2020年天津卷化学高考真题变式题1-12湖北省沙市中学2021-2022学年高二上学期期末考试化学试题广东省云浮市云安区云安中学2021-2022学年高二下学期第一次统测化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)专题1~2 综合检测(提升卷)(已下线)第14讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第29讲 原子结构与性质(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第29讲 原子结构与性质(讲)-2023年高考化学一轮复习讲练测(新教材新高考)北京市第八十中学2022-2023学年高三上学期期末测试化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型80 用表格承载信息考查元素周期律(已下线)第五章 物质结构与性质元素周期律 第27练 元素周期表和元素周期律北京市第八十中学2023届高三下学期二模适应考试化学试题(已下线)专题07 元素周期表与元素周期律(已下线)第2讲 元素素周期表 元素周期律天津市耀华中学2023-2024学年度高三上学期开学检测化学试题天津市红桥区2023-2024学年高三上学期期中考试化学试题河北省保定市唐县第一中学2023-2024学年高二上学期12月期中考试化学试题河南省南阳市第一中学校2023-2024学年高二上学期12月月考化学试题北京师范大学附属实验中学2023-2024学年高二下学期开学检测化学试题云南省保山市腾冲市第八中学2024届高三上学期期末模拟考试化学试卷广东省四会中学、广信中学2023-2024学年高二下学期第一次联合考试化学试题北京市第十四中学2023-2024学年高三下学期三模化学试题
名校
解题方法
4 . 现有四种元素的基态原子的电子排布式如下: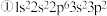 ;
; 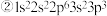 ;
; 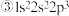 ;
;  则下列有关比较中正确的是
则下列有关比较中正确的是
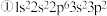 ;
; 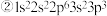 ;
; 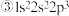 ;
;  则下列有关比较中正确的是
则下列有关比较中正确的是A.电负性: | B.原子半径: |
C.第一电离能: | D.最高正化合价: |
您最近一年使用:0次
2019-12-22更新
|
431次组卷
|
8卷引用:福建省福州第一中学2021-2022学年高二下学期期中考试化学试题
福建省福州第一中学2021-2022学年高二下学期期中考试化学试题2016-2017学年四川省成都市九校高二下学期期中联考化学试卷2016-2017学年山东省淄博市高青一中、淄博实验中学高二下学期期中联考化学试卷【全国百强校】内蒙古北方重工业集团有限公司第三中学2017-2018学年高二下学期期末考试化学试题湖北省黄冈市浠水实验高中2019—2020学年高二上学期12月月考化学试题山西省实验中学2019-2020学年高二下学期第一次月考化学试题(已下线)专题13 原子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)四川省广安市第二中学校2022-2023学年高二下学期期中考试化学试题
解题方法
5 . 硒化锌是一种透明黄色半导体,也可作红外光学材料,熔点1520℃。
(1)锌离子的电子排布式是_____________ 。
(2)根据元素周期律,电负性S______ Se,第一电离能Se______ As(填“>”或“<”)。
(3)H2O的沸点______________ (填“>”或“<”)H2Se的沸点,其原因是:______ 。
(4)NaCl晶胞如图所示,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。晶胞中Na+的配位数为____ ,若晶胞参数为a pm,阿伏伽德罗常数的值用NA表示,若晶体密度为_______ g·cm﹣3。(列出表达式)。
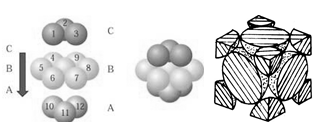
(5)铜晶体中铜原子的堆积方式如图所示,铜晶体中原子的堆积模型属于_______ 。若已知铜的原子半径为rcm,表示原子空间占有率的表达式为__________ 。
(1)锌离子的电子排布式是
(2)根据元素周期律,电负性S
(3)H2O的沸点
(4)NaCl晶胞如图所示,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。晶胞中Na+的配位数为
(5)铜晶体中铜原子的堆积方式如图所示,铜晶体中原子的堆积模型属于
您最近一年使用:0次
6 . Ⅰ、用下列:①H2O ②H2O2 ③Ba(OH)2 ④Na2O2 ⑤Cl2 ⑥Ar ⑦CO2 等物质填空。 (1—4小题填序号)
(1) 由离子键和非极性键构成的是_________________
(2) 由极性键和非极性键构成的是_________________
(3) 不存在化学键的是________
(4) 共价化合物有_________________
(5) 写出下列物质的电子式:Na2O2___________
Ⅱ、某元素原子的价电子构型为4s24p1,它属于第________ 周期________ 族,属________ 区元素
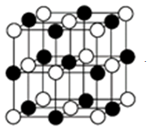
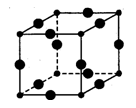
Ⅲ、Cu3N的晶胞结构如图,N3-的配位数为____ ,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为_________ g·cm-3。(阿伏加德罗常数用NA表示,Cu、N相对分子质量为64、14)
(1) 由离子键和非极性键构成的是
(2) 由极性键和非极性键构成的是
(3) 不存在化学键的是
(4) 共价化合物有
(5) 写出下列物质的电子式:Na2O2
Ⅱ、某元素原子的价电子构型为4s24p1,它属于第
Ⅲ、Cu3N的晶胞结构如图,N3-的配位数为

您最近一年使用:0次



