解题方法
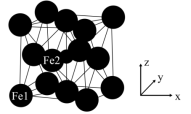
1 . X、Y、Z、R、Q是原子序数依次增大的短周期主族元素,其中基态X的最高能层中含有一个空轨道;同周期主族元素中只有两种元素的第一电离能大于Z;五种元素可形成某种离子液体阴离子的结构如下图所示。错误 的是

A.离子半径: | B.简单氢化物的沸点: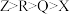 |
C.该阴离子中原子的价层孤电子对数: | D.电负性: |
您最近一年使用:0次
名校
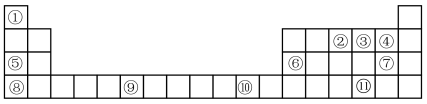
2 . 表格为门捷列夫元素周期表的一部分,其中的编号代表对应的元素。用元素符号回答下列问题:
(1)基态F原子有___________ 种运动状态的电子。
(2)元素③⑪电负性较大的是___________ ;Se的原子结构示意图为___________ 。
(3)元素铬的基态原子的价电子排布图为:___________ 。
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为___________ 。
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为________ 。
(6)②③的简单气态氢化物中较稳定的是___________ (填化学式),元素⑥⑦的最高价氧化物的水化物相互反应的离子方程式为___________ 。
(1)基态F原子有
(2)元素③⑪电负性较大的是
(3)元素铬的基态原子的价电子排布图为:
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为
(6)②③的简单气态氢化物中较稳定的是
您最近一年使用:0次
2023-09-16更新
|
254次组卷
|
2卷引用:福建省龙岩市连城县第一中学2022-2023学年高二下学期3月月考化学试题
3 . 现有四种元素基态原子的电子排布式如下。则下列有关比较中不正确的是
①1s22s22p5②1s22s22p3③1s22s22p63s23p4④1s22s22p63s23p3
①1s22s22p5②1s22s22p3③1s22s22p63s23p4④1s22s22p63s23p3
| A.电负性:①>②>③>④ |
| B.第一电离能:①>②>③>④ |
| C.原子半径:④>③>②>① |
| D.②、③的简单氢化物,中心原子均为sp3杂化,且均为极性分子 |
您最近一年使用:0次
名校
解题方法
4 . 2023年1月30日,中国科学院朱庆山团队研究六方相砷化镍(NiAs)型到正交相磷化锰(MnP)型结构转变,实现了对锂硫催化剂的精确设计。回答下列问题:
(1)Li、P、S三种元素中,电负性最小的是___________ 。第三周期元素中第一电离能比P大的元素有___________ 种。
(2)基态As原子的电子排布式为___________ 。
(3)PH3、AsH3中沸点较高的是___________ ,其主要原因是___________ 。
(4)Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],该配合物中锰原子的配位数为___________ 。
(5)等物质的量的CH3CN和CO中,π键数目之比___________ 。
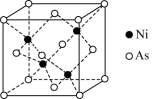
(6)NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为NA,晶体的密度为ρg/cm3,则该晶胞中最近的砷原子之间的距离为___________ pm。
(1)Li、P、S三种元素中,电负性最小的是
(2)基态As原子的电子排布式为
(3)PH3、AsH3中沸点较高的是
(4)Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],该配合物中锰原子的配位数为
(5)等物质的量的CH3CN和CO中,π键数目之比
(6)NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为NA,晶体的密度为ρg/cm3,则该晶胞中最近的砷原子之间的距离为

您最近一年使用:0次
名校
解题方法
5 . 下列类比或推理合理的是
| 选项 | 已知 | 方法 | 结论 |
| A | 钠保存在煤油中 | 类比 | 锂保存在煤油中 |
| B |  是离子化合物 是离子化合物 | 类比 |  是离子化合物 是离子化合物 |
| C | 非金属性: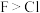 | 推理 | 沸点: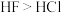 |
| D |  是正盐 是正盐 | 推理 |  是一元酸 是一元酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-11更新
|
449次组卷
|
3卷引用:福建省龙岩市上杭县第一中学2024届高三上学期10月月考化学试题
名校
解题方法
6 . 下列有关合成药物胃复安的说法不正确的是
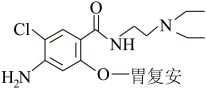
| A.分子中碳原子有2种杂化类型 |
| B.该分子组成元素的电负性由大到小的顺序为:O>N>C>H |
| C.该分子组成元素第一电离能最大的是O |
| D.分子中所有氮原子上都有一对孤电子对 |
您最近一年使用:0次
2023-03-16更新
|
248次组卷
|
2卷引用:福建省龙岩第一中学2022-2023学年高二下学期第一次月考化学试题
名校
解题方法
7 . 硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参数为pnm,乙图为晶胞的俯视图,下列说法正确的是
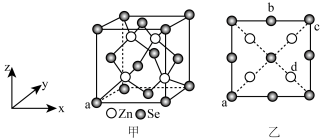
| A.晶胞中硒原子的配位数为12 |
B.晶胞中d点原子分数坐标为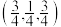 |
C.相邻两个Zn原子的最短距离为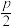 nm nm |
| D.电负性:Zn>Se |
您最近一年使用:0次
2023-03-03更新
|
1854次组卷
|
10卷引用:福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题
福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题山东省济宁市2023届高三一模考试(3月)化学试题山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题(已下线)专题十 晶胞示意图(练)河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题河南省驻马店市环际大联考2022-2023学年高二下学期4月期中考试化学试题(已下线)热点08 金属晶体和离子晶体山东省烟台市第一中学2023-2024学年高三下学期3月月考化学试题
名校
解题方法
8 . 科学研究发现铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,因此受到研究人员的广泛关注。γ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去_______ 轨道电子。
(2)NH3中H−N−H的键角比NH 中H−N−H的键角
中H−N−H的键角_______ (填“大”或“小”)。
(3)羰基铁粉[Fe(CO)5]中配位原子为_______ 。
(4)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为_______ 。
(5)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为_______ 。已知该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为_______ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)NH3中H−N−H的键角比NH
 中H−N−H的键角
中H−N−H的键角(3)羰基铁粉[Fe(CO)5]中配位原子为
(4)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(5)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(
 ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为
您最近一年使用:0次
2022-08-29更新
|
88次组卷
|
2卷引用:福建省龙岩第一中学2022-2023学年高三上学期第一次月考化学试题
名校
解题方法
9 . 某种锂盐的结构如图所示,其阴离子由W、X、Y、Z四种同周期主族元素构成,X原子的最外层电子数是W原子的次外层电子数的3倍,化合物中除Li+外其它原子均满足8电子稳定结构。下列说法正确的是
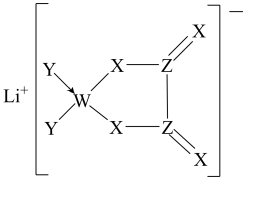

| A.W位于第2周期IVA族 | B.原子半径:Z>X>Y |
| C.元素电负性:Y>Z>X | D.最高化合价:Y>Z>W |
您最近一年使用:0次
2022-05-07更新
|
430次组卷
|
6卷引用:福建省龙岩市2022届高中毕业班第三次教学质量检测化学试题
解题方法
10 . 前四周期的A、B、C、D、E、F六种元素,原子序数依次增大。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上未成对的电子数最多;C元素为最活泼的非金属元素;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
(1)E元素在周期表中位置为_______ ,E3+价电子轨道表示式为_______ 。
(2)B、C、F三种元素电负性由大到小的顺序为_______ (用元素符号表示),第一电离能D_______ (填“>”、“<”或“=”)Al,其原因是_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)F元素可能的性质_______ (填标号)。
 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。(1)E元素在周期表中位置为
(2)B、C、F三种元素电负性由大到小的顺序为
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)F元素可能的性质
| A.其单质可作半导体材料 |
| B.存在-3、+3、+5等多种化合价 |
| C.最高价氧化物对应的水化物是强酸 |
| D.单质还原性弱于磷单质 |
您最近一年使用:0次
2022-04-16更新
|
298次组卷
|
3卷引用:福建省龙岩市一级校联盟(九校)2021-2022学年高二下学期期中联考化学试题



