1 . 用于检测室内空气中甲醛含量的一种常见试剂 的结构如图所示。下列关于该材料组成元素的说法正确的是
的结构如图所示。下列关于该材料组成元素的说法正确的是
 的结构如图所示。下列关于该材料组成元素的说法正确的是
的结构如图所示。下列关于该材料组成元素的说法正确的是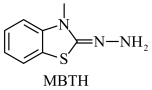
A.4种元素的电负性: |
| B.4种元素均位于p区 |
C.基态C原子的轨道表示式为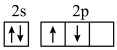 |
| D.基态S原子核外电子有16种运动状态 |
您最近一年使用:0次
2 . 下列对价电子构型为2s22p5的元素描述正确的是
| A.电负性最大 | B.最高正价为+7 |
| C.同周期中第一电离能最大 | D.同周期中原子半径最大 |
您最近一年使用:0次
3 . 离子液体是指由体积较大的阴、阳离子组成,并且在室温或接近室温下呈液态的盐,也称为低温熔融盐。有许多优点,例如难挥发,有良好的导电性,可作溶剂、电解质、催化剂等。1-正丁基-3-甲基咪唑六氟磷酸盐是一种离子液体,结构简式如图,下列关于它的叙述正确的是
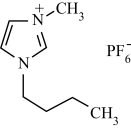 或
或
A.该新型化合物含有的C、N、P元素均为 杂化 杂化 |
| B.1-正丁基-3-甲基咪唑六氟磷酸盐属于含共价键的离子化合物 |
| C.电负性:F>N>H>C |
| D.该新型化合物的组成元素全部位于元素周期表p区 |
您最近一年使用:0次
4 . 我国某有机所研究团队合成一种盐,其阴离子结构如图所示。短周期主族元素X、Y、Z、R的原子序数依次增大,X、Y、Z的原子序数之和为23,下列有关叙述不正确的是
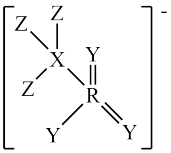
| A.电负性:Z>Y>R | B.简单氢化物的稳定性:Z>Y>X |
C.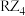 的键角和 的键角和 的键角相等 的键角相等 | D.X的单质可能是共价晶体 |
您最近一年使用:0次
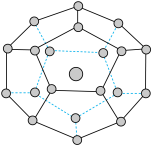
5 . 2017年5月海底天然气水合物(俗称可燃冰)试采成功,这是我国能源开发的一次历史性突破。一定条件下,CH4和CO2都能与H2O形成如图所示的笼状结构(表面的小球是水分子,内部的大球是CH4分子或CO2分子;“可燃冰”是CH4与H2O形成的水合物),其相关参数见下表。
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为___________ ;碳原子的最高能级的符号是___________ ,其电子云形状是___________ 。
(2) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子的空间结构为___________ 。
(3)为开采海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为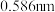 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________ 。
(4)“可燃冰”中分子间存在的作用力是氢键和___________ ,上图中最小的环中连接的原子总数是___________ 。
| 参数分子 | 分子直径/nm | 分子与H2O的结合能E(kJ·mol-1) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为
(2)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为(3)为开采海底的“可燃冰”,有科学家提出用
 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为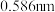 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是(4)“可燃冰”中分子间存在的作用力是氢键和
您最近一年使用:0次
名校
解题方法
6 . 3-氨基-1-金刚烷醇可用于合成药物维格列汀(治疗2型糖尿病),其分子结构如下图所示。下列说法不正确的是

A.分子中O原子和N原子均为 杂化 杂化 | B.分子中的键角: |
C.电负性: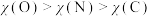 | D.第一电离能: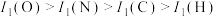 |
您最近一年使用:0次
2024-04-15更新
|
175次组卷
|
2卷引用:江西省新余市2023-2024学年高三上学期第一次调研考试化学试卷
名校
解题方法
7 . 下列性质的比较正确的是
A.单质的熔点: | B.键能: |
C.电负性: | D.微粒半径: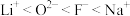 |
您最近一年使用:0次
名校
解题方法
8 . 下列说法不正确的是
| A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶规律解释 |
| B.光(辐射)是电子跃迁释放能量的重要形式 |
C. 的立体构型为三角锥形,中心原子的杂化方式为 的立体构型为三角锥形,中心原子的杂化方式为 |
| D.酸性强弱:三氟乙酸>三氯乙酸>乙酸 |
您最近一年使用:0次
9 . 以下说法中错误的是
A.在①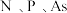 和② 和②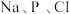 中,元素的电负性随原子序数增大而递增的是② 中,元素的电负性随原子序数增大而递增的是② |
B.在①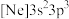 和② 和②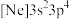 中,原子的第一电离能大的是② 中,原子的第一电离能大的是② |
C.某元素原子的部分逐级电离能 分别为,738、1451、7733、10540、13630,该元素可能在第三周期第ⅡA族 分别为,738、1451、7733、10540、13630,该元素可能在第三周期第ⅡA族 |
D.在共价键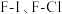 和 和 中,极性最强的是 中,极性最强的是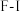 |
您最近一年使用:0次
10 . 银锌电池以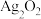 为正极、Zn为负极,KOH溶液作电解质,放电反应为:
为正极、Zn为负极,KOH溶液作电解质,放电反应为: ,下列说法
,下列说法不正确 的是
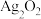 为正极、Zn为负极,KOH溶液作电解质,放电反应为:
为正极、Zn为负极,KOH溶液作电解质,放电反应为: ,下列说法
,下列说法A.基态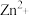 的价电子排布式: 的价电子排布式: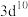 | B.电负性: |
C. 的电子式: 的电子式: | D.第一电离能: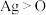 |
您最近一年使用:0次



