 具有良好的导电能力,为锂离子电池的发展做出了重要贡献,其晶胞结构如图所示,其中
具有良好的导电能力,为锂离子电池的发展做出了重要贡献,其晶胞结构如图所示,其中 位于体心。下列说法正确的是
位于体心。下列说法正确的是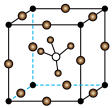
A.该晶胞中 位于体心和棱心 位于体心和棱心 |
B.电负性: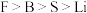 |
C. 周围距离最近且相等的 周围距离最近且相等的 的个数为4 的个数为4 |
D.若晶胞参数为 ,则晶体密度为 ,则晶体密度为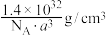 |
 )的新方法如下:
)的新方法如下: 、
、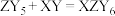 ,其中X、Y、Z、M、Q为原子序数依次增大的前20号主族元素,X、Q为金属元素,Y、M为同主族元素,且Y是电负性最大的元素,基态Z原子的成对电子数与未成对电子数之比为4∶1。下列说法错误的是
,其中X、Y、Z、M、Q为原子序数依次增大的前20号主族元素,X、Q为金属元素,Y、M为同主族元素,且Y是电负性最大的元素,基态Z原子的成对电子数与未成对电子数之比为4∶1。下列说法错误的是| A.基态X原子核外只有1个未成对电子 | B.第一电离能:Q<Z<M<Y |
| C.简单离子半径:Q>M>Y | D. 、 、 均为三角锥形分子 均为三角锥形分子 |
3 . 根据信息回答下列问题:
(1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
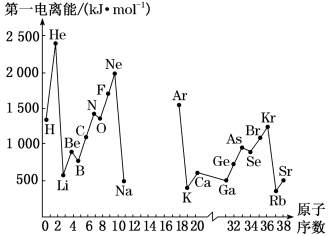
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
②图中Ge元素中未成对电子有
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出部分元素的电负性:
元素 | Al | B | Be | C | Cl | F | Li |
电负性 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | |
元素 | Mg | N | Na | O | P | S | Si |
电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①根据表中给出的数据,可推知元素的电负性具有的变化规律
②通过分析电负性值变化规律,确定Al元素电负性值的最小范围
③判断下列物质是离子化合物还是共价化合物:
A Li3N B PCl3 C MgCl2 D SiC
Ⅰ.属于离子化合物的是
Ⅱ.属于共价化合物的是
请设计一个实验方案证明上述所得到的结论
 ,M基态原子的所有s轨道上共有6个电子。下列说法错误的是
,M基态原子的所有s轨道上共有6个电子。下列说法错误的是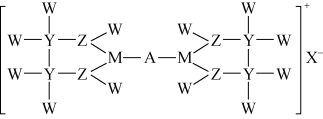
| A.化合物中除A外,其他原子均达到稀有气体的稳定结构 |
| B.W与M、Z均可形成18电子微粒,沸点前者高 |
C.化合物 的空间结构为正四面体形,可做灭火剂 的空间结构为正四面体形,可做灭火剂 |
D.电负性: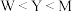 |
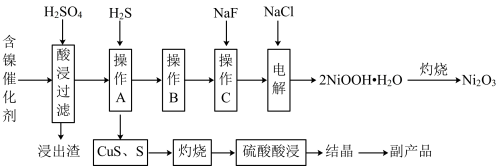
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
请回答下列问题:
(1)加快酸浸速率的常用措施有
(2)“浸出渣”主要成分为
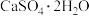 和
和(3)“操作B”的过程是:先在40~50℃温度下加入
 ,其作用是
,其作用是(4)在碱性条件下,电解产生
 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到 沉淀的离子方程式
沉淀的离子方程式(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(
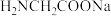 )即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
)即可得到它,配合物A中的配位原子的电负性由大到小的顺序是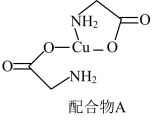
 与
与 同周期,
同周期, 与
与 对应的简单离子核外电子排布相同,且
对应的简单离子核外电子排布相同,且 、
、 、
、 的最外层电子数之和等于
的最外层电子数之和等于 的最外层电子数,下列说法错误的是
的最外层电子数,下列说法错误的是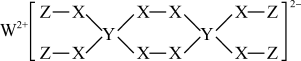
A.四种元素中 的电负性最大 的电负性最大 |
B. 该物质中含有 该物质中含有 配位键 配位键 |
C. 的最高价氧化物对应的水化物是一元弱酸 的最高价氧化物对应的水化物是一元弱酸 |
D.第一电离能介于 与 与 之间的同周期元素只有3种 之间的同周期元素只有3种 |
| A.电负性:Q>J;第一电离能:Y>Z | B.最高价含氧酸的酸性:Q>J |
C. 、 、 的中心原子杂化方式相同 的中心原子杂化方式相同 | D.简单离子半径:Y>Z、J>Q |

A.分子中存在 键、 键、 键 键 |
B.分子中的 键的键能小于 键的键能小于 键的键能 键的键能 |
C.分子中N、O、P原子的第一电离能由大到小的关系为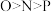 |
| D.分子中含有手性碳原子 |
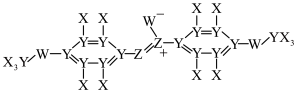
| A.电负性:W>Z>Y | B.第一电离能:Z>W>Y |
| C.常见单质分子键能:X>W>Z | D.简单氢化物沸点:W>Z>Y |
| 物质结构或性质 | 解释 | |
| A | 键角: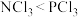 | N的电负性比P大,孤电子对对成键电子对的斥力比较大 |
| B | 稳定性:HF>HCl | HF分子间可以形成氢键,HCl没有氢键 |
| C | 配位键的稳定性: |  中O电负性更大,因而形成的配位键更稳定 中O电负性更大,因而形成的配位键更稳定 |
| D | 电子云半径:2s<4s | 4s电子的能量高,在离核更远的区域出现的概率大 |
| A.A | B.B | C.C | D.D |



