解题方法
1 . 碳、氧、氮、镁、铬、铁、锌是几种重要的元素,请回答下列问题:
(1)铝的基态原子的价电子排布式是_________________ 。
(2)用水解法制备一种磁性材料铁氧体时常加入尿素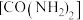 、醋酸钠等碱性物质。尿素分子中所含非金属元素的电负性由大到小的顺序是
、醋酸钠等碱性物质。尿素分子中所含非金属元素的电负性由大到小的顺序是_________ ,分子中 键和
键和 键的数目之比为
键的数目之比为__________ 。醋酸钠中碳原子的杂化类型为____________ 。
(3)Mg2+、 等金属离子与
等金属离子与 、
、 能形成稳定金属配离子,其中形成的化合物稳定性相对较高的是
能形成稳定金属配离子,其中形成的化合物稳定性相对较高的是__________  填“
填“ ”或“
”或“ ”
” ,其原因是
,其原因是__________ ;已知氨 熔点:
熔点: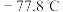 、沸点:
、沸点: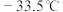 ,联氨
,联氨 熔点:
熔点: 、沸点:
、沸点: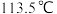 ,解释其熔沸点高低的主要原因:
,解释其熔沸点高低的主要原因:______________ 。
(4)碳溶解在 中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为
中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为__________ 。若晶体密度为 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为__________ 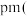 阿伏加 德罗常数的值用
阿伏加 德罗常数的值用 表示,写出简化后的计算式即可
表示,写出简化后的计算式即可 。
。

(1)铝的基态原子的价电子排布式是
(2)用水解法制备一种磁性材料铁氧体时常加入尿素
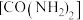 、醋酸钠等碱性物质。尿素分子中所含非金属元素的电负性由大到小的顺序是
、醋酸钠等碱性物质。尿素分子中所含非金属元素的电负性由大到小的顺序是 键和
键和 键的数目之比为
键的数目之比为(3)Mg2+、
 等金属离子与
等金属离子与 、
、 能形成稳定金属配离子,其中形成的化合物稳定性相对较高的是
能形成稳定金属配离子,其中形成的化合物稳定性相对较高的是 填“
填“ ”或“
”或“ ”
” ,其原因是
,其原因是 熔点:
熔点: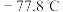 、沸点:
、沸点: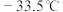 ,联氨
,联氨 熔点:
熔点: 、沸点:
、沸点: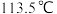 ,解释其熔沸点高低的主要原因:
,解释其熔沸点高低的主要原因:(4)碳溶解在
 中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为
中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为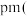 阿伏加 德罗常数的值用
阿伏加 德罗常数的值用 表示,写出简化后的计算式即可
表示,写出简化后的计算式即可 。
。 
您最近一年使用:0次
2020-01-27更新
|
189次组卷
|
2卷引用:2020届高三化学二轮冲刺新题专练——物质结构与性质
解题方法
2 . 坦桑石是一种世界公认的新兴宝石,这种宝石于1967年首次在赤道雪山脚下的阿鲁沙地区被发现。坦桑石的主要化学成分为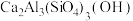 ,还可含有V、Cr、Mn等元素。
,还可含有V、Cr、Mn等元素。
 下列状态的铝中,电离最外层的一个电子所需能量最大的是
下列状态的铝中,电离最外层的一个电子所需能量最大的是________  填序号
填序号 。
。
①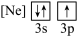 ②
②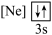 ③
③ ④
④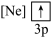
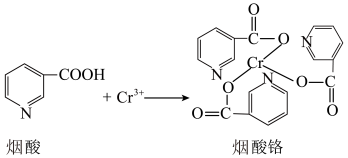
 烟酸铬是铬的一种化合物,其合成过程如下:
烟酸铬是铬的一种化合物,其合成过程如下:
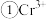 核外电子排布式为
核外电子排布式为________ 。
 、C、N、O的电负性由大到小的顺序是
、C、N、O的电负性由大到小的顺序是_________ 。
 烟酸中碳、氮原子的杂化方式分别为
烟酸中碳、氮原子的杂化方式分别为________ 、________ 。
 分子中的大
分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数
键的电子数 如二氧化碳分子中的大
如二氧化碳分子中的大 键可表示为
键可表示为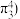 ,则烟酸中的大
,则烟酸中的大 键应表示为
键应表示为___________ 。
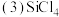 、
、 都极易水解。
都极易水解。 、
、 都属于
都属于______  填“极性”或“非极性”
填“极性”或“非极性” 分子,其熔点的关系为
分子,其熔点的关系为
________  填“
填“ ”“
”“ ”或“
”或“ ”
”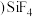 。
。
 将Mn掺入GaAs晶体
将Mn掺入GaAs晶体 图甲
图甲 可得到稀磁性半导体材料
可得到稀磁性半导体材料 图乙
图乙 ,图甲、图乙晶体结构不变。
,图甲、图乙晶体结构不变。
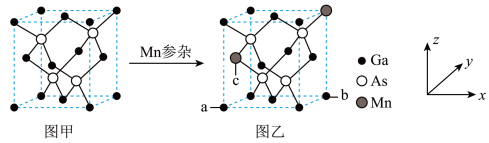
 图乙中a点和b点的原子坐标参数分别为
图乙中a点和b点的原子坐标参数分别为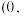 0,
0, 和
和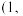 1,
1, ,则c点的原子坐标参数为
,则c点的原子坐标参数为________ 。
 设图甲晶体的密度为
设图甲晶体的密度为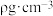 ,用
,用 表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为
表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为________________ pm。
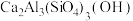 ,还可含有V、Cr、Mn等元素。
,还可含有V、Cr、Mn等元素。  下列状态的铝中,电离最外层的一个电子所需能量最大的是
下列状态的铝中,电离最外层的一个电子所需能量最大的是 填序号
填序号 。
。①
 ②
②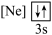 ③
③ ④
④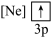
 烟酸铬是铬的一种化合物,其合成过程如下:
烟酸铬是铬的一种化合物,其合成过程如下:
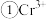 核外电子排布式为
核外电子排布式为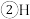 、C、N、O的电负性由大到小的顺序是
、C、N、O的电负性由大到小的顺序是 烟酸中碳、氮原子的杂化方式分别为
烟酸中碳、氮原子的杂化方式分别为 分子中的大
分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数
键的电子数 如二氧化碳分子中的大
如二氧化碳分子中的大 键可表示为
键可表示为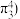 ,则烟酸中的大
,则烟酸中的大 键应表示为
键应表示为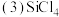 、
、 都极易水解。
都极易水解。 、
、 都属于
都属于 填“极性”或“非极性”
填“极性”或“非极性” 分子,其熔点的关系为
分子,其熔点的关系为
 填“
填“ ”“
”“ ”或“
”或“ ”
”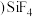 。
。 将Mn掺入GaAs晶体
将Mn掺入GaAs晶体 图甲
图甲 可得到稀磁性半导体材料
可得到稀磁性半导体材料 图乙
图乙 ,图甲、图乙晶体结构不变。
,图甲、图乙晶体结构不变。
 图乙中a点和b点的原子坐标参数分别为
图乙中a点和b点的原子坐标参数分别为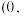 0,
0, 和
和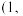 1,
1, ,则c点的原子坐标参数为
,则c点的原子坐标参数为 设图甲晶体的密度为
设图甲晶体的密度为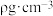 ,用
,用 表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为
表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为
您最近一年使用:0次
名校
解题方法
3 . 碳是地球上组成生命的最基本的元素之一。根据要求回答下列问题:
(1)碳原子的价电子排布式______________ ,核外有_________ 种不同运动状态的电子。
(2)碳可以形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。
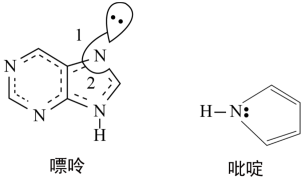
①嘌呤中所有元素的电负性由大到小的顺序__________________ 。
②嘌呤中轨道之间的夹角∠1比∠2大,解释原因__________________ 。
③吡啶结构中N原子的杂化方式__________________ 。
④分子中的大π键可用符号 表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为
表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为__________ 。
(3)碳元素能形成CO、CO2、H2CO3等多种无机化合物。
①二氧化碳的晶体叫做干冰,每个二氧化碳分子周围通常有__________ 个紧邻的分子。
②在CO转化成CO2的反应过程中,下列说法正确的是__________ 。
A.分子中孤电子对数不变 B.分子的极性发生变化
C.原子间成键方式发生改变 D.分子晶体的熔沸点升高
③H2CO3与H3PO4均有1个非羟基氧,H3PO4为中强酸,H2CO3为弱酸的原因_________ 。
(4)2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代形成碳的一种新型三维立方晶体结构,如下图。已知T碳晶胞参数为a pm,阿伏伽德罗常数为NA,则T碳的密度的表达式为__________ g/cm3。(写出表达式即可)

(1)碳原子的价电子排布式
(2)碳可以形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。

①嘌呤中所有元素的电负性由大到小的顺序
②嘌呤中轨道之间的夹角∠1比∠2大,解释原因
③吡啶结构中N原子的杂化方式
④分子中的大π键可用符号
 表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为
表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为(3)碳元素能形成CO、CO2、H2CO3等多种无机化合物。
①二氧化碳的晶体叫做干冰,每个二氧化碳分子周围通常有
②在CO转化成CO2的反应过程中,下列说法正确的是
A.分子中孤电子对数不变 B.分子的极性发生变化
C.原子间成键方式发生改变 D.分子晶体的熔沸点升高
③H2CO3与H3PO4均有1个非羟基氧,H3PO4为中强酸,H2CO3为弱酸的原因
(4)2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代形成碳的一种新型三维立方晶体结构,如下图。已知T碳晶胞参数为a pm,阿伏伽德罗常数为NA,则T碳的密度的表达式为

您最近一年使用:0次
2018-04-14更新
|
365次组卷
|
2卷引用:辽宁省大连市2018年高三第一次模拟考试理科综合试卷化学试题
名校
解题方法
4 . 图1是元素周期表的一部分,已知A、B、C、D、E、F、G都是周期表中的前四周期元素,它们在周期表中的位置如图1所示。
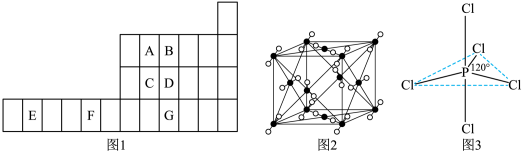
试回答下列问题:
(1)F元素基态原子的核外电子排布式为_________________ 。
(2)ABC的第一电离能由大到小的顺序______________ (用元素符号表示)。
(3)B元素单质分子中的_______ 个π键,与其互为等电子体的阴离子为____________________ 。
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用________ 杂化,每个分子周围有_____ 个分子与之距离相等且最近。若晶胞棱长为a pm,则该晶体密度的表达式为________ g·cm-3。
(5)G元素的氢化物分子的空间构型为________ ,其沸点与B元素的氢化物相比________ (填高或低),其原因是________ 。
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式________ 。
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同__________ ?(填“相同”或“不同”)。

试回答下列问题:
(1)F元素基态原子的核外电子排布式为
(2)ABC的第一电离能由大到小的顺序
(3)B元素单质分子中的
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用
(5)G元素的氢化物分子的空间构型为
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同
您最近一年使用:0次
解题方法
5 . 天宫二号空间实验室于2016年9月15 日在酒泉卫星发射中心发射成功。实验室承载了10余项太空实验,其中包含了好比科幻英雄“综合材料”多晶碲化锌(ZnTe)的实验。
(1)电负性Zn___________ Te(填“>”或“<”或“=”)。
(2)O、S、Se与Te元素位于同一主族。基态碲(Te)原子核外电子排布式为[Kr]________ ,有_______ 个未成对电子。
(3)H2O、H2S、H2Se沸点由低到高顺序为______ ,推断的依据是_______ ;SO2分子中S原子采取_____ 杂化;用价层电子对互斥理论解释SO42-的键角大于SO32-的原因是____________ 。
(4)向氯化锌溶液中加入过量的氨水,得到[Zn(NH3)4]Cl2,此配位化合物中含有的化学键有共价键、____ 、_______ 。
(5)碲化锌晶体有两种结构,其中一种晶胞结构如下图:
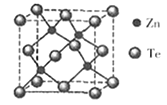
晶胞中含有_____ 个Te原子;与Te原子距离最近的Te原子有______ 个;若两个距离最近的Te原子间距为apm.则晶体密度为_________ g/cm3。
(1)电负性Zn
(2)O、S、Se与Te元素位于同一主族。基态碲(Te)原子核外电子排布式为[Kr]
(3)H2O、H2S、H2Se沸点由低到高顺序为
(4)向氯化锌溶液中加入过量的氨水,得到[Zn(NH3)4]Cl2,此配位化合物中含有的化学键有共价键、
(5)碲化锌晶体有两种结构,其中一种晶胞结构如下图:

晶胞中含有
您最近一年使用:0次
名校
6 . 晶体硅是制备太阳能电池板的主要原料,电池板中还含有硼、氮、钛、钻、钙等多种化学物质。
请回答下列问题:
1.第二周期元素的电负性按由小到大的顺序排列,B元素排在第__________ 位。
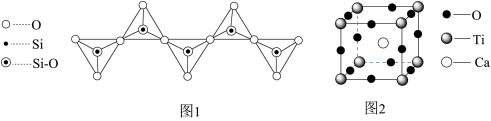
2.硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为____________ ,Si原子的杂化类型为__________________ 。
3.N元素位于元素周期表_____________ 区;基态N原子中,核外电子占据最高能级的电子云有____ 个伸展方向。
4. [Co(NH3)6]3+的几何构型为正八面体形,Co在中心。
①[Co(NH3)6]3+中,1个Co提供_______________ 个空轨道。
②若将[Co(NH3)6]3+中的两个NH3分子换成两个Cl-,可以形成_________ 种不同的结构形式。
5.—种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。
①与Ti紧邻的Ca有___________________ 个。
②若Ca与O之间的最短距离为α pm,阿伏伽德罗常数的值为NA,则晶体的密度ρ=__________________ g· cm-3(用含α、NA的代数式表示)。
请回答下列问题:
1.第二周期元素的电负性按由小到大的顺序排列,B元素排在第
2.硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为
3.N元素位于元素周期表
4. [Co(NH3)6]3+的几何构型为正八面体形,Co在中心。
①[Co(NH3)6]3+中,1个Co提供
②若将[Co(NH3)6]3+中的两个NH3分子换成两个Cl-,可以形成
5.—种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。
①与Ti紧邻的Ca有
②若Ca与O之间的最短距离为α pm,阿伏伽德罗常数的值为NA,则晶体的密度ρ=
您最近一年使用:0次
2018-01-08更新
|
379次组卷
|
2卷引用:黑龙江省牡丹江市第一高级中学2018届高三上学期期末考试化学试题
名校
解题方法
7 . 碳、 氮、磷、砷和硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。锂、钠、铝、铁等金属在日常生活、工业生产中也占有举足轻重的地位,请回答下列问题:
(1)基态As原子的电子排布式为[Ar]______________________ ;
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是___________________ (填角度)。
(3)砷化硼(BAs)是ⅢA一VA族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与____________ 个B相连,As的杂化形式为_______________ ;
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有____________ (填字母)。
A.离子键 B.金属键 C.极性键 D.氢键 E.配位键 F.σ键 G.π键
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于________________________________ (填晶体类型)。
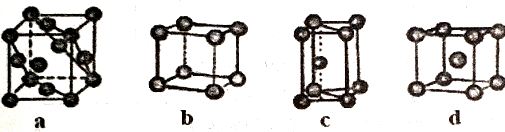
(5)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为___________ (填字母)。
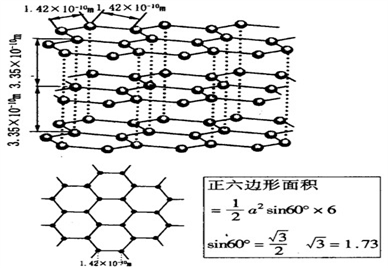
(6)石墨晶体的结构如下图,石墨的密度为________________________________ (只列式不化简不计算)
(1)基态As原子的电子排布式为[Ar]
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是
(3)砷化硼(BAs)是ⅢA一VA族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有
A.离子键 B.金属键 C.极性键 D.氢键 E.配位键 F.σ键 G.π键
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于
(5)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为

(6)石墨晶体的结构如下图,石墨的密度为

您最近一年使用:0次
解题方法
8 . (1) 写出镍原子的电子排布式_____________ 。
(2) 丙酮(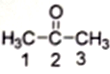 )分子中2号碳原子的杂化方式为
)分子中2号碳原子的杂化方式为__________ ;与CS2互为等电子体的阴离子是__________ (写一种)。
(3)含0.1mol[Cr(H2O)Cl]Cl2·H2O的水溶液与足量硝酸银溶液反应生成_______ molAgCl沉淀。H2O分子的键角比H2S分子的键角大,原因是_______ 。
(4) 由铜与氯形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。
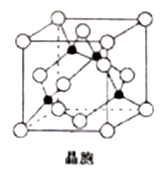
①该晶体的化学式为_______ 。
②将晶胞内的4个黑点相互连接所形成的立体构型是_______ 。
③晶体中与一个氯原子距离最近的氯原子有_______ 个。
④已知该晶体的密度为ρg.cm-3,阿伏伽德罗常数的值为NA,则该晶体中铜原子和氯原子之间的最短距离为_______ pm(列出计算式即可)。
(2) 丙酮(
 )分子中2号碳原子的杂化方式为
)分子中2号碳原子的杂化方式为(3)含0.1mol[Cr(H2O)Cl]Cl2·H2O的水溶液与足量硝酸银溶液反应生成
(4) 由铜与氯形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。

①该晶体的化学式为
②将晶胞内的4个黑点相互连接所形成的立体构型是
③晶体中与一个氯原子距离最近的氯原子有
④已知该晶体的密度为ρg.cm-3,阿伏伽德罗常数的值为NA,则该晶体中铜原子和氯原子之间的最短距离为
您最近一年使用:0次



