名校
1 . 科学家利用四种原子序数依次增大的短周期主族元素X、Y、Z、W组合成一种超分子,具有高效的催化性能,其分子结构示意图如图(注:实线代表共价键,其他重复单元的W、X未标注)。X、Z分别位于不同周期, 的第一电离能在同周期元素中最小。下列说法中不正确的是
的第一电离能在同周期元素中最小。下列说法中不正确的是
 的第一电离能在同周期元素中最小。下列说法中不正确的是
的第一电离能在同周期元素中最小。下列说法中不正确的是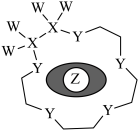
A.电负性: |
B.简单离子半径: |
| C.Z与Y组成的化合物可能含有共价键 |
| D.该化合物中X、Y、W均满足8电子稳定结构 |
您最近一年使用:0次
名校
解题方法
2 . 下列有关说法表达正确的是
A.基态Cu原子的价层电子排布式: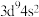 |
| B.基态Si原子中,有两个未成对电子 |
C.第二周期元素中,电负性: |
D. 与 与 均为直线型分子 均为直线型分子 |
您最近一年使用:0次
3 . 氟磷灰石的主要成分是 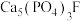 ,下列说法不正确的是
,下列说法不正确的是
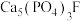 ,下列说法不正确的是
,下列说法不正确的是A.原子半径: | B.电负性: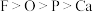 |
C.未成对电子数: 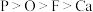 | D.最高正化合价: 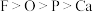 |
您最近一年使用:0次
名校
解题方法
4 . 下列解释错误的是
事实 | 解释 | |
A | 三氟乙酸的酸性强于三氯乙酸 | F的电负性大于Cl的电负性 |
B | 冰晶体中水分子周围的紧邻分子数为4, 周围的紧邻分子数为12 周围的紧邻分子数为12 | 水分子之间存在氢键,且氢键具有方向性 |
C |  的熔、沸点高于 的熔、沸点高于 的 的 | O-H的键能大于S-H的键能 |
D | N的第一电离能高于O的 | N的2p轨道半充满,结构更稳定,能量更低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-25更新
|
209次组卷
|
2卷引用:重庆市西北狼教育联盟2023-2024学年高二下学期4月期中联合测试化学试卷
解题方法
5 . 前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子中成对电子数是未成对电子数的3倍;E为第四周期元素且价层电子均为半充满状态,D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)E在元素周期表中的位置为___________ 。
(2)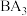 极易溶于水的主要原因是
极易溶于水的主要原因是___________ ;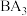 分子中键角
分子中键角___________ 109°28'(填“>”“<”或“=”)。
(3)元素A、B、C中,电负性最大的是___________ (填元素符号,下同),元素B、C、D第一电离能由大到小的顺序为___________ 。
(4) 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为___________ , 的空间构型
的空间构型___________ 。
(1)E在元素周期表中的位置为
(2)
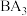 极易溶于水的主要原因是
极易溶于水的主要原因是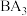 分子中键角
分子中键角(3)元素A、B、C中,电负性最大的是
(4)
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 的空间构型
的空间构型
您最近一年使用:0次
2023-06-16更新
|
87次组卷
|
2卷引用:重庆市渝东九校2022-2023学年高二下学期期中诊断测试化学试题
名校
6 . 三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。回答下列问题:
(1)基态 原子价电子排布图为
原子价电子排布图为__________ 、属于______ 区。
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠: ,其阴离子的空间结构是
,其阴离子的空间结构是______ 。
(3)利用离子液体 可电沉积还原金属
可电沉积还原金属 ,其熔点只有7℃,其中
,其熔点只有7℃,其中 结构如图所示。
结构如图所示。

①该物质的晶体类型是__________ 。
② 离子中组成元素的电负性由小到大的顺序是
离子中组成元素的电负性由小到大的顺序是__________ 。
(4)独立的 分子中H—N—H的键角为
分子中H—N—H的键角为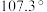 ,
, 离子中H—N—H的键角
离子中H—N—H的键角__________ 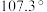 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(5)硒化锌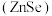 是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为
是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为 ,该晶胞中两个
,该晶胞中两个 原子之间的间距是
原子之间的间距是__________ pm;乙图为甲图的俯视图,A点坐标为 ,B点坐标为
,B点坐标为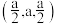 ,则D点坐标为
,则D点坐标为__________ ;若该晶胞密度为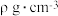 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为__________ (只列出计算式)。

(1)基态
 原子价电子排布图为
原子价电子排布图为(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:
 ,其阴离子的空间结构是
,其阴离子的空间结构是(3)利用离子液体
 可电沉积还原金属
可电沉积还原金属 ,其熔点只有7℃,其中
,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
①该物质的晶体类型是
②
 离子中组成元素的电负性由小到大的顺序是
离子中组成元素的电负性由小到大的顺序是(4)独立的
 分子中H—N—H的键角为
分子中H—N—H的键角为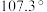 ,
, 离子中H—N—H的键角
离子中H—N—H的键角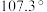 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(5)硒化锌
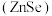 是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为
是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为 ,该晶胞中两个
,该晶胞中两个 原子之间的间距是
原子之间的间距是 ,B点坐标为
,B点坐标为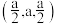 ,则D点坐标为
,则D点坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
您最近一年使用:0次
名校
7 . 部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是


| A.离子半径的大小顺序:e>f>g>h |
| B.y、z、d三种元素电负性的大小为:z>d>y |
| C.与x形成化合物的稳定性:d>z>y |
| D.e、f、g、h四种元素对应最高价氧化物的水化物相互之间均能发生反应 |
您最近一年使用:0次
8 . 下列结论与解释不匹配的是
| 选项 | 结论 | 解释 |
| A | CH4的稳定性强于SiH4的 | C-H键键长比Si-H键的短,C-H键键能更大 |
| B | 冰中1个水分子周围只有4个紧邻分子 | 水分子之间存在氢键,氢键具有方向性 |
| C | 氟乙酸的酸性强于氯乙酸的 | 氟的电负性大于氯的电负性 |
| D | CH3CH2OH的沸点比CH3OCH3的沸点高 | CH3CH2OH是极性分子,CH3OCH3是非极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-30更新
|
351次组卷
|
4卷引用:重庆市2022-2023学年高二下学期期中考试化学试题
重庆市2022-2023学年高二下学期期中考试化学试题四川省成都外国语学校2023-2024学年高二下学期3月月考化学试卷(已下线)2023年北京卷高考真题变式题(选择题6-10)北京市丰台区第二中学2024届高三下学期三模化学试题
名校
解题方法
9 . 物质甲可作催化剂和阻燃剂,其结构如图所示,W、X、Y、Z为原子序数依次增大的短周期主族元素,基态X原子的s电子比p电子多3,Z是周期表中电负性最大的元素,W与Y可以形成一种极易溶于水的气体。下列说法正确的是
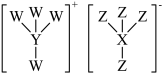
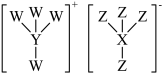
A.电负性: |
| B.物质甲含有离子键、极性共价键和非极性共价键 |
C.第一电离能: |
D.最简单氢化物的稳定性: |
您最近一年使用:0次
2023-04-30更新
|
247次组卷
|
3卷引用:重庆市2022-2023学年高二下学期期中考试化学试题
名校
解题方法
10 . 有关周期表和周期律的说法正确的是
| A.第二周期元素,电离能介于B和N之间的元素有1种 |
| B.钙元素电负性大于镓元素 |
| C.周期表p区所有元素,电子最后填入的能级均为p能级 |
| D.周期表第14列元素形成化合物种类最多 |
您最近一年使用:0次



