名校
1 . 固体电解质以其在电池、传感器等装置中的广泛应用而备受关注,大致分为无机物类及高分子类。
(1)固体电解质中研究得最多的是 和O等的导体。
和O等的导体。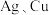 在元素周期表中位于同一族且
在元素周期表中位于同一族且 在
在 的下一周期,具有类似的价层电子排布式,
的下一周期,具有类似的价层电子排布式, 的价层电子排布式为
的价层电子排布式为___________ 。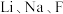 和O的电负性从小到大的顺序为
和O的电负性从小到大的顺序为___________ 。F的第二电离能___________ O的第二电离能(填“>”或“=”或“<”)。
(2) 中阴离子的空间构型为
中阴离子的空间构型为___________ 。
(3)1979年,法国Armand等报道了聚氧化乙烯( )碱金属盐络合物可用作锂离子电池固体聚合物电解质。聚氧化乙烯中O的
)碱金属盐络合物可用作锂离子电池固体聚合物电解质。聚氧化乙烯中O的___________ 杂化轨道与C的 杂化轨道成键;因氢键的形成,聚氧化乙烯是一种水溶性聚合物,若水分子之间形成的氢键可以表示为
杂化轨道成键;因氢键的形成,聚氧化乙烯是一种水溶性聚合物,若水分子之间形成的氢键可以表示为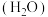
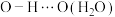 ,请写出使聚氧化乙烯具有水溶性的氢键的表示式
,请写出使聚氧化乙烯具有水溶性的氢键的表示式___________ 。
(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如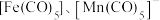 等都满足这个规则。钒配合物
等都满足这个规则。钒配合物 的熔点为
的熔点为 ,其晶体类型为:
,其晶体类型为:___________ ;已知该化合物满足18电子规则,其配体“ ”中的大
”中的大 键可表示为
键可表示为___________ 。(已知苯中的大 键表示为:
键表示为: )
)
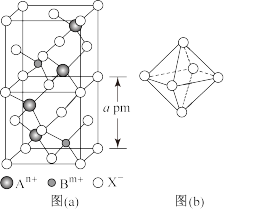
(5)图(a)为一种由阳离子 和阴离子
和阴离子 组成的无机固体电解质的晶胞结构。用A、B、X表示出这种电解质的化学式为
组成的无机固体电解质的晶胞结构。用A、B、X表示出这种电解质的化学式为___________ ,
___________ 。 堆积形成了正八面体和正四面体两种空隙,阳离子占据的空隙类型为
堆积形成了正八面体和正四面体两种空隙,阳离子占据的空隙类型为___________ ,占有率为___________ 。图(b)为 堆积形成的正八面体,其边长为
堆积形成的正八面体,其边长为___________  。(用含a的式子表示)
。(用含a的式子表示)
(1)固体电解质中研究得最多的是
 和O等的导体。
和O等的导体。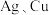 在元素周期表中位于同一族且
在元素周期表中位于同一族且 在
在 的下一周期,具有类似的价层电子排布式,
的下一周期,具有类似的价层电子排布式, 的价层电子排布式为
的价层电子排布式为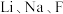 和O的电负性从小到大的顺序为
和O的电负性从小到大的顺序为(2)
 中阴离子的空间构型为
中阴离子的空间构型为(3)1979年,法国Armand等报道了聚氧化乙烯(
 )碱金属盐络合物可用作锂离子电池固体聚合物电解质。聚氧化乙烯中O的
)碱金属盐络合物可用作锂离子电池固体聚合物电解质。聚氧化乙烯中O的 杂化轨道成键;因氢键的形成,聚氧化乙烯是一种水溶性聚合物,若水分子之间形成的氢键可以表示为
杂化轨道成键;因氢键的形成,聚氧化乙烯是一种水溶性聚合物,若水分子之间形成的氢键可以表示为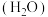
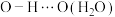 ,请写出使聚氧化乙烯具有水溶性的氢键的表示式
,请写出使聚氧化乙烯具有水溶性的氢键的表示式(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如
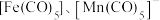 等都满足这个规则。钒配合物
等都满足这个规则。钒配合物 的熔点为
的熔点为 ,其晶体类型为:
,其晶体类型为: ”中的大
”中的大 键可表示为
键可表示为 键表示为:
键表示为: )
)(5)图(a)为一种由阳离子
 和阴离子
和阴离子 组成的无机固体电解质的晶胞结构。用A、B、X表示出这种电解质的化学式为
组成的无机固体电解质的晶胞结构。用A、B、X表示出这种电解质的化学式为
 堆积形成了正八面体和正四面体两种空隙,阳离子占据的空隙类型为
堆积形成了正八面体和正四面体两种空隙,阳离子占据的空隙类型为 堆积形成的正八面体,其边长为
堆积形成的正八面体,其边长为 。(用含a的式子表示)
。(用含a的式子表示)
您最近一年使用:0次
解题方法
2 . 铁及其化合物在生活、生产中有重要应用。回答下列问题:
(1)乳酸亚铁[CH3CH(OH)COO]2Fe是一种常用的补铁剂。
①Fe2+的价层电子排布式是___________ 。
②乳酸分子(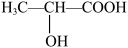 )中 σ 键与π键的数目比为
)中 σ 键与π键的数目比为___________ 。
③乳酸亚铁中各元素的电负性由大到小的顺序为___________ 。
(2)无水FeCl2可与NH3形成[Fe(NH3)6]Cl2。
①[Fe(NH3)6]Cl2中Fe2+的配位数为___________ 。
②NH3的空间构型是___________ ,其中N原子的杂化方式是___________ 。
(3)由铁、钾、硒形成的一种超导材料,其晶胞结构如图1所示。
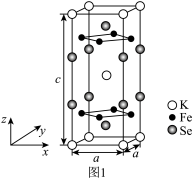
①该超导材料的化学式是___________ 。
②该晶胞参数a=0.4 nm、c=1.4 nm,该晶体密度ρ=___________ g·cm-3。(用 NA表示阿伏加德罗常数,写出计算表达式即可)
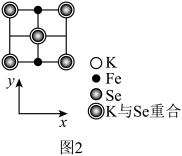
③该晶胞在xy平面投影如图2所示,将图2补充完整___________ 。
(1)乳酸亚铁[CH3CH(OH)COO]2Fe是一种常用的补铁剂。
①Fe2+的价层电子排布式是
②乳酸分子(
 )中 σ 键与π键的数目比为
)中 σ 键与π键的数目比为③乳酸亚铁中各元素的电负性由大到小的顺序为
(2)无水FeCl2可与NH3形成[Fe(NH3)6]Cl2。
①[Fe(NH3)6]Cl2中Fe2+的配位数为
②NH3的空间构型是
(3)由铁、钾、硒形成的一种超导材料,其晶胞结构如图1所示。

①该超导材料的化学式是
②该晶胞参数a=0.4 nm、c=1.4 nm,该晶体密度ρ=
③该晶胞在xy平面投影如图2所示,将图2补充完整

您最近一年使用:0次
3 . 碳酸丙烯酯是一种水溶性颜料的分散剂,工业上常用 作催化剂用1,2-丙二醇和尿素合成,原理如下:
作催化剂用1,2-丙二醇和尿素合成,原理如下:

回答下列问题:
(1)基态Zn原子的价电子排布式为___________ ,其位于元素周期表的___________ (填“d”或“ds”)区。
(2)尿素分子中,各元素电负性大小顺序为___________ ,第三电离能
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)碳酸丙烯酸酯中C原子的杂化方式为___________ ;其常温下呈液态,易溶于水,也易溶于乙醚、苯等有机溶剂,则碳酸丙烯酸酯的晶体类型为___________ 。
(4) 能与
能与 形成稳定的配离子
形成稳定的配离子 ,其中配体的立体结构为
,其中配体的立体结构为___________ ,配离子中 的键角比
的键角比 的键角大,试从物质结构的角度解释其原因
的键角大,试从物质结构的角度解释其原因___________ 。
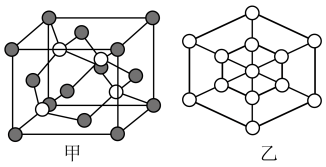
(5) 有多种晶体结构,其中一种六方晶胞的结构如图所示,则锌的配位数为
有多种晶体结构,其中一种六方晶胞的结构如图所示,则锌的配位数为___________ ;该晶体的密度为___________  (写出计算式,阿伏加德罗常数的值为
(写出计算式,阿伏加德罗常数的值为 )。
)。

 作催化剂用1,2-丙二醇和尿素合成,原理如下:
作催化剂用1,2-丙二醇和尿素合成,原理如下:
回答下列问题:
(1)基态Zn原子的价电子排布式为
(2)尿素分子中,各元素电负性大小顺序为

 (填“>”或“<”)。
(填“>”或“<”)。(3)碳酸丙烯酸酯中C原子的杂化方式为
(4)
 能与
能与 形成稳定的配离子
形成稳定的配离子 ,其中配体的立体结构为
,其中配体的立体结构为 的键角比
的键角比 的键角大,试从物质结构的角度解释其原因
的键角大,试从物质结构的角度解释其原因(5)
 有多种晶体结构,其中一种六方晶胞的结构如图所示,则锌的配位数为
有多种晶体结构,其中一种六方晶胞的结构如图所示,则锌的配位数为 (写出计算式,阿伏加德罗常数的值为
(写出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解题方法
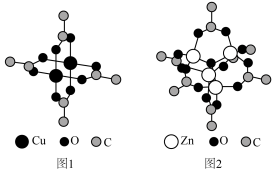
4 . 铜配合物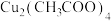 (见图1,未表示出氢原子)和锌配合物
(见图1,未表示出氢原子)和锌配合物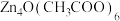 (见图2,未表示出氢原子)可分别形成笼状配合物和多孔配位聚合物。回答下列问题:
(见图2,未表示出氢原子)可分别形成笼状配合物和多孔配位聚合物。回答下列问题:
(1)基态 的未成对电子数为
的未成对电子数为___________ ; 第二电离能较大者是
第二电离能较大者是___________ 。
(2) 中C原子的轨道杂化类型为
中C原子的轨道杂化类型为___________ ,所含元素电负性由小到大的顺序为___________ 。
(3)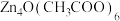 中锌离子的配位数为
中锌离子的配位数为___________ ;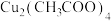 熔点为
熔点为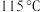 ,属于
,属于___________ (填“离子”、“共价”或“分子”)晶体。
(4)用对苯二甲酸根替换 后,
后,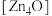 团簇被对苯二甲酸根相互连接形成的晶体Z立方晶胞的1/8如图。已知该晶体密度为
团簇被对苯二甲酸根相互连接形成的晶体Z立方晶胞的1/8如图。已知该晶体密度为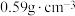 ,假设其摩尔质量为
,假设其摩尔质量为 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
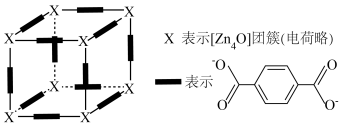
①对苯二甲酸根的___________ 原子提供孤对电子与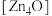 团簇形成配位键。
团簇形成配位键。
②晶体Z的化学式为___________ 。
③立方晶胞参数为___________  (列出计算式)。
(列出计算式)。
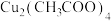 (见图1,未表示出氢原子)和锌配合物
(见图1,未表示出氢原子)和锌配合物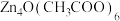 (见图2,未表示出氢原子)可分别形成笼状配合物和多孔配位聚合物。回答下列问题:
(见图2,未表示出氢原子)可分别形成笼状配合物和多孔配位聚合物。回答下列问题:
(1)基态
 的未成对电子数为
的未成对电子数为 第二电离能较大者是
第二电离能较大者是(2)
 中C原子的轨道杂化类型为
中C原子的轨道杂化类型为(3)
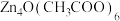 中锌离子的配位数为
中锌离子的配位数为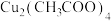 熔点为
熔点为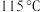 ,属于
,属于(4)用对苯二甲酸根替换
 后,
后,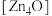 团簇被对苯二甲酸根相互连接形成的晶体Z立方晶胞的1/8如图。已知该晶体密度为
团簇被对苯二甲酸根相互连接形成的晶体Z立方晶胞的1/8如图。已知该晶体密度为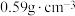 ,假设其摩尔质量为
,假设其摩尔质量为 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
①对苯二甲酸根的
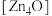 团簇形成配位键。
团簇形成配位键。②晶体Z的化学式为
③立方晶胞参数为
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2024-01-06更新
|
336次组卷
|
2卷引用:2024届四川省成都市高三第一次诊断性检测理科综合试题
名校
解题方法
5 . 二茂铁( )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
(1)Fe在周期表中的___________ 区,若受热后Fe的1个4s电子会跃迁至4p轨道,写出Fe的该激发态简化电子排布式:___________ 。
(2)羰基铁粉[ ]中铁元素的配位数是
]中铁元素的配位数是___________ ,配位原子为___________ 。
(3)二茂铁的衍生物可和 等微粒产生静电作用,H、B、O和C的电负性由大到小的顺序为;
等微粒产生静电作用,H、B、O和C的电负性由大到小的顺序为;___________ ; 空间构型为
空间构型为_________ 。 的键角比
的键角比 的
的_______ (填“大”或“小”)
(4)T-碳是碳的一种同素异形体,其晶体结构可以看成是金刚石晶体(如图甲)中每个碳原子被一个由四个碳原子组成的正四面体结构单元( )所取代(如图乙)。
)所取代(如图乙)。

一个T-碳晶胞中含有___________ 个碳原子,已知T-碳的密度约为金刚石的一半。则T-碳晶胞的边长和金刚石晶胞的边长之比为___________ 。
 )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。(1)Fe在周期表中的
(2)羰基铁粉[
 ]中铁元素的配位数是
]中铁元素的配位数是(3)二茂铁的衍生物可和
 等微粒产生静电作用,H、B、O和C的电负性由大到小的顺序为;
等微粒产生静电作用,H、B、O和C的电负性由大到小的顺序为; 空间构型为
空间构型为 的键角比
的键角比 的
的(4)T-碳是碳的一种同素异形体,其晶体结构可以看成是金刚石晶体(如图甲)中每个碳原子被一个由四个碳原子组成的正四面体结构单元(
 )所取代(如图乙)。
)所取代(如图乙)。
一个T-碳晶胞中含有
您最近一年使用:0次
6 . 决定物质性质的根本因素是物质结构。请回答下列问题:
(1)物质 中非金属元素的电负性由小到大的顺序为
中非金属元素的电负性由小到大的顺序为______ 。
(2)Ca元素基态原子的价电子排布式为______ ;Ca元素的气态原子逐个依次失去第1至第5个电子所需能量(电离能)用I1至I5表示,其中所需能量差值最大的是______ (填字母)。
A、 B、
B、 C、
C、 D、
D、
(3)物质Na3AsO3中As原子的杂化方式为______ ;AsCl3的空间构型为______ 。
(4)已知:GaAs和GaN的晶胞结构均与金刚石的相似,GaAs熔点为1238℃,GaN熔点约为l500℃,则GaAs熔点低于GaN的原因为______ 。
(5)与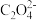 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为______ (写一种)。
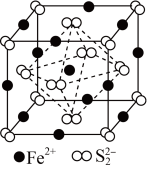
(6)FeS2晶体的晶胞如图所示。晶胞边长为anm,FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______ 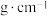 ;晶胞中Fe2+位于S2-所形成的正八面体的体心,该正八面体的边长为
;晶胞中Fe2+位于S2-所形成的正八面体的体心,该正八面体的边长为______ nm。
(1)物质
 中非金属元素的电负性由小到大的顺序为
中非金属元素的电负性由小到大的顺序为(2)Ca元素基态原子的价电子排布式为
A、
 B、
B、 C、
C、 D、
D、
(3)物质Na3AsO3中As原子的杂化方式为
(4)已知:GaAs和GaN的晶胞结构均与金刚石的相似,GaAs熔点为1238℃,GaN熔点约为l500℃,则GaAs熔点低于GaN的原因为
(5)与
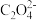 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为(6)FeS2晶体的晶胞如图所示。晶胞边长为anm,FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为
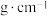 ;晶胞中Fe2+位于S2-所形成的正八面体的体心,该正八面体的边长为
;晶胞中Fe2+位于S2-所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
名校
解题方法
7 . 硼和镓及其化合物在合金工业、制药工业、电池工业有广泛的应用。用于制氢的氨硼烷是非常有应用潜力的车载储氢材料之一,氨硼烷水解释放氢气,在催化剂存在条件下进行,该反应是氢元素间的归中反应,其反应方程式为:NH3BH3+2H2O= +
+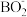 +3H2↑。回答下列问题:
+3H2↑。回答下列问题:
(1)基态B原子的最高能级电子排布式为___________ 。
(2)NH3BH3中所含元素电负性由大到小的顺序为___________ ,氨硼烷比其等电子体乙烷熔点高,原因是___________ 。
(3)反应方程式中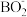 是
是 的简写形式,
的简写形式, 中含有一个六元环状结构,且只有氧原子最外层达到8e-稳定结构,写出
中含有一个六元环状结构,且只有氧原子最外层达到8e-稳定结构,写出 的结构式:
的结构式:___________ 。
(4)一种含镓的药物合成方法如图所示:

①化合物Ⅰ中环上N原子的杂化方式为___________ ,1mol化合物Ⅰ中含有的C-H和C-Cσ键的数目共为___________ NA。
②化合物Ⅱ中Ga的配位数为___________ ,x=___________ 。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如图甲所示,已知该晶体的密度为ρg/cm3),设NA是阿伏加德罗常数的值,若P原子半径为apm,晶胞中B、P原子相切,则B原子半径为___________ pm(写计算表达式);磷化硼晶胞沿着体对角线方向的投影(图乙中○表示P原子的投影),在图乙中用●画出B原子的投影位置___________ 。
 +
+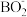 +3H2↑。回答下列问题:
+3H2↑。回答下列问题:(1)基态B原子的最高能级电子排布式为
(2)NH3BH3中所含元素电负性由大到小的顺序为
(3)反应方程式中
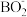 是
是 的简写形式,
的简写形式, 中含有一个六元环状结构,且只有氧原子最外层达到8e-稳定结构,写出
中含有一个六元环状结构,且只有氧原子最外层达到8e-稳定结构,写出 的结构式:
的结构式:(4)一种含镓的药物合成方法如图所示:

①化合物Ⅰ中环上N原子的杂化方式为
②化合物Ⅱ中Ga的配位数为
(5)磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如图甲所示,已知该晶体的密度为ρg/cm3),设NA是阿伏加德罗常数的值,若P原子半径为apm,晶胞中B、P原子相切,则B原子半径为

您最近一年使用:0次
解题方法
8 . CO2固定是实现碳达峰、碳中和的有效途径。使用不同催化剂,CO2固定的产物也不同。在戊二酸锌催化下,CO2固定方式主要有:

研究发现,利用氧化锌和戊二酸制备的戊二酸锌的催化效能良好。回答下列问题:
(1)一个基态氧原子的价层电子轨道表示式为_______ ;基态碳原子核外有_______ 个未成对电子。
(2)1mol丁含_______ molσ键,1个丁分子含_______ 个手性碳原子。
(3)乙中所含元素电负性由大到小的顺序为_______ (填元素符号),乙中碳原子的杂化类型是_______ 。
(4)戊二酸、丙二酸二甲酯的沸点分别为303℃、181℃,它们沸点差别较大的原因是_______ 。
(5)配离子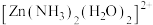 的空间结构只有1种,由此推知
的空间结构只有1种,由此推知 的空间结构是
的空间结构是_______ 。
(6)ZnO晶胞结构如图所示。已知:ZnO晶体的密度为ρg∙cm-3,NA代表阿伏加德罗常数的值。氧离子的配位数为_______ 。氧和锌的最近距离为_______ nm。


研究发现,利用氧化锌和戊二酸制备的戊二酸锌的催化效能良好。回答下列问题:
(1)一个基态氧原子的价层电子轨道表示式为
(2)1mol丁含
(3)乙中所含元素电负性由大到小的顺序为
(4)戊二酸、丙二酸二甲酯的沸点分别为303℃、181℃,它们沸点差别较大的原因是
(5)配离子
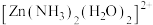 的空间结构只有1种,由此推知
的空间结构只有1种,由此推知 的空间结构是
的空间结构是(6)ZnO晶胞结构如图所示。已知:ZnO晶体的密度为ρg∙cm-3,NA代表阿伏加德罗常数的值。氧离子的配位数为

您最近一年使用:0次
名校
解题方法
9 . 二茂铁(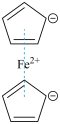 )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
(1)Fe在周期表中的___________ 区,Fe变为Fe2+时是失去___________ 轨道电子;若受热后Fe的1个4s电子会跃迁至4p轨道,写出Fe的该激发态电子排布式:[Ar]___________ 。
(2)羰基铁粉【Fe(CO)5】中铁元素的配位数是___________ ,配位原子为___________ 。
(3)二茂铁的衍生物可和H3O+等微粒产生静电作用,H、O和C的电负性由大到小的顺序为___________ ;H3O+中氧原子的杂化方式为___________ ,H3O+空间构型为___________ 。
(4)T-碳是碳的一种同素异形体,其晶体结构可以看成是金刚石晶体(如图甲)中每 个碳原子被一个由四个碳原子组成的正四面体结构单元( )所取代(如图乙)。
)所取代(如图乙)。

一个T-碳晶胞中含有___________ 个碳原子,已知T-碳的密度约为金刚石的一半。则T-碳晶胞的边长和金刚石晶胞的边长之比为___________ 。
 )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。(1)Fe在周期表中的
(2)羰基铁粉【Fe(CO)5】中铁元素的配位数是
(3)二茂铁的衍生物可和H3O+等微粒产生静电作用,H、O和C的电负性由大到小的顺序为
(4)T-碳是碳的一种同素异形体,其晶体结构可以看成是金刚石晶体(如图甲)中每 个碳原子被一个由四个碳原子组成的正四面体结构单元(
 )所取代(如图乙)。
)所取代(如图乙)。
一个T-碳晶胞中含有
您最近一年使用:0次
名校
解题方法
10 . 元素周期表中第四周期过渡元素在工业及生活方面有重要应用。请回答下列问题:
(1)“钛”被称为21世纪金属,画出基态钛的价电子的电子排布图___________ 。
(2)CrO5中Cr为+6价,则-1价的O与-2价的O的个数比为_________ 。
(3)[Co(NH3)4Cl2]+中中心离子的配位数_________ 。能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是_________ (填标号)。
A.浓氨水 B.NaOH溶液 C.稀H2SO4 D.AgNO3溶液
(4)K3[Fe(CN)6]是鉴别Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是_________ (填元素符号),下列碳的杂化为sp的是_________ (填标号)。
A.CH2Cl2 B.C2H2 C.溴苯 D.HCN
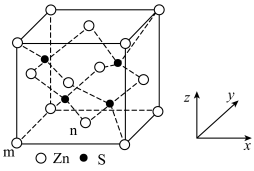
(5)ZnS的晶胞如图所示,若m点坐标为(0,0,0),n点坐标为( ,
, ,0)此晶胞中与n点最远的S的坐标为
,0)此晶胞中与n点最远的S的坐标为___________ 。若晶胞参数为apm,则ZnS的密度为___________ g·cm-3(设NA为阿伏加德罗常数的值)。
(1)“钛”被称为21世纪金属,画出基态钛的价电子的电子排布图
(2)CrO5中Cr为+6价,则-1价的O与-2价的O的个数比为
(3)[Co(NH3)4Cl2]+中中心离子的配位数
A.浓氨水 B.NaOH溶液 C.稀H2SO4 D.AgNO3溶液
(4)K3[Fe(CN)6]是鉴别Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是
A.CH2Cl2 B.C2H2 C.溴苯 D.HCN
(5)ZnS的晶胞如图所示,若m点坐标为(0,0,0),n点坐标为(
 ,
, ,0)此晶胞中与n点最远的S的坐标为
,0)此晶胞中与n点最远的S的坐标为
您最近一年使用:0次



