1 . 铬是一种重要的元素,在合金、电镀、鞣制领域都有重要的应用, 的配位能力很强,可以形成多种配离子。
的配位能力很强,可以形成多种配离子。
(1)基态Cr原子价层电子的轨道表达式为__________ ,同周期元素的基态原子最外层电子数与Cr相同的元素有__________ 种。
(2) 是最重要的铬(Ⅲ)盐之一,阴离子
是最重要的铬(Ⅲ)盐之一,阴离子 的空间构型为
的空间构型为__________ ,基态S原子核外电子中成对电子数和未成对电子数之比为__________ 。
(3)NH3、H2O、 都是常见的配体,以上配体中所含元素的电负性由大到小的顺序是
都是常见的配体,以上配体中所含元素的电负性由大到小的顺序是____________________ 。
(4) 中
中 键的数目为
键的数目为__________ ,基态N原子电子占据最高能级的电子云轮廓图为__________ 形。
(5)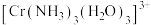 中配体
中配体 的杂化类型是
的杂化类型是__________ , 的键角
的键角__________  的键角(填“大于”、“小于”或“等于”),判断依据是
的键角(填“大于”、“小于”或“等于”),判断依据是______________________________ 。
 的配位能力很强,可以形成多种配离子。
的配位能力很强,可以形成多种配离子。(1)基态Cr原子价层电子的轨道表达式为
(2)
 是最重要的铬(Ⅲ)盐之一,阴离子
是最重要的铬(Ⅲ)盐之一,阴离子 的空间构型为
的空间构型为(3)NH3、H2O、
 都是常见的配体,以上配体中所含元素的电负性由大到小的顺序是
都是常见的配体,以上配体中所含元素的电负性由大到小的顺序是(4)
 中
中 键的数目为
键的数目为(5)
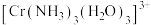 中配体
中配体 的杂化类型是
的杂化类型是 的键角
的键角 的键角(填“大于”、“小于”或“等于”),判断依据是
的键角(填“大于”、“小于”或“等于”),判断依据是
您最近一年使用:0次
2024-02-01更新
|
270次组卷
|
2卷引用:山东省德州市2023-2024学年高二上学期期末考试化学试题
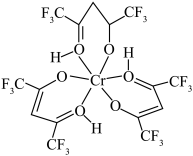
2 . 铬元素是哺乳类代谢过程中必须的微量元素,目前六氟代乙酰丙酮铬(Ⅲ)螯合物(其结构如图)的检出极限已达到 。回答下列问题:
。回答下列问题:
(1)基态铬原子的价电子排布式为___________ ,H、C、O、F的电负性由大到小的顺序为___________ 。
(2)与 具有相同未成对电子数的同周期基态原子的元素有
具有相同未成对电子数的同周期基态原子的元素有___________ 种,其中原子序数最大的元素在周期表中的位置是___________ 。
(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有___________ 。
a.极性共价键 b.非极性共价键 c.离子键 d.配位键
(4)六氟代乙酰丙酮(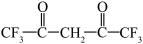 )中
)中 键有
键有___________ 个。
(5)分子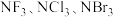 中键角由小到大的顺序是
中键角由小到大的顺序是___________ ,其原因是___________ 。
 。回答下列问题:
。回答下列问题:
(1)基态铬原子的价电子排布式为
(2)与
 具有相同未成对电子数的同周期基态原子的元素有
具有相同未成对电子数的同周期基态原子的元素有(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有
a.极性共价键 b.非极性共价键 c.离子键 d.配位键
(4)六氟代乙酰丙酮(
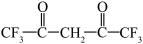 )中
)中 键有
键有(5)分子
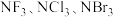 中键角由小到大的顺序是
中键角由小到大的顺序是
您最近一年使用:0次
解题方法
3 . 某笼形络合物 晶胞结构中,镍离子与
晶胞结构中,镍离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,所有N原子均参与形成配位键,苯分子填充于空隙正中心,其晶胞结构如图(H原子未画出)。回答下列问题:
分子连接,所有N原子均参与形成配位键,苯分子填充于空隙正中心,其晶胞结构如图(H原子未画出)。回答下列问题:

(1)C、N、H电负性大小顺序___________ ;晶胞中N原子的杂化方式为___________ 。
(2)晶胞中镍离子的价电子轨道表示式为___________ ,与镍同周期的元素中,基态原子的未成对电子数与镍相同的有___________ 种。
(3)已知苯环中 键长为npm,则晶胞中A号C原子的分数坐标
键长为npm,则晶胞中A号C原子的分数坐标___________ ;晶胞M中含有 键数目为
键数目为___________ 个。
(4)镍离子的配位数为___________ ,晶胞的密度为___________  (用代数式表示)。
(用代数式表示)。
 晶胞结构中,镍离子与
晶胞结构中,镍离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,所有N原子均参与形成配位键,苯分子填充于空隙正中心,其晶胞结构如图(H原子未画出)。回答下列问题:
分子连接,所有N原子均参与形成配位键,苯分子填充于空隙正中心,其晶胞结构如图(H原子未画出)。回答下列问题:
(1)C、N、H电负性大小顺序
(2)晶胞中镍离子的价电子轨道表示式为
(3)已知苯环中
 键长为npm,则晶胞中A号C原子的分数坐标
键长为npm,则晶胞中A号C原子的分数坐标 键数目为
键数目为(4)镍离子的配位数为
 (用代数式表示)。
(用代数式表示)。
您最近一年使用:0次
解题方法
4 . 材料是人类文明进步的阶梯,主族非金属元素是组成特殊材料的重要元素。请回答下列问题:
(1)氮氧共掺杂多孔碳材料是一种新型高效的能源存储材料,其中的三种主要元素C、N、O,电负性从小到大的顺序是_____ ,第一电离能从大到小的顺序是_____ 。
(2)根据杂化轨道理论的相关知识,在NH3、BF3、SO 、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是
、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是______ (填化学式);已知等电子体具有相同的空间构型,结合价电子对互斥理论可知N2O分子为______ 形。
(3)有一种配合物组成为[M(NH3)5(H2O)]Cl3,该配合物中提供孤电子对的原子是_____ (填符号);配合物T与[M(NH3)5(H2O)]Cl3组成所含微粒种类和数目相同,中心离子的配位数相同且T中也只有两种配体,若1molT溶于水,加入足量AgNO3溶液只生成2molAgCl,则T的配合物可表示为_____ 。
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为_____ 。

(1)氮氧共掺杂多孔碳材料是一种新型高效的能源存储材料,其中的三种主要元素C、N、O,电负性从小到大的顺序是
(2)根据杂化轨道理论的相关知识,在NH3、BF3、SO
 、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是
、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是(3)有一种配合物组成为[M(NH3)5(H2O)]Cl3,该配合物中提供孤电子对的原子是
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为

您最近一年使用:0次
名校
5 . 一种合成药物中间体的结构式如图所示,X、Y、Z、W为短周期主族元素,且X、Y、Z的原子序数之和等于W的原子序数。下列说法正确的是


| A.电负性W<X<Y |
| B.第一电离能Y<W<Z |
| C.简单气态氢化物的沸点W比Z的高 |
| D.W的基态原子的核外电子共占据8个轨道 |
您最近一年使用:0次
2023-04-28更新
|
123次组卷
|
2卷引用:山东省德州市2022-2023学年高二下学期4月期中考试化学试题
6 . 自然界中存在大量的金属元素,在工农业生产中有着广泛的应用。回答下列问题:
(1)下列有关微粒性质的排列顺序错误的是___________。
(2)基态Ni原子核外电子运动状态有___________ 种,其核外电子排布式中未成对电子数为___________ 个。
(3)钌−多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(II)的配位数是___________ ,N原子的杂化类型为___________ 。

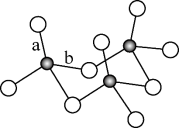
(4)SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为___________ ;该结构中S−O键长有两类,一类键长约140pm,另一类键长约为160pm,较长的键为___________ (填图中字母),该分子中含有___________ 个σ键。
(1)下列有关微粒性质的排列顺序错误的是___________。
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
| C.离子半径:O2−>Na+>Mg2+ | D.原子的未成对电子数:Mn>Si>Cl |
(3)钌−多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(II)的配位数是

(4)SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为

您最近一年使用:0次
名校
7 . 2021年9月24日《科学》杂志发表了我国科学家的原创性重大突破,首次在实验室实现从 到淀粉的全合成。其合成路线如下:
到淀粉的全合成。其合成路线如下:
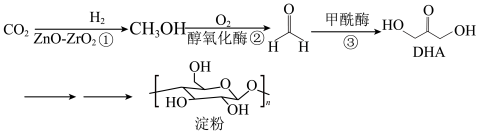
下列说法错误的是
 到淀粉的全合成。其合成路线如下:
到淀粉的全合成。其合成路线如下:
下列说法错误的是
| A.电负性:O>C>H>Zn |
| B.甲醇分子中H—C—O键角大于甲醛分子中H—C—O键角 |
| C.DHA分子间存在氢键 |
D.Zn溶于氨水形成配合物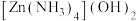 , , 的配位数为6 的配位数为6 |
您最近一年使用:0次
2023-03-17更新
|
218次组卷
|
2卷引用:山东省德州市第一中学2022-2023学年高二下学期4月期中化学试题
名校
8 . 自然界中存在大量的金属元素,在工农业生产中有着广泛的应用。回答下列问题:
(1)下列有关微粒性质的排列顺序错误的是_____ 。
(2)基态Ni原子核外电子运动状态有_____ 种,其核外电子排布式中未成对电子数为_____ 个。
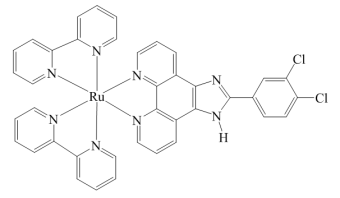
(3)钌-多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(II)的配位数是______ ,N原子的杂化类型为______ 。
(4)氧铬酸钙是一种常见含铬矿石,其立方晶胞如图所示。
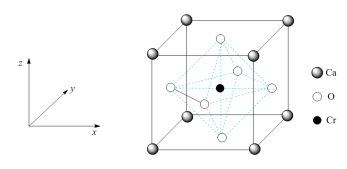
①氧铬酸钙的化学式为_____ 。
②1个钙原子与_____ 个氧原子最近且等距离。
③该晶体密度为_____ g•cm-3(列出计算式即可。已知Ca和O的最近距离为anm,NA代表阿伏加德罗常数)
(1)下列有关微粒性质的排列顺序错误的是
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
| C.离子半径:O2->Na+>Mg2+ | D.原子的未成对电子数:Mn>Si>Cl |
(3)钌-多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(II)的配位数是

(4)氧铬酸钙是一种常见含铬矿石,其立方晶胞如图所示。

①氧铬酸钙的化学式为
②1个钙原子与
③该晶体密度为
您最近一年使用:0次
名校
解题方法
9 . 硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参数为pnm,乙图为晶胞的俯视图,下列说法正确的是
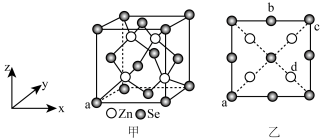
| A.晶胞中硒原子的配位数为12 |
B.晶胞中d点原子分数坐标为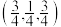 |
C.相邻两个Zn原子的最短距离为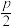 nm nm |
| D.电负性:Zn>Se |
您最近一年使用:0次
2023-03-03更新
|
1858次组卷
|
11卷引用:山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题
山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题山东省济宁市2023届高三一模考试(3月)化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题(已下线)专题十 晶胞示意图(练)福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题河南省驻马店市环际大联考2022-2023学年高二下学期4月期中考试化学试题(已下线)热点08 金属晶体和离子晶体山东省烟台市第一中学2023-2024学年高三下学期3月月考化学试题山东省临沂市第二十四中学2023-2024学年高二下学期3月学科素养水平监测化学试题
解题方法
10 . 亚铁氰化钾( )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。
(1)O元素位于_______ 区,基态O原子核外电子的空间运动状态有_______ 种。
(2)Fe在元素周期表中的位置_______ ,基态Fe原子的价电子轨道表示式为_______ 。
(3)黄血盐( )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是_______ ,该原子能量最高的电子所在能级符号为_______ 。
(4)亚铁氰化钾( )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为_______ 。
(5)普鲁士蓝( )中不同价态铁元素的简单微粒较稳定的是
)中不同价态铁元素的简单微粒较稳定的是_______ ,其原因是_______ 。
 )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。(1)O元素位于
(2)Fe在元素周期表中的位置
(3)黄血盐(
 )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是(4)亚铁氰化钾(
 )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为(5)普鲁士蓝(
 )中不同价态铁元素的简单微粒较稳定的是
)中不同价态铁元素的简单微粒较稳定的是
您最近一年使用:0次



