解题方法
1 . 已知: ,氢氧化铜悬浊液受热易分解生成
,氢氧化铜悬浊液受热易分解生成 。蚀刻含铜电路板有多种方法,用蚀刻废液可制备
。蚀刻含铜电路板有多种方法,用蚀刻废液可制备 。
。
(1)酸性蚀刻液法(过氧化氢-盐酸法)。
①用过氧化氢和盐酸蚀刻含铜电路板时发生的离子反应方程式为_______ 。
②反应后有气泡产生,且反应一段时间后,随着溶液变蓝,产生气泡的速率加快,可能的原因是_______ 。
(2)碱性蚀刻液法。碱性含铜蚀刻液主要成分为 、氨水、氯化铵等。蚀刻过程中,
、氨水、氯化铵等。蚀刻过程中, 与电路板上的铜发生反应生成
与电路板上的铜发生反应生成 ,失去蚀刻能力,通入空气可恢复蚀刻能力。
,失去蚀刻能力,通入空气可恢复蚀刻能力。
①
 中
中 键的数目为
键的数目为_______ 。
②蚀刻能力恢复的化学方程式为_______ 。
(3)酸性蚀刻废液与碱性蚀刻废液混和可析出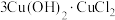 沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
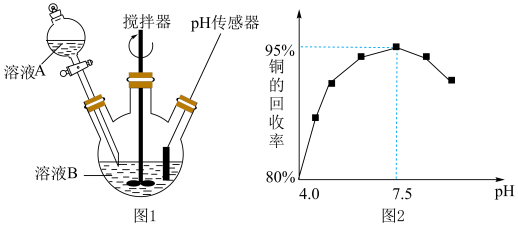
①为减少 胶体形成而影响后续操作,溶液A为
胶体形成而影响后续操作,溶液A为_______ (选填“酸性”或“碱性”)蚀刻废液。
② 时,铜元素回收率下降的原因为
时,铜元素回收率下降的原因为_______ 。
(4)设计从酸性蚀刻废液中制备氧化铜的实验方案。向一定质量的酸性蚀刻废液中_______ 。(实验中必须 使用的试剂:20% 溶液、硝酸银溶液、稀硝酸、蒸馏水)
溶液、硝酸银溶液、稀硝酸、蒸馏水)
 ,氢氧化铜悬浊液受热易分解生成
,氢氧化铜悬浊液受热易分解生成 。蚀刻含铜电路板有多种方法,用蚀刻废液可制备
。蚀刻含铜电路板有多种方法,用蚀刻废液可制备 。
。(1)酸性蚀刻液法(过氧化氢-盐酸法)。
①用过氧化氢和盐酸蚀刻含铜电路板时发生的离子反应方程式为
②反应后有气泡产生,且反应一段时间后,随着溶液变蓝,产生气泡的速率加快,可能的原因是
(2)碱性蚀刻液法。碱性含铜蚀刻液主要成分为
 、氨水、氯化铵等。蚀刻过程中,
、氨水、氯化铵等。蚀刻过程中, 与电路板上的铜发生反应生成
与电路板上的铜发生反应生成 ,失去蚀刻能力,通入空气可恢复蚀刻能力。
,失去蚀刻能力,通入空气可恢复蚀刻能力。①

 中
中 键的数目为
键的数目为②蚀刻能力恢复的化学方程式为
(3)酸性蚀刻废液与碱性蚀刻废液混和可析出
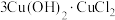 沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
①为减少
 胶体形成而影响后续操作,溶液A为
胶体形成而影响后续操作,溶液A为②
 时,铜元素回收率下降的原因为
时,铜元素回收率下降的原因为(4)设计从酸性蚀刻废液中制备氧化铜的实验方案。向一定质量的酸性蚀刻废液中
 溶液、硝酸银溶液、稀硝酸、蒸馏水)
溶液、硝酸银溶液、稀硝酸、蒸馏水)
您最近一年使用:0次
真题
名校
2 . 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是
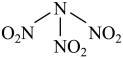

| A.分子中N、O间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 |
D.15.2g该物资含有6.02× 个原子 个原子 |
您最近一年使用:0次
2019-01-30更新
|
1467次组卷
|
38卷引用:2011-2012学年江苏省重点中学高二5月质量检测化学试卷
(已下线)2011-2012学年江苏省重点中学高二5月质量检测化学试卷(已下线)2012-2013学年江苏省启东中学高二下学期期中考试化学试卷2011年普通高等学校招生全国统一考试化学卷(安徽)(已下线)2012届湖北省襄阳五中高三上学期期中考试化学试卷(已下线)2011-2012学年浙江省杭州十四中高二上学期期末化学试卷(已下线)2011-2012学年福建省三明一中高二下学期第一次月考化学试卷(已下线)2013届江西省九江市第一中学高三入学考试化学试卷(已下线)2012-2013学年四川省成都七中高二10月阶段性考试化学试卷(已下线)2012--2013学年新疆乌鲁木齐市一中高二下学期期中考试化学试卷(特长班)(已下线)2012-2013学年四川省昭觉中学高二10月月考化学试卷(已下线)2013-2014甘肃省兰州一中下学期期中考试高二化学试卷(已下线)2013-2014甘肃省兰州一中下学期期中考试高二化学试卷(已下线)2013届新疆乌鲁木齐市一中高二下学期特长班期中考试化学试卷(已下线)2015届江西省南昌市三校高三上第一次联考化学试卷2014-2015宁夏银川市唐徕回民中学高二下学期3月月考化学试卷2014-2015福建省长泰县第一中学高二下学期期中化学试卷(A)2016-2017学年安徽省六安市第一中学高二下学期第一次阶段检测化学试卷甘肃省兰州第一中学2016-2017学年高一下学期期中考试化学试题河北省唐山市曹妃甸区第一中学2016-2017学年高二下学期期末考试化学试题河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第二章 综合检测2安徽省定远重点中学2017-2018学年高一下学期第一次月考化学试题福建省长汀一中2017-2018学年高二实验班下学期第一次月考化学试题【全国百强校】黑龙江省实验中学2017-2018学年高二下学期期中考试(理)化学试题贵州省六盘水盘县四中2017-2018学年高二下学期期末考试化学试题(已下线)2019年3月10日 《每日一题》人教选修3-每周一测上海市交通大学附属中学2018-2019学年高一下学期期中考试化学试题山西省平遥中学校2018-2019学年高二下学期第二次月考化学试题(已下线)上海交大附中2018-2019学年高一下学期期中化学试题2020高三总复习二轮复习——物质结构与性质复习卷云南省金平县第一中学2019-2020学年高二上学期期末考试化学试题苏教版高一化学必修2专题一第二单元第二课时《共价键》(夯基提能)山东省滕州市第一中学2020届高三3月线上模拟考试化学试题(已下线)上海市奉贤区2013年高考二模化学试题安徽省六安市舒城中学2019-2020学年高二下学期第一次月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高二4月月考化学试题重庆市第七中学校2021-2022学年高一下学期3月月考化学试题福建省德化第一中学2021-2022学年高二下学期第一次质检化学试题安徽省青阳县第一中学2021-2022学年高二下学期3月月考化学试卷
名校
解题方法
3 . 氮族和碳族元素的单质及其化合物在研究和生产中有着广泛的应用。试回答下列问题:
(1) 是一种重要的化工原料,有毒,
是一种重要的化工原料,有毒, 也是一种食品添加剂,使用时须严格控制用量。已知:
也是一种食品添加剂,使用时须严格控制用量。已知: 有强氧化性,酸性
有强氧化性,酸性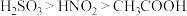 。
。
①亚硝酰氯 是一种红褐色液体,每个原子最外层都达到8电子结构,则其电子式为
是一种红褐色液体,每个原子最外层都达到8电子结构,则其电子式为_____ ,其与水反应会生成两种酸,写出该化学方程式_______ 。
②往冷的 溶液中加入下列某种物质可得
溶液中加入下列某种物质可得 稀溶液,该物质是
稀溶液,该物质是______ (填字母)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)硅和氯气单质反应可以得到 。
。
①和 互为等电子体的阴离子有
互为等电子体的阴离子有___________ 。(写一种)___________ ,1个 中含有
中含有___________ 个 键。
键。
(3)砷化镓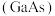 是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
①基态 原子外围电子轨道表示式为
原子外围电子轨道表示式为___________ ,N、 、
、 第一电离能由大到小的顺序是
第一电离能由大到小的顺序是___________ 。
②砷化镓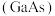 太阳能电池为我国“玉兔二号”月球车提供充足能量。
太阳能电池为我国“玉兔二号”月球车提供充足能量。 的晶胞结构如图甲所示,将
的晶胞结构如图甲所示,将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料如图乙所示。
的晶体中得到稀磁性半导体材料如图乙所示。 中
中 的化合价为
的化合价为___________ 。在 掺杂到
掺杂到 的晶体中每个
的晶体中每个 最近且等距离的
最近且等距离的 的数目为
的数目为___________ 。
(1)
 是一种重要的化工原料,有毒,
是一种重要的化工原料,有毒, 也是一种食品添加剂,使用时须严格控制用量。已知:
也是一种食品添加剂,使用时须严格控制用量。已知: 有强氧化性,酸性
有强氧化性,酸性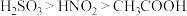 。
。①亚硝酰氯
 是一种红褐色液体,每个原子最外层都达到8电子结构,则其电子式为
是一种红褐色液体,每个原子最外层都达到8电子结构,则其电子式为②往冷的
 溶液中加入下列某种物质可得
溶液中加入下列某种物质可得 稀溶液,该物质是
稀溶液,该物质是a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)硅和氯气单质反应可以得到
 。
。①和
 互为等电子体的阴离子有
互为等电子体的阴离子有② 与
与 -甲基咪唑(
-甲基咪唑(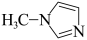 )反应可以得到
)反应可以得到 ,其结构如图所示:
,其结构如图所示:
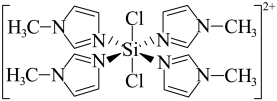
 中含有
中含有 键。
键。(3)砷化镓
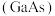 是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。①基态
 原子外围电子轨道表示式为
原子外围电子轨道表示式为 、
、 第一电离能由大到小的顺序是
第一电离能由大到小的顺序是②砷化镓
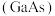 太阳能电池为我国“玉兔二号”月球车提供充足能量。
太阳能电池为我国“玉兔二号”月球车提供充足能量。 的晶胞结构如图甲所示,将
的晶胞结构如图甲所示,将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料如图乙所示。
的晶体中得到稀磁性半导体材料如图乙所示。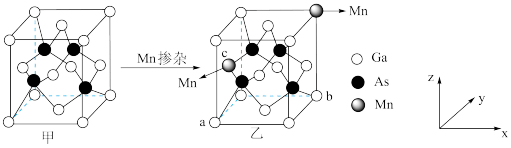
 中
中 的化合价为
的化合价为 掺杂到
掺杂到 的晶体中每个
的晶体中每个 最近且等距离的
最近且等距离的 的数目为
的数目为
您最近一年使用:0次
4 . 运用化学反应原理研究硫、氮等单质及其化合物的反应,对生产、生活、环境保护等领域有着重要的意义。
(1)天然气中要加入少量有特殊气味的乙硫醇( ),
), 分子中S—H的极性小于
分子中S—H的极性小于 分子中O—H的极性,请解释其原因:
分子中O—H的极性,请解释其原因:___________ 。
(2)工业上采用 催化还原
催化还原 ,不仅可以消除
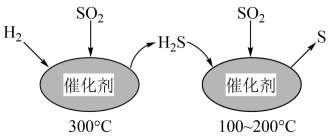
,不仅可以消除 污染,而且可得到有价值的单质S。反应分两步完成,如图所示,
污染,而且可得到有价值的单质S。反应分两步完成,如图所示, 催化还原
催化还原 第一步反应的化学方程式为
第一步反应的化学方程式为___________ 。
(3)燃煤烟气中含有 和
和 ,工业上常用
,工业上常用 溶液对燃煤烟气进行脱硫脱硝。已知
溶液对燃煤烟气进行脱硫脱硝。已知 溶液具有强氧化性,酸性条件下
溶液具有强氧化性,酸性条件下 发生歧化反应生成
发生歧化反应生成 ,
, 易溶于水,具有强氧化性,可氧化
易溶于水,具有强氧化性,可氧化 或
或 。
。
①在实验室模拟脱硫过程:调节 吸收液的pH为5,向其中通入含
吸收液的pH为5,向其中通入含 的模拟烟气。测得脱硫反应后,溶液中的阴离子为
的模拟烟气。测得脱硫反应后,溶液中的阴离子为 和
和 ,则脱硫反应的离子方程式为
,则脱硫反应的离子方程式为___________ 。
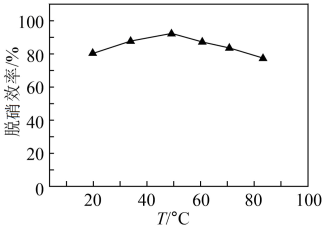
②在实验室模拟脱硝过程:调节 吸收液的pH为5,向其中通入含NO的模拟烟气。测得脱硝效率(即NO的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于50℃时,随温度升高脱硝效率下降的原因是
吸收液的pH为5,向其中通入含NO的模拟烟气。测得脱硝效率(即NO的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于50℃时,随温度升高脱硝效率下降的原因是___________ 。
③在实验室模拟同时脱硫、脱硝过程:调节 吸收液的pH为5,向其中通入含
吸收液的pH为5,向其中通入含 和NO(体积比4:1)的模拟烟气。测得脱硫反应速率大于脱硝反应速率,原因是除了
和NO(体积比4:1)的模拟烟气。测得脱硫反应速率大于脱硝反应速率,原因是除了 和NO在烟气中的初始浓度不同,还可能是
和NO在烟气中的初始浓度不同,还可能是___________ 。
(1)天然气中要加入少量有特殊气味的乙硫醇(
 ),
), 分子中S—H的极性小于
分子中S—H的极性小于 分子中O—H的极性,请解释其原因:
分子中O—H的极性,请解释其原因:(2)工业上采用
 催化还原
催化还原 ,不仅可以消除
,不仅可以消除 污染,而且可得到有价值的单质S。反应分两步完成,如图所示,
污染,而且可得到有价值的单质S。反应分两步完成,如图所示, 催化还原
催化还原 第一步反应的化学方程式为
第一步反应的化学方程式为
(3)燃煤烟气中含有
 和
和 ,工业上常用
,工业上常用 溶液对燃煤烟气进行脱硫脱硝。已知
溶液对燃煤烟气进行脱硫脱硝。已知 溶液具有强氧化性,酸性条件下
溶液具有强氧化性,酸性条件下 发生歧化反应生成
发生歧化反应生成 ,
, 易溶于水,具有强氧化性,可氧化
易溶于水,具有强氧化性,可氧化 或
或 。
。①在实验室模拟脱硫过程:调节
 吸收液的pH为5,向其中通入含
吸收液的pH为5,向其中通入含 的模拟烟气。测得脱硫反应后,溶液中的阴离子为
的模拟烟气。测得脱硫反应后,溶液中的阴离子为 和
和 ,则脱硫反应的离子方程式为
,则脱硫反应的离子方程式为②在实验室模拟脱硝过程:调节
 吸收液的pH为5,向其中通入含NO的模拟烟气。测得脱硝效率(即NO的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于50℃时,随温度升高脱硝效率下降的原因是
吸收液的pH为5,向其中通入含NO的模拟烟气。测得脱硝效率(即NO的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于50℃时,随温度升高脱硝效率下降的原因是
③在实验室模拟同时脱硫、脱硝过程:调节
 吸收液的pH为5,向其中通入含
吸收液的pH为5,向其中通入含 和NO(体积比4:1)的模拟烟气。测得脱硫反应速率大于脱硝反应速率,原因是除了
和NO(体积比4:1)的模拟烟气。测得脱硫反应速率大于脱硝反应速率,原因是除了 和NO在烟气中的初始浓度不同,还可能是
和NO在烟气中的初始浓度不同,还可能是
您最近一年使用:0次
名校
解题方法
5 . 氮是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反应中,N2(g)与H2(g)反应生成1molNH3(g)放出46kJ的热量,实验室用加热NH4Cl和Ca(OH)2固体混合物的方法制取少量氨气,同时生成CaCl2。肼(N2H4)是一种良好的液体燃料。下列物质结构与性质或物质性质与用途具有对应关系的是
| A.N2分子内含有N≡N,N2具有氧化性 |
| B.NH3极易溶于水,液氨可用作制冷剂 |
| C.NH3分子之间形成氢键,NH3(g)的热稳定性比PH3(g)的高 |
| D.N2H4具有还原性,可用作喷气式发动机的燃料 |
您最近一年使用:0次
6 . 由多个单原子组成的“超级原子”具有单个原子不具有的化学性质,如 和
和 ,可与呈链形的碘分子发生反应,“超级原子”
,可与呈链形的碘分子发生反应,“超级原子” 会取代碘分子中的一个碘原子的位置,其他碘原子也“悬挂”在“超级原子”上,这种新的碘铝化合物既有金属铝的性质,又有非金属碘的性质,通常“超级原子”易形成最外层电子数之和为40的相对稳定状态。下列说法错误的是
会取代碘分子中的一个碘原子的位置,其他碘原子也“悬挂”在“超级原子”上,这种新的碘铝化合物既有金属铝的性质,又有非金属碘的性质,通常“超级原子”易形成最外层电子数之和为40的相对稳定状态。下列说法错误的是
 和
和 ,可与呈链形的碘分子发生反应,“超级原子”
,可与呈链形的碘分子发生反应,“超级原子” 会取代碘分子中的一个碘原子的位置,其他碘原子也“悬挂”在“超级原子”上,这种新的碘铝化合物既有金属铝的性质,又有非金属碘的性质,通常“超级原子”易形成最外层电子数之和为40的相对稳定状态。下列说法错误的是
会取代碘分子中的一个碘原子的位置,其他碘原子也“悬挂”在“超级原子”上,这种新的碘铝化合物既有金属铝的性质,又有非金属碘的性质,通常“超级原子”易形成最外层电子数之和为40的相对稳定状态。下列说法错误的是A. 具有氧化性, 具有氧化性, 具有还原性 具有还原性 | B.Al的第一电离能比Mg小 |
C. 可与Mg形成 可与Mg形成 | D. 中的Al原子间通过离子键结合 中的Al原子间通过离子键结合 |
您最近一年使用:0次
2022-03-17更新
|
883次组卷
|
3卷引用:江苏省泰州中学2021-2022学年高一下学期期中考试化学试题
7 . V2O5是冶金、化工等工业中的重要催化剂,是一种橙黄色片状晶体,微溶于水,具有强氧化性,属于两性氧化物。某研究小组将从钒铅锌矿(主要含有V2O5、PbO、ZnO、CaO)中提取V2O5及回收铅、锌等金属。工艺流程如图所示:
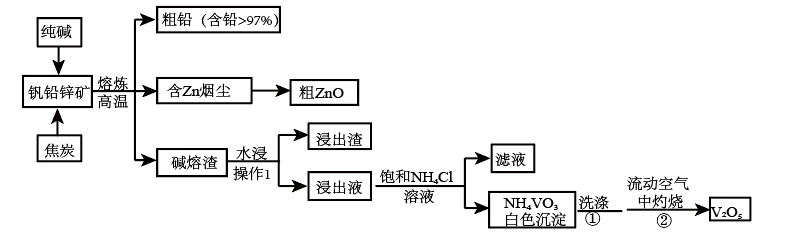
已知:①NH4VO3是白色粉末,可溶于热水,微溶于冷水,不溶于乙醇、乙醚。
②2NH4VO3 V2O5+2NH3↑+H2O
V2O5+2NH3↑+H2O
请回答:
(1)V2O5的结构式为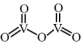 ,则1个V2O5分子中σ键的数目为
,则1个V2O5分子中σ键的数目为___________ 。
(2)钒铅锌矿高温熔炼时,V2O5与纯碱反应的化学方程式为___________ 。
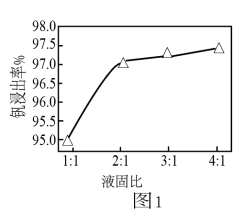
(3)钒浸出过程中,液固比(液体质量:固体质量)对钒浸出率的影响如图1所示。分析图象可知,浸出过程的液固比最合适的比例约为2:1,理由是___________ 。
(4)在洗涤①操作时,为减少产物的溶解损失,可选用冷水。证明沉淀洗涤干净的操作是___________ 。
(5)在灼烧②操作时,需在流动空气中灼烧的可能原因___________ 。
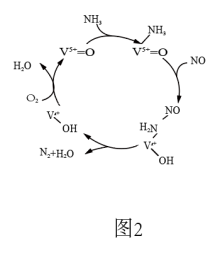
(6)V2O5的应用:有氧条件下,NO在钒基催化剂(V2O5)作用下可被NH3还原为N2。根据图2所示反应机理,NO、NH3在有氧条件下的总化学方程式是___________ 。

已知:①NH4VO3是白色粉末,可溶于热水,微溶于冷水,不溶于乙醇、乙醚。
②2NH4VO3
 V2O5+2NH3↑+H2O
V2O5+2NH3↑+H2O请回答:
(1)V2O5的结构式为
 ,则1个V2O5分子中σ键的数目为
,则1个V2O5分子中σ键的数目为(2)钒铅锌矿高温熔炼时,V2O5与纯碱反应的化学方程式为
(3)钒浸出过程中,液固比(液体质量:固体质量)对钒浸出率的影响如图1所示。分析图象可知,浸出过程的液固比最合适的比例约为2:1,理由是

(4)在洗涤①操作时,为减少产物的溶解损失,可选用冷水。证明沉淀洗涤干净的操作是
(5)在灼烧②操作时,需在流动空气中灼烧的可能原因
(6)V2O5的应用:有氧条件下,NO在钒基催化剂(V2O5)作用下可被NH3还原为N2。根据图2所示反应机理,NO、NH3在有氧条件下的总化学方程式是

您最近一年使用:0次
名校
8 . 高分子纳米活性钛无霸是钛氧化物经过光照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解存在生活空间中的一些有害物质(甲醛、氮氧化物等)。
(1)Ti2+的基态价电子排布式为_______________________ 。
(2)甲醛分子中C原子轨道杂化类型为____________ 。1mol甲醛分子中含有σ键的数目为___________ 。
(3)甲醛易溶于水,除因为它们都是极性分子外,还因为_______________________ 。
(4)与N2O互为等电子体的一种分子为________________________ (填化学式) 。
(5)某含钛化合物晶胞结构如图所示,该化合物的化学式为_____________________ 。

(1)Ti2+的基态价电子排布式为
(2)甲醛分子中C原子轨道杂化类型为
(3)甲醛易溶于水,除因为它们都是极性分子外,还因为
(4)与N2O互为等电子体的一种分子为
(5)某含钛化合物晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
2016-01-12更新
|
219次组卷
|
2卷引用:2016届江苏省苏北四市高三上学期期中质量抽测化学试卷
名校
9 . 下列说法中不正确的是( )
| A.N2O与CO2、CCl3F与CC12F2互为等电子体 |
| B.CCl2F2无同分异构体,说明其中碳原子采用sp3方式杂化 |
| C.H2CO3与H3PO4的非羟基氧原子数均为1,二者的酸性(强度)非常相近 |
| D.由I A族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子化合物 |
您最近一年使用:0次
2017-02-23更新
|
738次组卷
|
9卷引用:江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题
江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题2016-2017学年河北省衡水中学高二上学期五调考试化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第二章 综合检测2吉林省扶余市第一中学2018-2019学年高二下学期第一次月考化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题黑龙江省鸡西市鸡东县第二中学2019-2020 学年高二下学期期末考试化学试题福建省福州第一中学2019-2020学年高二下学期期末考试化学试题福建省建瓯市芝华中学2020-2021学年高二下学期第一阶段考试化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题



