名校
1 . 下列说法错误的是
| A.NH4+和CH4属于等电子体,立体构型都是正四面体 |
| B.主族元素的原子核外电子最后填入的能级是s能级或p能级 |
| C.BF3、NCl3、H2O分子中所有原子都满足最外层为8电子结构的是NCl3 |
| D.向盛有硫酸铜溶液的试管里加入过量氨水,将得到蓝色的氢氧化铜沉淀 |
您最近一年使用:0次
2016-12-09更新
|
456次组卷
|
4卷引用:2014-2015宁夏银川市唐徕回民中学高二下学期3月月考化学试卷
名校
2 . 海底有大量的天然气水合物,可满足人类1000年的能源需要。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O分子。若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为
| A.CH4·14H2O |
| B.CH4·8H2O |
C.CH4· H2O H2O |
| D.CH4·6H2O |
您最近一年使用:0次
2016-12-09更新
|
141次组卷
|
2卷引用:2014-2015黑龙江省哈尔滨六中高二上期末化学试卷
14-15高三上·浙江绍兴·阶段练习
名校
解题方法
3 . 下列说法正确的是
| A.π键是由两个p轨道“头碰头”重叠形成的 |
| B.σ键就是单键,π键就是双键 |
| C.乙烷分子中的键全为σ键,而乙烯分子中含σ键和π键 |
| D.H2分子中含σ键,而Cl2分子中含π键 |
您最近一年使用:0次
2016-12-09更新
|
454次组卷
|
5卷引用:2015届浙江省柯桥中学高三月考(10月)化学试卷
13-14高二下·河北唐山·期末
解题方法
4 . 下列关于σ键和π键的理解不正确的是
| A.σ键能单独形成,而π键一定不能单独形成 |
| B.σ键可以绕键轴旋转,π键一定不能绕键轴旋转 |
| C.HCl 分子中的σ键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成的 |
| D.气体单质中一定存在σ键,可能存在π键 |
您最近一年使用:0次
13-14高二下·山西太原·期中
5 . 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z基态原子的2p轨道上有3个未成对电子。下列说法正确的是
| A.X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有12mol σ键 |
| B.Z的最高价含氧酸分子中,羟基氧和非羟基氧个数比为1:1 |
| C.Y的气态氢化物分子中H—Y—H键角比Y的最高价氧化物分子中O—Y—O键角小 |
| D.Z的气态氢化物比Y的气态氢化物稳定,是因为氢键的影响 |
您最近一年使用:0次
2016-12-09更新
|
395次组卷
|
3卷引用:2013-2014山西省太原五中高二下学期期中化学(理)试卷
(已下线)2013-2014山西省太原五中高二下学期期中化学(理)试卷河北省邢台三中2017-2018学年高二下学期3月月考化学试题福建省永春县第一中学2018-2019学年高二下学期期中考试化学试题
6 . 电子数相等的微粒叫做等电子微粒,下列各组微粒属于等电子微粒是
| A.CO和CO2 | B.NO和CO | C.CH4和NH3 | D.OH- 和S2- |
您最近一年使用:0次
2016-12-09更新
|
2009次组卷
|
6卷引用:2013-2014甘肃省嘉峪关市第二学期期末高一联合考试化学试卷
2014高三·全国·专题练习
7 . 【物质结构与性质】
已知A、B、C、D、E都是元素周期表中前36号的元素,它们的原子序数依次增大。A原子基态时最外层电子数是其内层电子总数的2倍,B原子基态时s电子数与P电子数相等,C在元素周期表的各元素中电负性最大,D的基态原子核外有6个能级且全部充满电子,E原子基态时未成对电子数是同周期元素中最多的。
(1)基态E原子的价电子排布式为________________________ ;
(2)AB32-的立体构型是____________ ,其中A原子的杂化轨道类型是___________________________ 。
(3)A22-与B22+互为等电子体,B22+的电子式可表示为________________ ,1molB22+中含有的π键数目为________________________ 。
(4)用氢键表示式写出C的氢化物水溶液中存在的所有氢键___________________ 。
(5)化合物DC2的晶胞结构如图所示,该离子化合协晶体的密度为ag/cm3,则晶胞的体积是_________________ (只要求列算式,阿伏加德罗常数的值为NA)
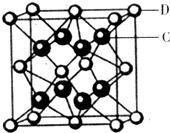
已知A、B、C、D、E都是元素周期表中前36号的元素,它们的原子序数依次增大。A原子基态时最外层电子数是其内层电子总数的2倍,B原子基态时s电子数与P电子数相等,C在元素周期表的各元素中电负性最大,D的基态原子核外有6个能级且全部充满电子,E原子基态时未成对电子数是同周期元素中最多的。
(1)基态E原子的价电子排布式为
(2)AB32-的立体构型是
(3)A22-与B22+互为等电子体,B22+的电子式可表示为
(4)用氢键表示式写出C的氢化物水溶液中存在的所有氢键
(5)化合物DC2的晶胞结构如图所示,该离子化合协晶体的密度为ag/cm3,则晶胞的体积是

您最近一年使用:0次
2016-12-09更新
|
1361次组卷
|
3卷引用:2014高考名师推荐化学--预测8
(已下线)2014高考名师推荐化学--预测8广西钦州市钦州港经济技术开发区2016-2017学年高二下学期期末考试化学试题贵州省遵义航天高级中学2018届高三第一次模拟考试(9月月考)理科综合化学试题
名校
解题方法
8 . 某分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法中错误的是( )


| A.X原子可能为第ⅤA族元素 |
| B.Y原子一定为第ⅠA族元素 |
| C.该分子中既含有极性共价键又含有非极性共价键 |
| D.从圆球的大小分析,该分子可能为N2F4 |
您最近一年使用:0次
2016-12-09更新
|
401次组卷
|
13卷引用:2014-2015学年重庆市巫山中学高一下学期期末考试化学试卷
2014-2015学年重庆市巫山中学高一下学期期末考试化学试卷2015-2016学年辽宁沈阳市第二中学高一下期末考试化学卷2016-2017学年湖南省长沙一中高一上第二次月考化学卷湖南省长沙市明德中学2015-2016学年高一(文化班)下学期期中考试化学试题河北省张家口市第一中学2016-2017学年高一(衔接班)下学期期末考试(理)化学试题【全国百强校】河北省张家口市第一中学2018-2019学年高一下学期4月月考化学试题苏教版高一化学必修2专题一第二单元第二课时《共价键》(夯基提能)专题5 第二单元综合拔高练-高中化学苏教2019版必修第一册四川省成都市阳安中学2020-2021学年高一下学期3月月考化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期中考试化学试题陕西省汉中市洋县中学2020-2021学年高一上学期第三次月考试题内蒙古包头市第四中学2020-2021学年高一下学期4月月考化学试题四川省成都东部新区养马中学2020-2021学年高一下学期第一次月考化学试题
2013·山东济宁·一模
名校
解题方法
9 . MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的核外电子排布式________________________ 。
(2)CoTiO3晶体结构模型如图1所示。在CoTiO3晶体中1个Ti原子、1个Co原子,周围距离最近的O原子数目分别为_______ 个、_______ 个。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂, 常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为______________ 、_______ (各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图所示。
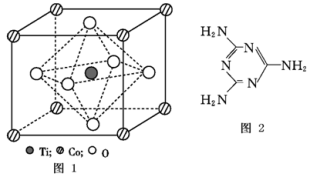
三聚氰胺分子中氮原子轨道杂化类型是______ ,1 mol三聚氰胺分子中σ键的数目为_______ 。
(1)写出基态Mn原子的核外电子排布式
(2)CoTiO3晶体结构模型如图1所示。在CoTiO3晶体中1个Ti原子、1个Co原子,周围距离最近的O原子数目分别为
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂, 常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为
(4)三聚氰胺是一种含氮化合物,其结构简式如图所示。

三聚氰胺分子中氮原子轨道杂化类型是
您最近一年使用:0次
14-15高三上·上海·阶段练习
解题方法
10 . 下列物质性质的变化规律中与共价键键能大小有关的是
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低
| A.仅③ | B.①③ | C.②④ | D.②③ |
您最近一年使用:0次



