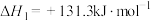1 . 已知 与少量
与少量 的反应为
的反应为 。下列说法正确的是
。下列说法正确的是
 与少量
与少量 的反应为
的反应为 。下列说法正确的是
。下列说法正确的是A. 分子中含 分子中含 键 键 | B. 分子中含 分子中含  键 键 |
C. 分子中含孤电子对 分子中含孤电子对 | D.热稳定性: |
您最近半年使用:0次
2 . 已知四氨合铜离子的模型如图甲,CaF2晶体的晶胞如图乙,阿伏加德罗常数的值用NA表示。下列有关说法正确的是
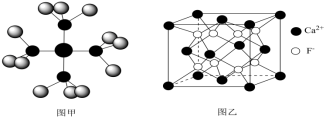
A.若CaF2晶胞的棱长为acm,CaF2的密度为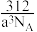 g/cm3 g/cm3 |
| B.四氨合铜离子中存在极性共价键、配位键、离子键 |
| C.距离Ca2+最近且等距离的F-有6个 |
| D.基态Cu2+的电子排布式为[Ar]3d84s1 |
您最近半年使用:0次
名校
解题方法
3 . 下列有关分子的结构和性质的说法正确的是
A. 和 和 均为直线形的非极性分子 均为直线形的非极性分子 |
B.酸性: ,是因为-CF3基团的推电子作用 ,是因为-CF3基团的推电子作用 |
C.硫难溶于水,微溶于酒精,易溶于 ,说明分子极性: ,说明分子极性: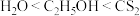 |
D. 和 和 均是极性分子, 均是极性分子, 的键角小于 的键角小于 的 的 |
您最近半年使用:0次
解题方法
4 . 水煤气是一种优质燃料和重要的化工原料,其制备方法是将水蒸气与焦炭在高温下混合反应,然后投入固体 进行处理。
进行处理。
I.在温度 下将高温水蒸气通入炽热的焦炭中,其中可能发生的一些反应如下:
下将高温水蒸气通入炽热的焦炭中,其中可能发生的一些反应如下:
(1)已知反应 的焓变
的焓变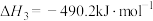 ,近似认为反应焓变不随温度变化,则焦炭的燃烧热
,近似认为反应焓变不随温度变化,则焦炭的燃烧热
______  。
。
(2)在温度 下体系达到化学平衡,将这一时刻记为
下体系达到化学平衡,将这一时刻记为 ,然后将可压缩的恒温反应容器突然压缩至原来体积的一半。将压缩之后这一瞬间的时刻记为
,然后将可压缩的恒温反应容器突然压缩至原来体积的一半。将压缩之后这一瞬间的时刻记为 ,重新达到平衡时的时刻记为
,重新达到平衡时的时刻记为 ,则______(填标号)。
,则______(填标号)。
(3)反应②的平衡常数 很小,若近似忽略生成
很小,若近似忽略生成 的反应,在一个体积固定的恒温容器内投入足量焦炭与一定量的水蒸气,在温度
的反应,在一个体积固定的恒温容器内投入足量焦炭与一定量的水蒸气,在温度 下达到平衡时水蒸气的转化率为
下达到平衡时水蒸气的转化率为 ,下图的三条曲线分别代表了达到平衡时不同的转化率
,下图的三条曲线分别代表了达到平衡时不同的转化率 对应的水蒸气分压、
对应的水蒸气分压、 分压、体系的总压,则代表
分压、体系的总压,则代表 分压的曲线是
分压的曲线是______ (填标号)。欲使平衡转化率为 ,则初始充入水蒸气的压强应为
,则初始充入水蒸气的压强应为______  (结果保留两位有效数字)。
(结果保留两位有效数字)。 ,生成
,生成 。除了以外,钙还有多种氧化物。
。除了以外,钙还有多种氧化物。
(4) 在大约
在大约 的高压条件下还可以进一步与
的高压条件下还可以进一步与 反应得到由
反应得到由 和
和 构成的另一种钙的氧化物
构成的另一种钙的氧化物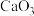 ,预测
,预测 的VSEPR模型名称是
的VSEPR模型名称是______ .
(5)反应生成的 在自然界中会被溶解有
在自然界中会被溶解有 的雨水溶蚀,该过程的离子方程式为
的雨水溶蚀,该过程的离子方程式为______ 。已知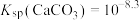 ,碳酸的
,碳酸的 (碳酸浓度以
(碳酸浓度以 形式计算)、
形式计算)、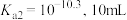 某雨水恰好能够溶解
某雨水恰好能够溶解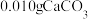 ,此时该雨水中的
,此时该雨水中的 浓度为
浓度为 ,忽略固体溶解产生的体积变化,则此时该雨水的
,忽略固体溶解产生的体积变化,则此时该雨水的 为
为______ 。
 进行处理。
进行处理。I.在温度
 下将高温水蒸气通入炽热的焦炭中,其中可能发生的一些反应如下:
下将高温水蒸气通入炽热的焦炭中,其中可能发生的一些反应如下:反应方程式 | 焓变 | 压强平衡常数 |
① |
|
|
② |
|
|
(1)已知反应
 的焓变
的焓变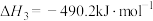 ,近似认为反应焓变不随温度变化,则焦炭的燃烧热
,近似认为反应焓变不随温度变化,则焦炭的燃烧热
 。
。(2)在温度
 下体系达到化学平衡,将这一时刻记为
下体系达到化学平衡,将这一时刻记为 ,然后将可压缩的恒温反应容器突然压缩至原来体积的一半。将压缩之后这一瞬间的时刻记为
,然后将可压缩的恒温反应容器突然压缩至原来体积的一半。将压缩之后这一瞬间的时刻记为 ,重新达到平衡时的时刻记为
,重新达到平衡时的时刻记为 ,则______(填标号)。
,则______(填标号)。A. 时,反应①的正反应速率比 时,反应①的正反应速率比 时增大 时增大 | B. 时,反应②的逆反应速率比 时,反应②的逆反应速率比 时减小 时减小 |
C. 时,反应①的压强平衡常数 时,反应①的压强平衡常数 比 比 时增大 时增大 | D. 时,水蒸气的转化率比 时,水蒸气的转化率比 时减小 时减小 |
(3)反应②的平衡常数
 很小,若近似忽略生成
很小,若近似忽略生成 的反应,在一个体积固定的恒温容器内投入足量焦炭与一定量的水蒸气,在温度
的反应,在一个体积固定的恒温容器内投入足量焦炭与一定量的水蒸气,在温度 下达到平衡时水蒸气的转化率为
下达到平衡时水蒸气的转化率为 ,下图的三条曲线分别代表了达到平衡时不同的转化率
,下图的三条曲线分别代表了达到平衡时不同的转化率 对应的水蒸气分压、
对应的水蒸气分压、 分压、体系的总压,则代表
分压、体系的总压,则代表 分压的曲线是
分压的曲线是 ,则初始充入水蒸气的压强应为
,则初始充入水蒸气的压强应为 (结果保留两位有效数字)。
(结果保留两位有效数字)。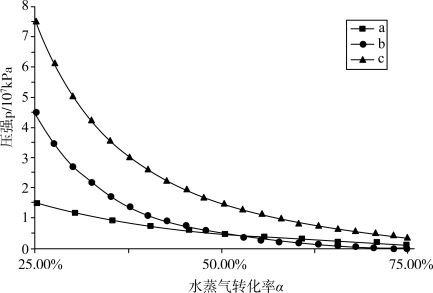
 ,生成
,生成 。除了以外,钙还有多种氧化物。
。除了以外,钙还有多种氧化物。(4)
 在大约
在大约 的高压条件下还可以进一步与
的高压条件下还可以进一步与 反应得到由
反应得到由 和
和 构成的另一种钙的氧化物
构成的另一种钙的氧化物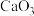 ,预测
,预测 的VSEPR模型名称是
的VSEPR模型名称是(5)反应生成的
 在自然界中会被溶解有
在自然界中会被溶解有 的雨水溶蚀,该过程的离子方程式为
的雨水溶蚀,该过程的离子方程式为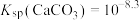 ,碳酸的
,碳酸的 (碳酸浓度以
(碳酸浓度以 形式计算)、
形式计算)、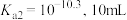 某雨水恰好能够溶解
某雨水恰好能够溶解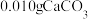 ,此时该雨水中的
,此时该雨水中的 浓度为
浓度为 ,忽略固体溶解产生的体积变化,则此时该雨水的
,忽略固体溶解产生的体积变化,则此时该雨水的 为
为
您最近半年使用:0次
7日内更新
|
200次组卷
|
2卷引用:湖南省新高考教学教研联盟2023-2024学年高三下学期第二次联考化学试题
解题方法
5 . 锌-空气电池被认为是替代锂离子电池、满足电动汽车爆炸性需求的下一代候选电池。用光照充电的锌-空气电池的工作原理如图所示。光照时,光电极 (空穴),驱动阴极和阳极反应。下列叙述不正确的是
(空穴),驱动阴极和阳极反应。下列叙述不正确的是
 (空穴),驱动阴极和阳极反应。下列叙述不正确的是
(空穴),驱动阴极和阳极反应。下列叙述不正确的是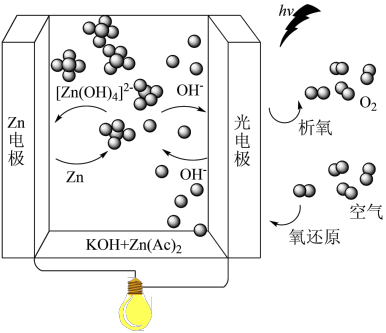
A.放电时, 向光电极迁移 向光电极迁移 | B.充电时的阳极反应为 |
C.放电时,光电子经电解液向 极移动 极移动 | D. 是配离子,配位数是4 是配离子,配位数是4 |
您最近半年使用:0次
7日内更新
|
261次组卷
|
2卷引用:湖南省新高考教学教研联盟2023-2024学年高三下学期第二次联考化学试题
解题方法
6 . 物质的结构决定其性质。下列实例与解释不相符的是
| 选项 | 事实 | 解释 |
| A | 金属是电的良导体 | 金属晶体中的自由电子在外电场作用下发生定向移动 |
| B | NF3不易与Cu2+形成配位键 | F的电负性大,导致N原子核对其孤电子对的吸引力大 |
| C | CO的沸点高于N2 | CO的极性大于N2 |
| D |  中的键角小于 中的键角小于 | S的原子半径较大,其价层σ键电子对之间的斥力较小 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7日内更新
|
358次组卷
|
4卷引用:河北省石家庄市2024届高三下学期4月第二次质检化学试题
河北省石家庄市2024届高三下学期4月第二次质检化学试题河北省石家庄二中实验学校2023-2024学年高二下学期第一次月考化学试题(已下线)化学(天津卷01)-2024年高考押题预测卷河北省重点高中2023-2024学年高三下学期5月高考模拟化学试题(二)
名校
7 . M、X、Y、Z、Q为相邻两个短周期的主族元素,且原子序数依次增大。这五种元素可形成化合物甲,其结构式如图所示,1mol甲含58mol电子,并且含有1mol配位键。下列说法正确的是
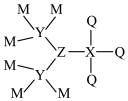
| A.Q是五种元素中原子半径最大的 |
B.水中溶解性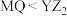 |
| C.Q、Y、Z三种元素的最简单氢化物具有相同的电子数 |
D.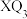 中所有原子均达到 中所有原子均达到 稳定结构 稳定结构 |
您最近半年使用:0次
8 . 一种叠氮化聚合物材料的片段结构如图所示,下列说法正确的是
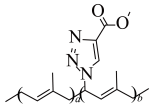
A.片段 的单体名称为2-甲基-2-丁烯 的单体名称为2-甲基-2-丁烯 | B.片段 中 中 原子的杂化方式有3种 原子的杂化方式有3种 |
C. 该片段中含有 该片段中含有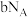 个手性碳原子 个手性碳原子 | D.该聚合物具有良好的导电性 |
您最近半年使用:0次
7日内更新
|
146次组卷
|
2卷引用:2024届江西省南昌市高三下学期二模考试化学试题
9 . 下列说法正确的是
A.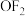 是由极性键构成的非极性分子 是由极性键构成的非极性分子 |
B.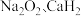 中均存在非极性键 中均存在非极性键 |
C. 中, 中, 提供空轨道, 提供空轨道, 提供孤对电子 提供孤对电子 |
D. 分子之间能形成氢键,因此 分子之间能形成氢键,因此 的热稳定性比 的热稳定性比 的强 的强 |
您最近半年使用:0次
7日内更新
|
195次组卷
|
2卷引用:河北省沧州市2024届普通高中高三下学期总复习质量监测(二模)化学试题
名校
解题方法
10 . 铬是人体内微量元素之一,是重要的血糖调节剂。
(1)铬在元素周期表中的位置为___________ ,其基态原子核外电子占据的原子轨道数为___________ 。
(2)已知 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。
①该配合物中提供孤电子对形成配位键的原子是___________ 。
②配体中中心原子的杂化方式为___________ (填字母)。
a. b.
b. c.sp d.
c.sp d.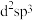
③该物质中, 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是___________ 。
(3)钛铬合金是一种高温结构材料,第二电离能
___________ (填“ ”或“
”或“ ”)
”)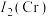 ,原因是
,原因是___________ 。
(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为 ,则B点分数坐标为
,则B点分数坐标为___________ ,已知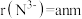 ,
,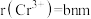 ,则AB间距离为
,则AB间距离为___________ nm。
(1)铬在元素周期表中的位置为
(2)已知
 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。①该配合物中提供孤电子对形成配位键的原子是
②配体中中心原子的杂化方式为
a.
 b.
b. c.sp d.
c.sp d.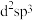
③该物质中,
 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是(3)钛铬合金是一种高温结构材料,第二电离能

 ”或“
”或“ ”)
”)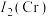 ,原因是
,原因是(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为
 ,则B点分数坐标为
,则B点分数坐标为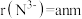 ,
,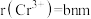 ,则AB间距离为
,则AB间距离为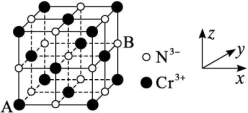
您最近半年使用:0次