名校
解题方法
1 . 碱金属氯化物是典型的离子化合物,NaCl和CsCl的晶胞结构如图所示。其中的碱金属离子能够与冠醚形成超分子。

A.NaCl晶胞中a为 |
B.CsCl晶体中 周围紧邻8个 周围紧邻8个 |
| C.熔点:NaCl<CsCl |
| D.不同空穴尺寸的冠醚可以对不同碱金属离子进行识别 |
您最近一年使用:0次
名校
解题方法
2 .  是一种典型的配合物,下列有关说法中正确的是
是一种典型的配合物,下列有关说法中正确的是
 是一种典型的配合物,下列有关说法中正确的是
是一种典型的配合物,下列有关说法中正确的是A.基态N原子的轨道表示式为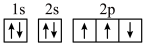 |
| B.第一电离能大小顺序:N>S>O |
C.1mol  中含有12mol共价键 中含有12mol共价键 |
D.N原子和S原子的杂化方式都为 杂化 杂化 |
您最近一年使用:0次
名校
3 . 根据下列实验操作和现象,得出的相应结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 用铂丝蘸取少量某溶液进行焰色试验 | 有黄色火焰,透过蓝色钴玻璃观察到紫色火焰 | 溶液中含有钠盐和钾盐 |
B | 向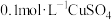 溶液中加入 溶液中加入 固体 固体 | 溶液由蓝色变为黄绿色 | 存在转化: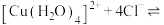 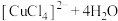 |
C | 向 溶液中滴加稀盐酸溶液 溶液中滴加稀盐酸溶液 | 有白色胶状沉淀 | 非金属性: |
D | 将铁锈溶于浓盐酸,滴入 溶液 溶液 | 紫红色褪去 | 铁锈中含有二价铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-04更新
|
251次组卷
|
3卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
4 . 常温下向 的混合液中滴加
的混合液中滴加 溶液,混合液中
溶液,混合液中 与
与 的关系如图所示,
的关系如图所示, 或
或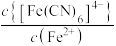 或
或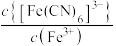 。下列叙述正确的是
。下列叙述正确的是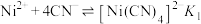 ;
;
② ;
;
③ ,且
,且 。
。
 的混合液中滴加
的混合液中滴加 溶液,混合液中
溶液,混合液中 与
与 的关系如图所示,
的关系如图所示, 或
或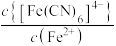 或
或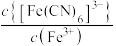 。下列叙述正确的是
。下列叙述正确的是
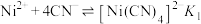 ;
;②
 ;
;③
 ,且
,且 。
。A.直线a代表 与 与 的关系 的关系 |
B.平衡常数 的数量级为 的数量级为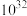 |
C.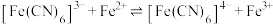 不易发生 不易发生 |
D.向含相同浓度的 和 和 的溶液中滴加 的溶液中滴加 溶液,先生成 溶液,先生成 |
您最近一年使用:0次
2024-06-04更新
|
210次组卷
|
3卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
解题方法
5 . 根据实验目的设计方案并进行实验,下列有关方案设计、实验现象或结论都正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 比较Cu和Fe的金属性强弱 | 取同浓度的① 、② 、② 溶液,滴加同浓度氨水 溶液,滴加同浓度氨水 | ①先沉淀后溶解,②沉淀后不溶解 | 金属性:Cu<Fe |
| B | 检验己烯中的碳碳双键 | 取少量己烯,加入溴的四氯化碳溶液,振荡 | 上下两层均无色 | 己烯中含碳碳双键 |
| C | 比较配离子的稳定性 | 向盛有少量蒸馏水的试管里加2滴 ,然后再加2滴硫氰化钾溶液 ,然后再加2滴硫氰化钾溶液 | 溶液由黄色变血红色 |  与 与 形成的配离子更稳定 形成的配离子更稳定 |
| D | 比较温度对反应速率的影响 | 将2mL 0.1mol/L  溶液(A)浸入0℃水浴中、2mL 0.05mol/L 溶液(A)浸入0℃水浴中、2mL 0.05mol/L  溶液(B)浸入50℃水浴中,再同时滴加0.1mol/L稀硫酸2mL 溶液(B)浸入50℃水浴中,再同时滴加0.1mol/L稀硫酸2mL | B溶液比A溶液先出现浑浊 | 温度越高,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-04更新
|
359次组卷
|
2卷引用:重庆市部分学校2024年高三下学期考前最后一卷化学试题
解题方法
6 . CO2可被催化还原为HCOOH、CH3OH和CO等,下列说法错误的是
| A.CH3OH中C—O—H键角为109°28' |
| B.CO分子内存在轴对称的电子云 |
| C.CO2中的C原子采取sp杂化 |
| D.HCOOH分子间可形成氢键 |
您最近一年使用:0次
名校
7 . 某硫酸盐的阳离子结构如下所示,X、Y、Z均为短周期主族元素,原子序数依次增大,W的单质为红色固体,1mol该阳离子含有95mol电子。下列叙述错误的是
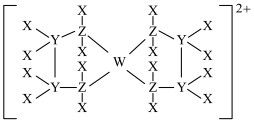
| A.原子半径:Y>Z | B.非金属性:X<Z |
| C.W的原子最外层电子数为1 | D.Z的氧化物均为无色气体 |
您最近一年使用:0次
名校
解题方法
8 . 铁及其化合物在生活、生产中有重要应用。回答下列问题:
(1)乳酸亚铁 是一种常用的补铁剂。
是一种常用的补铁剂。
① 的价电子排布图为
的价电子排布图为___________ 。 可用于治疗急性心率衰竭。
可用于治疗急性心率衰竭。
①硝普钠中 的配位数为
的配位数为___________ 。
②硝普钠中不存在的化学键有___________ (填序号)。
a.离子键 b.金属键 c. 配位键 d.极性共价键
(3)咔唑 (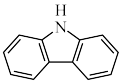 ),)用于制备靶向Fe2+荧光探针,咔唑沸点比
),)用于制备靶向Fe2+荧光探针,咔唑沸点比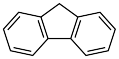 高的主要原因是
高的主要原因是___________ ,咔唑分子中所有原子共平面,咔唑与  都能与
都能与  配位,配位能力: 咔唑
配位,配位能力: 咔唑___________ 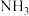 (填"> "、"<"、"=")。
(填"> "、"<"、"=")。
(4)由铁、钾、硒形成的一种超导材料,其晶胞结构和xy平面投影如图所示。___________ 。
②该晶胞参数分别为 a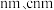 ,该晶体密度
,该晶体密度
___________ 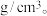 ( 用
( 用  表示阿伏加德罗常数 )
表示阿伏加德罗常数 )
(1)乳酸亚铁
 是一种常用的补铁剂。
是一种常用的补铁剂。①
 的价电子排布图为
的价电子排布图为②乳酸分子( )中
)中  键与
键与  键的数目之比为
键的数目之比为
 可用于治疗急性心率衰竭。
可用于治疗急性心率衰竭。①硝普钠中
 的配位数为
的配位数为②硝普钠中不存在的化学键有
a.离子键 b.金属键 c. 配位键 d.极性共价键
(3)咔唑 (
 ),)用于制备靶向Fe2+荧光探针,咔唑沸点比
),)用于制备靶向Fe2+荧光探针,咔唑沸点比 高的主要原因是
高的主要原因是 都能与
都能与  配位,配位能力: 咔唑
配位,配位能力: 咔唑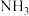 (填"> "、"<"、"=")。
(填"> "、"<"、"=")。(4)由铁、钾、硒形成的一种超导材料,其晶胞结构和xy平面投影如图所示。

②该晶胞参数分别为 a
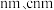 ,该晶体密度
,该晶体密度
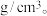 ( 用
( 用  表示阿伏加德罗常数 )
表示阿伏加德罗常数 )
您最近一年使用:0次
9 . 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为 2 。元素 基态原子的
基态原子的 轨道上有4个电子。元素
轨道上有4个电子。元素 的原子最外层电子数是其内层电子数的3倍。元素
的原子最外层电子数是其内层电子数的3倍。元素 的原子核外电子的运动状态有5种,
的原子核外电子的运动状态有5种, 和
和 位于同一周期,且
位于同一周期,且 的原子半径在同周期主族元素中最小。
的原子半径在同周期主族元素中最小。
(1)Z的基态原子电子排布式为___________ 。
(2)上述非金属元素中电负性最小的是(填元素符号)___________ 。
(3) 分子的空间构型为
分子的空间构型为___________ ,属于___________ (填“极性”或”非极性”)分子;该分子易与 离子结合形成
离子结合形成 ,
, 中
中 的杂化轨道类型为
的杂化轨道类型为___________ 。
(4)化合物XY是一种优良的宽带隙半导体锂离子电池负极材料。在充电过程中,负极材料晶胞的组成变化如图所示。 位于周期表
位于周期表___________ 区。
②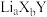 中,a:b=
中,a:b=___________ 。
 基态原子的
基态原子的 轨道上有4个电子。元素
轨道上有4个电子。元素 的原子最外层电子数是其内层电子数的3倍。元素
的原子最外层电子数是其内层电子数的3倍。元素 的原子核外电子的运动状态有5种,
的原子核外电子的运动状态有5种, 和
和 位于同一周期,且
位于同一周期,且 的原子半径在同周期主族元素中最小。
的原子半径在同周期主族元素中最小。(1)Z的基态原子电子排布式为
(2)上述非金属元素中电负性最小的是(填元素符号)
(3)
 分子的空间构型为
分子的空间构型为 离子结合形成
离子结合形成 ,
, 中
中 的杂化轨道类型为
的杂化轨道类型为(4)化合物XY是一种优良的宽带隙半导体锂离子电池负极材料。在充电过程中,负极材料晶胞的组成变化如图所示。

 位于周期表
位于周期表②
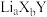 中,a:b=
中,a:b=
您最近一年使用:0次
名校
解题方法
10 . X、Y、Z、W是原子序数依次增大的短周期主族元素,其中W的最外层电子数是次外层电子数的3倍,由X、Y、Z、W四种元素形成的离子化合物G结构如下,下列有关说法不正确的是
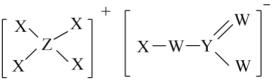
| A.X与Y、Z、W均能形成10电子化合物 |
| B.上述阳离子里没有配位键 |
| C.简单氢化物的沸点:Y<Z<W |
| D.X与Y形成的化合物可能是非极性分子 |
您最近一年使用:0次




