名校
1 . 吡啶(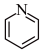 )类似于芳香化合物,化合物(Ⅲ)为吡啶类杂环有机物,可用作医药中间体,其合成路线如图,下列说法不正确的是
)类似于芳香化合物,化合物(Ⅲ)为吡啶类杂环有机物,可用作医药中间体,其合成路线如图,下列说法不正确的是
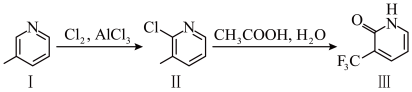
 )类似于芳香化合物,化合物(Ⅲ)为吡啶类杂环有机物,可用作医药中间体,其合成路线如图,下列说法不正确的是
)类似于芳香化合物,化合物(Ⅲ)为吡啶类杂环有机物,可用作医药中间体,其合成路线如图,下列说法不正确的是
| A.在水中溶解度:吡啶>苯 |
| B.吡啶和化合物I互为同系物 |
| C.氮原子上电子云密度:化合物I<吡啶 |
| D.C-N-C键角:物质Ⅱ>物质Ⅲ |
您最近一年使用:0次
2 . 重氮化合物是一类活泼的化合物,在有机合成方面有着重要应用。重氮化合物A在光照及甲醇参与反应的条件下经过一系列活泼中间体转化为F的路线如下:
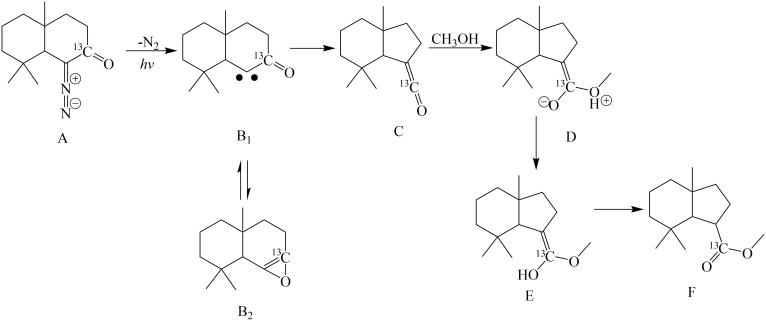
回答下列问题:
(1)为研究反应历程,A中的羰基上的碳原子用13C标记,这种研究方法称为___________ 。
(2)B1中的一个碳原子含有未共用电子对,易与B2相互转化或转化为C,B2的官能团名称为___________ ;上述路线中与B1、B2互为同分异构体的是___________ (填标号)。
(3)从结果上看,C和CH3OH生成E的反应类型为___________ ;写出CH2=C=O与CH3CH2OH反应的化学方程式___________ (不要求写出中间体)。
(4)E不稳定,能自发转化为F,说明稳定性C=O___________ C=C(填“大于”“小于”或“等于”),理由是___________ (从键参数的角度说明)。
(5)X、Y是二十多年前才发现的两种生物碱,在室温下可相互转化:
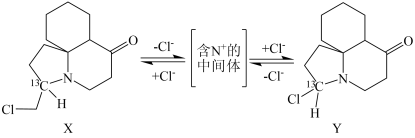
含N+的中间体的结构简式为____________

回答下列问题:
(1)为研究反应历程,A中的羰基上的碳原子用13C标记,这种研究方法称为
(2)B1中的一个碳原子含有未共用电子对,易与B2相互转化或转化为C,B2的官能团名称为
(3)从结果上看,C和CH3OH生成E的反应类型为
(4)E不稳定,能自发转化为F,说明稳定性C=O
(5)X、Y是二十多年前才发现的两种生物碱,在室温下可相互转化:

含N+的中间体的结构简式为
您最近一年使用:0次
解题方法
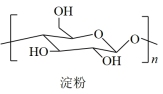
3 . 2021年我国首次实现从 到淀粉的全合成,其部分合成路线如下:
到淀粉的全合成,其部分合成路线如下:
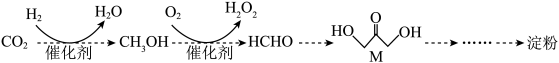
设 为阿伏加德罗常数的值。下列说法不正确的是
为阿伏加德罗常数的值。下列说法不正确的是
 到淀粉的全合成,其部分合成路线如下:
到淀粉的全合成,其部分合成路线如下: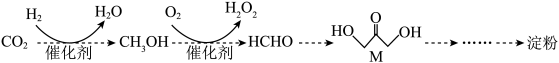
设
 为阿伏加德罗常数的值。下列说法不正确的是
为阿伏加德罗常数的值。下列说法不正确的是A.甲醛分子中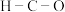 键角大于甲醇分子中 键角大于甲醇分子中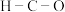 键角 键角 |
B.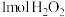 含有的电子数为 含有的电子数为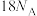 |
C. 与M的混合物中所含氧原子数为 与M的混合物中所含氧原子数为 |
D.淀粉与纤维素均可用 来表示,二者互为同分异构体 来表示,二者互为同分异构体 |
您最近一年使用:0次
2023·全国·模拟预测
解题方法
4 . 聚四氟乙烯具有耐热、耐酸碱腐蚀等优异的性能,用途广泛,有“塑料王”之称,其合成路线如图。
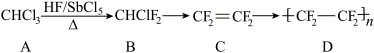
下列说法错误的是
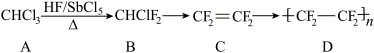
下列说法错误的是
| A.图中合成路线中涉及的碳原子杂化类型有2种 |
| B.由化合物C到化合物D的反应符合原子经济性要求 |
C. (共价化合物)中Sb的价层电子对数为5 (共价化合物)中Sb的价层电子对数为5 |
| D.H—F键的键能比H—Cl键大,所以HF的酸性强于HCl |
您最近一年使用:0次
解题方法
5 . 氯化亚砜(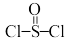 )常用作脱水剂和氯化剂。如图流程表示其制备及用途,回答下列问题:
)常用作脱水剂和氯化剂。如图流程表示其制备及用途,回答下列问题:
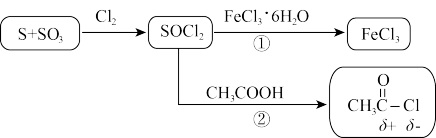
(1)用硫磺、氯气和三氧化硫为原料,在一定条件下可合成SOCl2,原子利用率达100%。写出该反应方程式______ 。
(2)下列有关说法不正确 的是______ 。
(3)途径②除了CH3COCl外还产生两种酸性气体,写出该反应方程式______ 。
(4)SOCl2极易水解,试从共价键的极性角度分析其原因______ 。
(5)途径①可能发生氧化还原反应而生成副产物,设计实验分别检验氧化产物和还原产物的存在______ 。
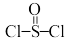 )常用作脱水剂和氯化剂。如图流程表示其制备及用途,回答下列问题:
)常用作脱水剂和氯化剂。如图流程表示其制备及用途,回答下列问题:
(1)用硫磺、氯气和三氧化硫为原料,在一定条件下可合成SOCl2,原子利用率达100%。写出该反应方程式
(2)下列有关说法
| A.SO3是极性分子,容易与H2O发生反应 |
| B.途径①能制得无水FeCl3是因为SOCl2吸水性强且产物HCl能抑制Fe3+水解 |
C.FeCl3在溶液中分步水解,第一步反应为:Fe3++H2O Fe(OH)2++H+ Fe(OH)2++H+ |
| D.CH3COCl能与NH3反应生成乙酰胺 |
(4)SOCl2极易水解,试从共价键的极性角度分析其原因
(5)途径①可能发生氧化还原反应而生成副产物,设计实验分别检验氧化产物和还原产物的存在
您最近一年使用:0次
6 . 2021年9月24日《科学》杂志发表了我国科学家的原创性重大突破,首次在实验室实现从CO2到淀粉的全合成。其合成路线如下:
CO2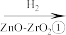 CH3OH
CH3OH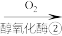
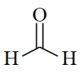
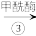
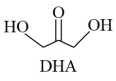
下列说法错误的是
CO2
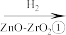 CH3OH
CH3OH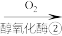



下列说法错误的是
| A.电负性:O>C>H>Zn |
| B.甲醇分子中H-C-O键角小于甲醛分子中H-C-O键角 |
| C.DHA分子间存在氢键 |
| D.Zn溶于氨水形成配合物[Zn(NH3)4](OH)2,Zn2+的配位数为6 |
您最近一年使用:0次
2022-03-04更新
|
946次组卷
|
3卷引用:山东省潍坊市2022届高三普通高等学校招生全国统一考试(一模)化学试题
山东省潍坊市2022届高三普通高等学校招生全国统一考试(一模)化学试题(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)新疆石河子第一中学2021-2022学年高二4月月考化学试题
解题方法
7 . 羟胺 是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成
是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成 和
和 ,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。
,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。
已知: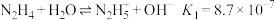 ;
;
 。
。
下列有关说法正确的是
 是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成
是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成 和
和 ,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。
,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。已知:
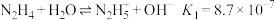 ;
; 。
。下列有关说法正确的是
| A.羟胺的碱性比氨强 |
B.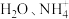 与 与 的VSEPR模型相同 的VSEPR模型相同 |
| C.羟胺极易溶于水主要原因是形成分子内氢键 |
D. 大小: 大小: |
您最近一年使用:0次
名校
解题方法
8 . 中国科学家在国际上首次实现了 到淀粉的合成,不依赖植物光合作用,原料只需
到淀粉的合成,不依赖植物光合作用,原料只需 、
、 比和电,相关成果发表在《科学》上。回答下列问题:
比和电,相关成果发表在《科学》上。回答下列问题:
(1) 的空间结构为
的空间结构为_______ 形,基态碳原子的价电子排布式为_______ 。
(2)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是_______ 。(用离子方程式表示)。
(3)淀粉在一定条件下可水解成葡萄糖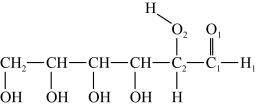 ,葡萄糖分子中键角
,葡萄糖分子中键角
_______ 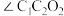 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)①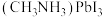 ,的晶胞结构如图所示:
,的晶胞结构如图所示:

其中B代表 。则
。则_______ 代表 ,原子分数坐标A为
,原子分数坐标A为 ,B为
,B为 ,则C的原子分数坐标为
,则C的原子分数坐标为_______ 。
②已知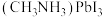 的摩尔质量为M
的摩尔质量为M  ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为_______  。该晶胞沿体对角线方向的投影图为
。该晶胞沿体对角线方向的投影图为_______ (填选项字母)。
a. b.
b. 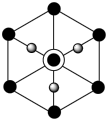 c.
c.  d.
d.
 到淀粉的合成,不依赖植物光合作用,原料只需
到淀粉的合成,不依赖植物光合作用,原料只需 、
、 比和电,相关成果发表在《科学》上。回答下列问题:
比和电,相关成果发表在《科学》上。回答下列问题:(1)
 的空间结构为
的空间结构为(2)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是
(3)淀粉在一定条件下可水解成葡萄糖
 ,葡萄糖分子中键角
,葡萄糖分子中键角
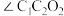 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)①
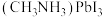 ,的晶胞结构如图所示:
,的晶胞结构如图所示:
其中B代表
 。则
。则 ,原子分数坐标A为
,原子分数坐标A为 ,B为
,B为 ,则C的原子分数坐标为
,则C的原子分数坐标为②已知
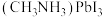 的摩尔质量为M
的摩尔质量为M  ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。该晶胞沿体对角线方向的投影图为
。该晶胞沿体对角线方向的投影图为a.
 b.
b.  c.
c.  d.
d.
您最近一年使用:0次
解题方法
9 . 我国是率先掌握通过非线性光学晶体( KBBF)变频来获得深紫外激光技术的国家,KBF4是合成KBBF的主要原料,高温下分解为KF和BF3。
(1)灼烧钾及其化合物时,会产生特殊的焰色,这是由于钾元素的核外电子由_______ ( 填“激发态”或“基态”)跃迁到另一个状态时产生的光谱,该光谱属于_______ (填“发射”或“吸收”)光谱。
(2)离子晶体KF的晶格能(气态离子形成1 mol离子晶体释放的能量)可通过Bom-Haber循环计算得到:

①KF的晶格能为_______ kJ·mol-1。
②已知:气态非金属原子获得1个电子形成气态阴离子所释放的能量叫该原子的第一亲和能,则F原子的第一亲和能为_______ kJ·mol-1,试解释同周期元素第一亲和能F>O>C>N的原因:_______ 。
(3)BF3、NH3和PH3分子中键角由大到小的顺序为_______ 。
(4)已知BF3中存在π键,则BF3中B- F键的键长_______ (填“大于”“小于”或“等于”)  中B-F键的键长;
中B-F键的键长; 的中心原子的轨道杂化类型是
的中心原子的轨道杂化类型是_______ 。
(5)KF晶体的晶胞与NaCl相似,若K+按ABCACB……方式堆积,则F-占据的是K+围成的_______ 空隙(填几何空间构型) ,每个K+周围紧邻的K+个数为_______ 。设 NA为阿伏加德罗常数的值,KF晶体的密度为ρg·cm-3,则K+与K+的最短距离为_______ pm(用含ρ、NA的代数式表示)。
(1)灼烧钾及其化合物时,会产生特殊的焰色,这是由于钾元素的核外电子由
(2)离子晶体KF的晶格能(气态离子形成1 mol离子晶体释放的能量)可通过Bom-Haber循环计算得到:

①KF的晶格能为
②已知:气态非金属原子获得1个电子形成气态阴离子所释放的能量叫该原子的第一亲和能,则F原子的第一亲和能为
(3)BF3、NH3和PH3分子中键角由大到小的顺序为
(4)已知BF3中存在π键,则BF3中B- F键的键长
 中B-F键的键长;
中B-F键的键长; 的中心原子的轨道杂化类型是
的中心原子的轨道杂化类型是(5)KF晶体的晶胞与NaCl相似,若K+按ABCACB……方式堆积,则F-占据的是K+围成的
您最近一年使用:0次
名校
10 . 铜及其化合物有广泛的用途。回答下列问题:
(1)同周期元素中,与Cu最外层电子数相同的元素还有___________ 种。
(2)往 中逐滴加入氨水至沉淀恰好溶解,将该溶液冷却结晶,得到蓝色晶体。
中逐滴加入氨水至沉淀恰好溶解,将该溶液冷却结晶,得到蓝色晶体。
①该晶体中各元素电负性由大到小顺序为___________ ;
②该晶体中不存在的作用力为___________ 。
A.离子键 B.氢键 C.金属键 D.σ键 E.范德华力 F.配位键
③已知 分子中键角为107°,则上述晶体中氮氢之间的键角
分子中键角为107°,则上述晶体中氮氢之间的键角___________ 107°(填选项标号)。
A.大于 B.小于 C.等于 D.无法确定
(3)已知铜的某些化合物的熔点如表所示。三者熔点出现差异的原因是:___________ 。
(4)溴化亚铜(CuBr)常用作有机合成原料和反应催化剂,其晶胞结构如下图所示。

已知①、②号铜原子坐标分数依次为(0,0,0)、( ,
, ,0),则③号溴原子的坐标分数为
,0),则③号溴原子的坐标分数为_______ ;设CuBr的密度为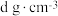 ,
, ,
, 为阿伏加德罗常数,则Cu原子与Br原子的核间距离为
为阿伏加德罗常数,则Cu原子与Br原子的核间距离为________ cm(用含a、d、 的代数式表示)。
的代数式表示)。
(1)同周期元素中,与Cu最外层电子数相同的元素还有
(2)往
 中逐滴加入氨水至沉淀恰好溶解,将该溶液冷却结晶,得到蓝色晶体。
中逐滴加入氨水至沉淀恰好溶解,将该溶液冷却结晶,得到蓝色晶体。①该晶体中各元素电负性由大到小顺序为
②该晶体中不存在的作用力为
A.离子键 B.氢键 C.金属键 D.σ键 E.范德华力 F.配位键
③已知
 分子中键角为107°,则上述晶体中氮氢之间的键角
分子中键角为107°,则上述晶体中氮氢之间的键角A.大于 B.小于 C.等于 D.无法确定
(3)已知铜的某些化合物的熔点如表所示。三者熔点出现差异的原因是:
| CuO | CuS | CuSe | |
| 熔点(℃) | 1326 | 220 | 387 |
(4)溴化亚铜(CuBr)常用作有机合成原料和反应催化剂,其晶胞结构如下图所示。

已知①、②号铜原子坐标分数依次为(0,0,0)、(
 ,
, ,0),则③号溴原子的坐标分数为
,0),则③号溴原子的坐标分数为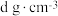 ,
, ,
, 为阿伏加德罗常数,则Cu原子与Br原子的核间距离为
为阿伏加德罗常数,则Cu原子与Br原子的核间距离为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2022-03-05更新
|
489次组卷
|
2卷引用:福建省龙岩市2022届高三下学期第一次教学质量检测化学试题



