名校
解题方法
1 . 下列对物质性质解释合理的是
| 选项 | 性质 | 解释 |
| A | 酸性: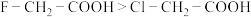 | 电负性:F>Cl |
| B | 熔点:晶体硅<碳化硅 | 碳化硅中分子间作用力较大 |
| C | 热稳定性: | HF中存在氢键 |
| D | 熔点: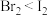 | Br-Br键较强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-13更新
|
326次组卷
|
3卷引用:北京市汇文中学2023-2024学年高二上学期期末化学试题
名校
2 . 多杂原子—氢键桥接电子传递途径赋予了超分子催化体系很高的光催化性能,有机物 和
和 配合物形成的超分子催化体系的局部结构如图所示。下列说法错误的是
配合物形成的超分子催化体系的局部结构如图所示。下列说法错误的是

 和
和 配合物形成的超分子催化体系的局部结构如图所示。下列说法错误的是
配合物形成的超分子催化体系的局部结构如图所示。下列说法错误的是
A.与 同周期且未成对电子数相同的元素还有3种 同周期且未成对电子数相同的元素还有3种 |
B.每个配体与 形成2个配位键 形成2个配位键 |
| C.①和②处氮原子杂化方式相同 |
D.①处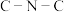 键夹角小于③处 键夹角小于③处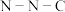 键夹角 键夹角 |
您最近一年使用:0次
2024-02-13更新
|
248次组卷
|
2卷引用:河北省沧州市泊头市部分学校2023-2024学年高三上学期12月月考化学试题
名校
3 . 已知S4O 的结构为
的结构为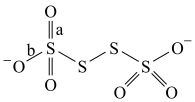 ,下列叙述不正确的是
,下列叙述不正确的是
 的结构为
的结构为 ,下列叙述不正确的是
,下列叙述不正确的是| A.基态S原子核外电子的空间运动状态有9种 |
B.S4O 的结构中,中间的两个S原子均有两对孤对电子 的结构中,中间的两个S原子均有两对孤对电子 |
C.S4O 的结构中a、b为键长,则a<b 的结构中a、b为键长,则a<b |
D.沸点: > > |
您最近一年使用:0次
解题方法
4 . 液氨可以微弱的电离产生 和
和 ,是一种很好的溶剂。下列有关说法正确的是
,是一种很好的溶剂。下列有关说法正确的是
 和
和 ,是一种很好的溶剂。下列有关说法正确的是
,是一种很好的溶剂。下列有关说法正确的是| A.NH2OH 难溶于水 | B.NH 的空间构型为直线形 的空间构型为直线形 |
C.NH3的键角比NH 中的大 中的大 | D.1 mol [Cu(NH3)4]2⁺中含有4 mol σ键 |
您最近一年使用:0次
名校
5 . 下列性质与解释中错误的是
| 选项 | 性质 | 解释 |
| A | 键角: |  、 、 的杂化方式相同,但 的杂化方式相同,但 上含孤电子对 上含孤电子对 |
| B | 稳定性: |  中含氢键 中含氢键 |
| C | 熔点: ( (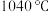 )远高于 )远高于 ( (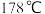 升华) 升华) |  为离子晶体, 为离子晶体, 为分子晶体 为分子晶体 |
| D | 酸性: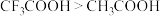 |  电负性更大使羟基极性变强 电负性更大使羟基极性变强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 硅、锗(Ge)、镓及其化合物广泛应用于光电材料领域。请回答:
(1)比较硅与锗的第一电离能大小:Si___________ (填“>”或“<”)Ge。
(2)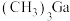 分子是
分子是___________ (填“极性”或“非极性”)分子。
(3)氮化硅( )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且最外层均达到8电子稳定结构,比较晶体结构中键角大小:
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且最外层均达到8电子稳定结构,比较晶体结构中键角大小:
___________ (填“>”“<”“=”) 。
。

(4)GaAs的熔点为1238℃,其晶胞结构如图所示,该晶体中Ga和As以___________ 键结合,Ga的配位数为________ 。若GaAs晶胞边长为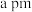 ,则Ga与最近As的核间距为
,则Ga与最近As的核间距为_________ pm。

(1)比较硅与锗的第一电离能大小:Si
(2)
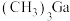 分子是
分子是(3)氮化硅(
 )是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且最外层均达到8电子稳定结构,比较晶体结构中键角大小:
)是一种耐磨损、耐高温的结构陶瓷材料,其部分空间结构如图所示,其结构中每个原子杂化类型相同且最外层均达到8电子稳定结构,比较晶体结构中键角大小:
 。
。
(4)GaAs的熔点为1238℃,其晶胞结构如图所示,该晶体中Ga和As以
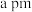 ,则Ga与最近As的核间距为
,则Ga与最近As的核间距为
您最近一年使用:0次
名校
解题方法
7 . 下列实验事实的理论解释不正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 磷原子的第一电离能大于硫原子 | 磷原子3p能级半充满 |
| B |  分子在水中有一定溶解度 分子在水中有一定溶解度 |  与水分子极性上相似 与水分子极性上相似 |
| C | 浓 溶液显绿色,加水稀释过程中变蓝 溶液显绿色,加水稀释过程中变蓝 |  与 与 、 、 均能形成配合物 均能形成配合物 |
| D | 石墨比金刚石熔点高 | 金刚石碳碳键键能更小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-08更新
|
105次组卷
|
2卷引用:吉林省长春吉大附中实验学校2023-2024学年高二上学期1月期末化学试题
名校
解题方法
8 . DNA中四种碱基间的配对方式如图。以下说法不正确的是


| A.配对碱基间的作用力属于共价键 |
| B.碱基中元素第一电离能大小关系为N>O>C |
| C.鸟嘌呤与胞嘧啶之间的相互作用比腺嘌呤与胸腺嘧啶之间的更强 |
| D.若图中①②分别代表不同化学键,则键能:②<① |
您最近一年使用:0次
名校
解题方法
9 . 某种离子液体的结构如图所示,X、Y、Z、M、Q为原子序数依次增大的五种短周期非金属元素,Z的原子序数等于X、Y原子序数之和,Q为非金属性最强的元素。

A. 的键角大于 的键角大于 的键角 的键角 | B.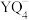 的VSEPR模型为正四面体形 的VSEPR模型为正四面体形 |
C.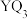 是极性分子, 是极性分子, 是非极性分子 是非极性分子 | D.M2的键能小于Q2的键能 |
您最近一年使用:0次
2024-02-08更新
|
148次组卷
|
2卷引用:吉林省长春吉大附中实验学校2023-2024学年高二上学期1月期末化学试题
名校
10 . 2020年11月24日4时30分,长征五号遥五运载火箭在中国文昌航天发射场点火升空,将嫦娥五号月球探测器运送至地月转移轨道,开启我国首次地外天体采样返回之旅。月球的沙土中含有丰富的钛铁矿,土壤中还含有硅、铝、钾、钡、钴、铷、汞、铜和稀土元素等。
(1)钛在元素周期表中的位置是___________ ,与Ti处于同周期、未成对电子数与Ti相同的元素还有___________ 种。
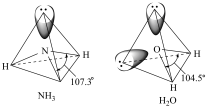
(2)[Cu(NH3)4]SO4·H2O是一种蓝色晶体,其中的NH3、H2O的空间结构和相应的键角如图所示,H2O的键角比NH3小的原因是___________ 。
(3)基态铁原子的价层电子排布图为___________ 。相同条件下,Fe3+和Fe2+相比,___________ 更稳定,原因是___________ 。
(4)某钙钛矿的晶体结构属于立方结构,具有高度的对称性,其晶胞结构如图所示。
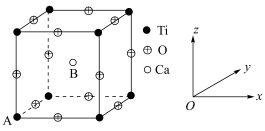
①在该晶体中每个钛离子周围与它最近且距离相等的钛离子有___________ 个。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。晶胞中A的原子分数坐标为(0,0,0),则B(Ca)的原子分数坐标为___________ 。
(1)钛在元素周期表中的位置是
(2)[Cu(NH3)4]SO4·H2O是一种蓝色晶体,其中的NH3、H2O的空间结构和相应的键角如图所示,H2O的键角比NH3小的原因是

(3)基态铁原子的价层电子排布图为
(4)某钙钛矿的晶体结构属于立方结构,具有高度的对称性,其晶胞结构如图所示。

①在该晶体中每个钛离子周围与它最近且距离相等的钛离子有
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。晶胞中A的原子分数坐标为(0,0,0),则B(Ca)的原子分数坐标为
您最近一年使用:0次



