1 . 洲际弹道导弹DF—31A的制造材料中包含了Fe、Cr、Ni、C等多种元素。
(1)基态铁原子的价电子排布式为___________ ,Cr的未成对电子个数___________ ,Ni位于周期表的___________ 区。
(2)Fe、Co均能与CO形成配合物,如Fe(CO)5、Co2(CO)8,其结构分别如图1、图2所示,

则Fe(CO)5中σ键与π键的个数比___________ ,图2中C的杂化方式有___________ ,形成上述两种化合物的四种元素中电负性最大的是___________ (填元素符号),写出一种与CO互为等电子体的分子___________ 。
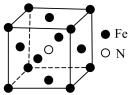
(3)铁与氮形成的化合物的立方晶胞结构如图所示,N位于有Fe构成的___________ 的体心(填“正四面体”或“八面体”或“立方体”),若晶体密度为b ,则顶点Fe与N的距离为
,则顶点Fe与N的距离为__________ pm。(用含NA、b的代数式表示,NA为阿伏加德罗常数的值)
(1)基态铁原子的价电子排布式为
(2)Fe、Co均能与CO形成配合物,如Fe(CO)5、Co2(CO)8,其结构分别如图1、图2所示,

则Fe(CO)5中σ键与π键的个数比
(3)铁与氮形成的化合物的立方晶胞结构如图所示,N位于有Fe构成的
 ,则顶点Fe与N的距离为
,则顶点Fe与N的距离为
您最近一年使用:0次
2 . 铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)基态Cu原子的价电子排布式为_______ ;在周期表中,Cu元素属于_______ 区。
(2)往硫酸铜溶液中加入氨水,先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色透明溶液,写出沉淀溶解的离子方程式:_______ 。
(3)1mol[Cu(H2O)4]2+中含有σ键的数目为_______ 。
(4)[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl—取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_______ ,其结构可用示意图表示为_______ 。
(1)基态Cu原子的价电子排布式为
(2)往硫酸铜溶液中加入氨水,先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色透明溶液,写出沉淀溶解的离子方程式:
(3)1mol[Cu(H2O)4]2+中含有σ键的数目为
(4)[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl—取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
您最近一年使用:0次
名校
3 . 中科院大连物化所成功利用具有尖晶石结构的Co3O4电催化剂电解水。
(1)Co在周期表中的位置是____ ,基态Co的电子占据的最高能层符号为____ 。
(2)钴盐引发动物中毒时,通常可以用EDTA(结构如图)解毒。其中,N的杂化方式均为____ ,N的I1(第一电离能)大于O的I1,其原因是____ ;自由基是指含单电子的基团,1mol—COOH(羧基自由基)中存在____ molσ键和____ molπ键。

(3)EDTA可以由乙二胺与甲醛、氰化钠间接得到。离子化合物氰化钠的晶体类型为____ ,甲醛分子的空间构型为____ 。
(4)Co3O4晶体中O作面心立方最密堆积(如图),Co随机填充在晶胞中O构成的8个四面体空隙和4个八面体空隙中,则Co的配位数分别为____ ,Co总的空隙填充率为____ ,如果晶胞边长为anm,Co3O4的摩尔质量为Mg/mol,NA为阿伏加德罗常数的值,则Co3O4的晶体密度为____ g/cm3(列出计算式)。

(1)Co在周期表中的位置是
(2)钴盐引发动物中毒时,通常可以用EDTA(结构如图)解毒。其中,N的杂化方式均为

(3)EDTA可以由乙二胺与甲醛、氰化钠间接得到。离子化合物氰化钠的晶体类型为
(4)Co3O4晶体中O作面心立方最密堆积(如图),Co随机填充在晶胞中O构成的8个四面体空隙和4个八面体空隙中,则Co的配位数分别为

您最近一年使用:0次
2022-03-26更新
|
383次组卷
|
3卷引用:四川省遂宁市2022届高三第二次诊断性考试(二模)理综化学试题
名校
解题方法
4 . 第三代半导体材料氮化镓(GaN)适合于制作高温、高频、抗辐射及大功率器件,通常称为高温半导体材料。回答下列问题:
(1)基态Ga原子价层电子的轨道表达式为_______ ,第一电离能介于N和B之间的第二周期元素有_______ 种。
(2)HCN分子中σ键与π键的数目之比为_______ ,其中σ键的对称方式为______ 。与CN-互为等电子体的分子为__________ 。
(3)NaN3是汽车安全气囊中的主要化学成分,其中阴离子中心原子的杂化轨道类型为_________ ,NF3的空间构型为_________ 。
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如表所示,分析其变化原因_____________ 。
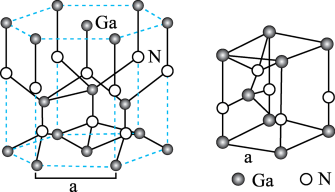
(5)GaN晶胞结构如图所示:晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为_________ ;
(1)基态Ga原子价层电子的轨道表达式为
(2)HCN分子中σ键与π键的数目之比为
(3)NaN3是汽车安全气囊中的主要化学成分,其中阴离子中心原子的杂化轨道类型为
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如表所示,分析其变化原因
| GaN | GaP | GaAs | |
| 熔点 | 1700℃ | 1480℃ | 1238℃ |
(5)GaN晶胞结构如图所示:晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为

您最近一年使用:0次
2019-09-09更新
|
171次组卷
|
2卷引用:四川省射洪县射洪中学2020届高三补习班上学期入学考试化学试题



