名校
解题方法
1 . 完成下列问题
(1)蓝矾(CuSO4 ·5H2O)的结构如图所示: 的立体构型是
的立体构型是___________ ,其中S原子的杂化轨道类型是___________ ;基态O原子的价电子排布图为___________ ;
(2)气态三氧化硫以单分子形式存在,其分子的立体构型为___________ 形;将纯液态SO3冷却到289. 8 K时凝固得到固体,其结构如图,固体三氧化硫中S原子的杂化轨道类型为___________ 。___________ ,中心原子的杂化方式为___________ 。
(4)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为___________ ,SnBr2分子中的键角___________ 120°(填“>”“<”或“=”)。
(5)元素A是形成有机物的主要元素,下列分子中碳原子采取sp和sp3杂化方式的是___________ 。
(1)蓝矾(CuSO4 ·5H2O)的结构如图所示:

 的立体构型是
的立体构型是(2)气态三氧化硫以单分子形式存在,其分子的立体构型为

(4)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为
(5)元素A是形成有机物的主要元素,下列分子中碳原子采取sp和sp3杂化方式的是
A. B.CH4 C.CH2=CHCH3 D.CH3CH2C≡CH E.CH3CH3
B.CH4 C.CH2=CHCH3 D.CH3CH2C≡CH E.CH3CH3
您最近一年使用:0次
2 . 2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟新方向。
(1)基态钛原子的核外电子排布式为_______ ,其中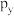 原子轨道上的电子数为
原子轨道上的电子数为_______ 个。
(2) 的配合物有多种。在
的配合物有多种。在 和
和 三种微粒的配体中,所含原子电负性由大到小的排序为
三种微粒的配体中,所含原子电负性由大到小的排序为_______ ; 含有
含有_______ 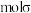 键;
键;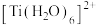 的配体中提供孤电子对的原子是
的配体中提供孤电子对的原子是_______ ; 中
中 的化合价是
的化合价是_______ ; 的球棍结构如图,
的球棍结构如图, 的配位数是
的配位数是_______ 。

(1)基态钛原子的核外电子排布式为
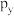 原子轨道上的电子数为
原子轨道上的电子数为(2)
 的配合物有多种。在
的配合物有多种。在 和
和 三种微粒的配体中,所含原子电负性由大到小的排序为
三种微粒的配体中,所含原子电负性由大到小的排序为 含有
含有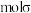 键;
键;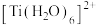 的配体中提供孤电子对的原子是
的配体中提供孤电子对的原子是 中
中 的化合价是
的化合价是 的球棍结构如图,
的球棍结构如图, 的配位数是
的配位数是
您最近一年使用:0次
名校
3 . I.A、B、C、D、E 为短周期元素且它们的原子序数依次增大,A 的核外电子总数与其周期数相同;其中D原子的 L电子层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的 L 电子层中未成对电子数与D相同,但有空轨道;D与E同族,请回答下列问题:
(1)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的电子式为____________ ,A分别与 B、C、D形成的共价化合物中既含有极性共价键,又含有非极性共价键的化合物是____________________ (填化学式,任意写出两种)。
(2)B的一种氢化物的相对分子质量是 26,其分子中σ键和π键的数目之比为____________ 。
(3)常温下,相同c(H+)的H2E溶液和硫酸溶液,稀释相同的倍数后的c(H+)前者与后者的关系_________ 。(“大于”、“小于”、“相等”)
Ⅱ.(1)在某温度(T ℃)的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x 与y 关系如图所示。

该温度下,水的离子积为_____ ,T ℃_______ 25℃(填“大于”“小于”或“等于”)。
(2)某温度下,纯水的c(H+)=2.0×10-7mol·L-1。在此温度下,某溶液中由水电离出的c(H+)=4.0×10-13 mol·L-1,则该溶液的pH可能是___________ 。(lg4≈0.6)
(1)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的电子式为
(2)B的一种氢化物的相对分子质量是 26,其分子中σ键和π键的数目之比为
(3)常温下,相同c(H+)的H2E溶液和硫酸溶液,稀释相同的倍数后的c(H+)前者与后者的关系
Ⅱ.(1)在某温度(T ℃)的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x 与y 关系如图所示。

该温度下,水的离子积为
(2)某温度下,纯水的c(H+)=2.0×10-7mol·L-1。在此温度下,某溶液中由水电离出的c(H+)=4.0×10-13 mol·L-1,则该溶液的pH可能是
您最近一年使用:0次
解题方法
4 . 贝壳、珍珠、方解石等主要成分均含有CaCO3,回答下列问题:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧碳酸钙时的焰色为_______ (填标号)。
A 黄色 B 红色 C 紫色 D 绿色
(2)CaCO3中三种元素第一电离能由小到大的顺序是__________ 。CaCO3中的化学键除了σ键外,还存在_________________ 。
(3)关于CO2和CO32-的下列说法正确的是__________ 。
a 两种微粒价层电子对数相同 b 两种微粒的中心原子均无孤电子对
c 键角:CO2>CO32- d 两种微粒的中心原子杂化方式相同
(4)难溶碳酸盐易分解,CaCO3、BaCO3热分解温度更高的是_____ ,原因是______ 。
(5)方解石的菱面体结构如图1,沿三次轴的俯视图为正六边形。方解石的六方晶胞结构如图2,晶胞底面为平行四边形,其较小夹角为60°,边长为a nm,晶胞高为c nm。

A点在俯视图中为a,则B点在俯视图中的位置为_________ (填字母)。方解石的六方晶胞中,Ca2+和CO32-个数比为___________ ;若阿伏加 德罗常数为NA,则该方解石的密度为________ g/cm3(列出计算式)。
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧碳酸钙时的焰色为
A 黄色 B 红色 C 紫色 D 绿色
(2)CaCO3中三种元素第一电离能由小到大的顺序是
(3)关于CO2和CO32-的下列说法正确的是
a 两种微粒价层电子对数相同 b 两种微粒的中心原子均无孤电子对
c 键角:CO2>CO32- d 两种微粒的中心原子杂化方式相同
(4)难溶碳酸盐易分解,CaCO3、BaCO3热分解温度更高的是
(5)方解石的菱面体结构如图1,沿三次轴的俯视图为正六边形。方解石的六方晶胞结构如图2,晶胞底面为平行四边形,其较小夹角为60°,边长为a nm,晶胞高为c nm。

A点在俯视图中为a,则B点在俯视图中的位置为
您最近一年使用:0次
解题方法
5 . (1)下列数据是对应物质的熔点(℃)
据此作出的下列判断中,错误的是_____ 。
A 铝的化合物晶体中不存在离子晶体
B 表中只有BCl3、干冰是分子晶体
C 同族元素的氧化物可形成不同类型的晶体
D 不同族元素的氧化物可形成不同类型的晶体
(2)SiO2晶体结构片断如图所示。SiO2晶体中Si原子数目和Si﹣O键数目的比例为_____ 。

通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
Si(s)+ O2(g)=SiO2(s),该反应的反应热△H=__________ 。
(3)单质铝晶体晶胞特征如图乙所示.则晶胞中铝原子的配位数为_____ ,晶胞中存在两种空隙,分别是___________ 、___________ 。

| NaCl | Na2O | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 801 | 920 | 1291 | 190 | -109 | 2073 | -57 | 1723 |
据此作出的下列判断中,错误的是
A 铝的化合物晶体中不存在离子晶体
B 表中只有BCl3、干冰是分子晶体
C 同族元素的氧化物可形成不同类型的晶体
D 不同族元素的氧化物可形成不同类型的晶体
(2)SiO2晶体结构片断如图所示。SiO2晶体中Si原子数目和Si﹣O键数目的比例为

通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
| 化学键 | Si-O | Si-Si | O=O |
| 键能/KJ•mol-1 | 460 | 176 | 498 |
Si(s)+ O2(g)=SiO2(s),该反应的反应热△H=
(3)单质铝晶体晶胞特征如图乙所示.则晶胞中铝原子的配位数为

您最近一年使用:0次



