1 . 、臭氧 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。
(1)基态铁原子有___________ 种空间运动状态不同的电子; 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ ; 的空间构型为
的空间构型为___________ (用文字描述); 为
为___________ 分子(填“极性”、“非极性”)。
(2)碘的四氯化碳溶液为紫红色,加入浓碘化钾水溶液,振荡后溶液紫色变浅,请用离子方程式说明原因___________ 。
(3)硫单质的常见形式为 ,其环状结构如图所示,
,其环状结构如图所示, 中含有
中含有___________  键。
键。 的熔点为1090℃,远高于
的熔点为1090℃,远高于 的192℃,由此可以判断铝氟之间的化学键为
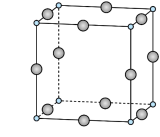
的192℃,由此可以判断铝氟之间的化学键为___________ 键。 结构属立方晶系,晶胞如图所示,
结构属立方晶系,晶胞如图所示, 的配位数为。若晶胞参数为
的配位数为。若晶胞参数为 ,晶体密度
,晶体密度
___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 在
在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 ,
, 也可在其他条件下被还原为
也可在其他条件下被还原为 。
。(1)基态铁原子有
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间构型为
的空间构型为 为
为(2)碘的四氯化碳溶液为紫红色,加入浓碘化钾水溶液,振荡后溶液紫色变浅,请用离子方程式说明原因
(3)硫单质的常见形式为
 ,其环状结构如图所示,
,其环状结构如图所示, 中含有
中含有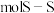 键。
键。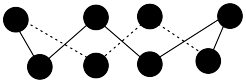
 的熔点为1090℃,远高于
的熔点为1090℃,远高于 的192℃,由此可以判断铝氟之间的化学键为
的192℃,由此可以判断铝氟之间的化学键为 结构属立方晶系,晶胞如图所示,
结构属立方晶系,晶胞如图所示, 的配位数为。若晶胞参数为
的配位数为。若晶胞参数为 ,晶体密度
,晶体密度
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解题方法
2 . 丁二酮肟( )是检验
)是检验 的灵敏试剂,在稀氨水介质中,
的灵敏试剂,在稀氨水介质中, 与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。

回答下列问题:
(1)Ni在元素周期表中的位置为_______ ;基态Ni中最外层电子所占据的原子轨道有_______ 个伸展方向。
(2)Ni与Ca位于同一周期且最外层电子数相同,单质Ni的熔点明显高于Ca,其原因是____ 。
(3)1mol丁二酮肟分子含有σ键数目为_______ ( 是阿伏加德罗常数的值)。
是阿伏加德罗常数的值)。
(4)丁二酮肟镍分子中C原子的杂化轨道类型有_______ ;元素N和O在周期表中相邻,元第一电离能 的原因是
的原因是_______ 。
(5)丁二酮肟镍分子内不存在的作用力有_______ (填序号)。
A.金属键 B.氢键 C.π键 D.配位键 E.范德华力
 )是检验
)是检验 的灵敏试剂,在稀氨水介质中,
的灵敏试剂,在稀氨水介质中, 与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
与丁二酮肟反应可生成鲜红色沉淀丁二酮肟镍,其分子结构如图所示。
回答下列问题:
(1)Ni在元素周期表中的位置为
(2)Ni与Ca位于同一周期且最外层电子数相同,单质Ni的熔点明显高于Ca,其原因是
(3)1mol丁二酮肟分子含有σ键数目为
 是阿伏加德罗常数的值)。
是阿伏加德罗常数的值)。(4)丁二酮肟镍分子中C原子的杂化轨道类型有
 的原因是
的原因是(5)丁二酮肟镍分子内不存在的作用力有
A.金属键 B.氢键 C.π键 D.配位键 E.范德华力
您最近一年使用:0次
名校
解题方法
3 . 请回答下列有关问题。
(1)Fe元素按周期表分区属于___________ 区元素
(2)地壳中含量最多的三种元素O、Si、Al中,电负性最大的是___________ 。
(3)钠在火焰上灼烧产生的黄光是一种___________ (填字母)
A.吸收光谱 B.发射光谱
(4)Cu的基态原子的电子排布式是___________ 。
(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是___________ 。
(6)基态Fe3+与Fe2+离子中未成对的电子数之比为___________
(7)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为________ 。
(8)H2O分子的空间构型为___________
(1)Fe元素按周期表分区属于
(2)地壳中含量最多的三种元素O、Si、Al中,电负性最大的是
(3)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(4)Cu的基态原子的电子排布式是
(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是
(6)基态Fe3+与Fe2+离子中未成对的电子数之比为
(7)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(8)H2O分子的空间构型为
您最近一年使用:0次
名校
解题方法
4 . 黄铜矿(主要成分为CuFeS2)是生产铜、铁和硫酸的原料。回答下列问题:
(1)基态Cu原子的价电子排布式为_______ 。
(2)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如图所示:
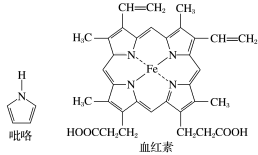
①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为_______ 。
②1mol吡咯分子中所含的σ键总数为_______ 个。
③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为_______ (填化学式)。
④血液中O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过_______ 键相结合的。
(3)黄铜矿冶炼铜时产生的SO2可经过SO2→SO3→H2SO4途径形成酸雨。SO2的立体构型为_______ 。H2SO4的酸性强于H2SO3的原因是_______ 。
(1)基态Cu原子的价电子排布式为
(2)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如图所示:

①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为
②1mol吡咯分子中所含的σ键总数为
③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为
④血液中O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过
(3)黄铜矿冶炼铜时产生的SO2可经过SO2→SO3→H2SO4途径形成酸雨。SO2的立体构型为
您最近一年使用:0次
2021-01-29更新
|
178次组卷
|
2卷引用:陕西省榆林市第十二中学2020-2021学年高二下学期第二次月考(5月底)化学试题
解题方法
5 . 铁及其化合物在国民生产、生活中用途广泛。
(1)向FeCl3溶液加入少量的KSCN溶液,生成红色的[Fe(SCN)(H2O)5]2+。N、C、H元素的第一电离能由大到小的顺序为___________ ,O、N、C、H四种元素电负性最大的是___________ (填元素符号) 。
(2)FeCl3 与K4[Fe(CN)6]溶液混合生成Fe4[Fe(CN)6]3沉淀。配体CN-中C原子的杂化方式为___________ ,CH2=CHCH2CN分子中σ键与π键的数目比n(σ)∶n(π)=___________ 。
(3)用邻二氮菲(phen,如图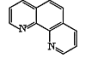 )与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
)与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
①[Fe(phen)3]2+中,存在的化学键有___________ (填序号)。
a.配位键 b.离子键 c.π键 d.氢键
②用邻二氮菲测定Fe2+浓度时应控制pH为2~9的适宜范围,请解释原因___________ 。
(4)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。
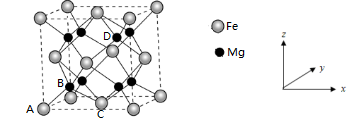
晶体中每个铁原子周围距离最近的镁原子有___________ 个,原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),B为( ),C为(
),C为(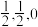 ),则D点坐标参数为
),则D点坐标参数为___________ 。
(1)向FeCl3溶液加入少量的KSCN溶液,生成红色的[Fe(SCN)(H2O)5]2+。N、C、H元素的第一电离能由大到小的顺序为
(2)FeCl3 与K4[Fe(CN)6]溶液混合生成Fe4[Fe(CN)6]3沉淀。配体CN-中C原子的杂化方式为
(3)用邻二氮菲(phen,如图
 )与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。
)与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。①[Fe(phen)3]2+中,存在的化学键有
a.配位键 b.离子键 c.π键 d.氢键
②用邻二氮菲测定Fe2+浓度时应控制pH为2~9的适宜范围,请解释原因
(4)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。

晶体中每个铁原子周围距离最近的镁原子有
 ),C为(
),C为(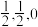 ),则D点坐标参数为
),则D点坐标参数为
您最近一年使用:0次
2021-01-29更新
|
299次组卷
|
2卷引用:河北省衡水市第十四中学2022-2023学年高二下学期第一次选择性考试化学试题
名校
解题方法
6 . A、B、C、D、E、F的核电荷数依次增大。A的最外层电子数是次外层电子数的一半、是最内层电子数的2倍,D和E的价电子数都是7,F的基态原子中有4个未成对电子。
(1)A在元素周期表中的位置是_______ ,基态 的核外电子排布式是
的核外电子排布式是_______ 。
(2)A、B、C、D的第一电离能由小到大的顺序是_______ (用元素符号表示)。
(3) 分子的空间结构为
分子的空间结构为_______ 。
(4)单质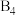 的结构如图所示,
的结构如图所示, 该分子中含有的
该分子中含有的 键的数目为
键的数目为_______ 。

(1)A在元素周期表中的位置是
 的核外电子排布式是
的核外电子排布式是(2)A、B、C、D的第一电离能由小到大的顺序是
(3)
 分子的空间结构为
分子的空间结构为(4)单质
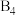 的结构如图所示,
的结构如图所示, 该分子中含有的
该分子中含有的 键的数目为
键的数目为
您最近一年使用:0次
7 . 以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵【(NH4)3Fe(C6H5O7)2】。
(1)Fe基态核外电子排布式为___________ ; 中与Fe2+配位的原子是
中与Fe2+配位的原子是________ (填元素符号)。
(2)NH3分子中氮原子的轨道杂化类型是____________ ;C、N、O元素的第一电离能由大到小的顺序为_______________ 。
(3)与NH 互为等电子体的一种分子为
互为等电子体的一种分子为_______________ (填化学式)。
(4)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为_________ mol。

(1)Fe基态核外电子排布式为
 中与Fe2+配位的原子是
中与Fe2+配位的原子是(2)NH3分子中氮原子的轨道杂化类型是
(3)与NH
 互为等电子体的一种分子为
互为等电子体的一种分子为(4)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为

您最近一年使用:0次
2020-07-11更新
|
4578次组卷
|
10卷引用:山东省潍坊市临朐县实验中学2021届高三9月月考化学试题
山东省潍坊市临朐县实验中学2021届高三9月月考化学试题2020年江苏卷化学高考试题(已下线)专题17 物质结构与性质(选修)-2020年高考真题和模拟题化学分项汇编(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)考向37 分子结构与性质-备战2022年高考化学一轮复习考点微专题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)2020年江苏卷化学高考真题变式题16-21(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习黑龙江省哈尔滨市第六中学2021-2022学年高二下学期期中考试化学试题(已下线)结构与性质
名校
解题方法
8 . 氢原子是最轻的原子,人们曾预言它可能是所有元素之母。碳是地球上组成生命的最基本的 元素之一。按要求回答:
(1)宇宙中含量最多的元素是氢和______ 。基态碳原子的核外电子占有______ 个原子轨道。
(2)光化学烟雾中除了含有 NOx 外,还含有 HCOOH、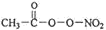 (PAN)等二次污染物。
(PAN)等二次污染物。
①PAN 中 C 的杂化方式有______ 。1mol PAN 中含有的σ键数目为______ 。组成PAN 的元素的电负性大小顺序为______ 。
②相同压强下,HCOOH 的沸点比 CH3OCH3______ (填“高”或“低”),
(3)水溶液中有 H3O+、H5O2+、H9O4+ 等微粒的形式。请画出 H5O2的结构式:______ 。
(4)硅和碳在同一主族。下图为 SiO2晶胞中 Si 原子沿 z 轴方向在 xy 平面的投影图(即俯视图),其 中 O原子略去,Si 原子旁标注的数字表示每个 Si 原子位于 z 轴的高度,则 SiA 与 SiB 之间的距离是______ nm。
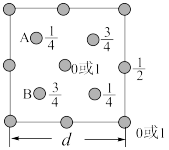 (d 的单位为 nm)
(d 的单位为 nm)
(1)宇宙中含量最多的元素是氢和
(2)光化学烟雾中除了含有 NOx 外,还含有 HCOOH、
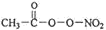 (PAN)等二次污染物。
(PAN)等二次污染物。①PAN 中 C 的杂化方式有
②相同压强下,HCOOH 的沸点比 CH3OCH3
(3)水溶液中有 H3O+、H5O2+、H9O4+ 等微粒的形式。请画出 H5O2的结构式:
(4)硅和碳在同一主族。下图为 SiO2晶胞中 Si 原子沿 z 轴方向在 xy 平面的投影图(即俯视图),其 中 O原子略去,Si 原子旁标注的数字表示每个 Si 原子位于 z 轴的高度,则 SiA 与 SiB 之间的距离是
 (d 的单位为 nm)
(d 的单位为 nm)
您最近一年使用:0次
2020-03-27更新
|
221次组卷
|
4卷引用:菏泽一中2020届高三3月份化学质量检测
解题方法
9 . (1)下列数据是对应物质的熔点(℃)
据此作出的下列判断中,错误的是_____ 。
A 铝的化合物晶体中不存在离子晶体
B 表中只有BCl3、干冰是分子晶体
C 同族元素的氧化物可形成不同类型的晶体
D 不同族元素的氧化物可形成不同类型的晶体
(2)SiO2晶体结构片断如图所示。SiO2晶体中Si原子数目和Si﹣O键数目的比例为_____ 。

通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
Si(s)+ O2(g)=SiO2(s),该反应的反应热△H=__________ 。
(3)单质铝晶体晶胞特征如图乙所示.则晶胞中铝原子的配位数为_____ ,晶胞中存在两种空隙,分别是___________ 、___________ 。

| NaCl | Na2O | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 801 | 920 | 1291 | 190 | -109 | 2073 | -57 | 1723 |
据此作出的下列判断中,错误的是
A 铝的化合物晶体中不存在离子晶体
B 表中只有BCl3、干冰是分子晶体
C 同族元素的氧化物可形成不同类型的晶体
D 不同族元素的氧化物可形成不同类型的晶体
(2)SiO2晶体结构片断如图所示。SiO2晶体中Si原子数目和Si﹣O键数目的比例为

通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
| 化学键 | Si-O | Si-Si | O=O |
| 键能/KJ•mol-1 | 460 | 176 | 498 |
Si(s)+ O2(g)=SiO2(s),该反应的反应热△H=
(3)单质铝晶体晶胞特征如图乙所示.则晶胞中铝原子的配位数为

您最近一年使用:0次
名校
解题方法
10 . 在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac。请回答下列问题:
(1)C、N、O的电负性由大到小的顺序为________ 。
(2)写出Cu的核外电子排布式________ 。
(3)化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为________ 。
(4)在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为________ ;1mol尿素分子中,σ 键的数目为________ 。
(1)C、N、O的电负性由大到小的顺序为
(2)写出Cu的核外电子排布式
(3)化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为
(4)在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为
您最近一年使用:0次
2018-07-13更新
|
142次组卷
|
2卷引用:【全国百强校】贵州省思南中学2018-2019学年高二下学期第二次月考化学试题



