解题方法
1 . 下列关于物质的结构或性质以及解释均正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 键角:NH3>BF3 | NH3中N的孤电子对数比BF3中B的孤电子对数多 |
| B | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl的电负性,使CF3COOH中羧基上的氢更易电离 |
| C | 熔点:碳化硅>金刚石 | C﹣Si键能大于C﹣C键能 |
| D | 稳定性:H2O>CH4 | H2O分子之间除了范德华力以外还存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 硅烷广泛应用在现代高科技领域。
制备硅烷的反应为 。
。
(1)①基态硅原子的价层电子轨道表示式为___________ 。
② 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是___________ 。
③下列说法正确的是___________ (填字母)。
a. 的稳定性比
的稳定性比 的差
的差
b. 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c. 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键
④ 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是___________ 。
(2) 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为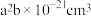 。
。 的
的 模型名称为
模型名称为___________ 。
②用 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为___________  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
制备硅烷的反应为
 。
。(1)①基态硅原子的价层电子轨道表示式为
②
 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是③下列说法正确的是
a.
 的稳定性比
的稳定性比 的差
的差b.
 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c.
 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键④
 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是(2)
 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为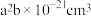 。
。
 的
的 模型名称为
模型名称为②用
 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
3 . 下列化学用语或图示表达正确的是
A.NO 的VSEPR模型: 的VSEPR模型: |
B.反-2-丁烯的分子结构模型: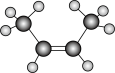 |
C.p-pσ键电子云轮廓图: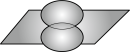 |
| D.基态Cr原子的价层电子排布式:3d44s2 |
您最近一年使用:0次
名校
解题方法
4 . 下列分子或离子的 模型与其空间结构不一致的是
模型与其空间结构不一致的是
 模型与其空间结构不一致的是
模型与其空间结构不一致的是A. | B. | C.SO2 | D. |
您最近一年使用:0次
名校
解题方法
5 . 下列化学用语或图示表达不正确 的是
A.HCl分子中 键的形成: 键的形成: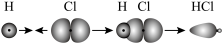 |
B.As的原子结构示意图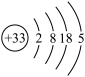 |
C. 的VSEPR模型: 的VSEPR模型: |
D.基态Cr原子的价层电子排布式: |
您最近一年使用:0次
名校
6 . 原子序数依次增大的短周期元素X、Y、Z、W的某些性质如下。
下列说法正确的是
| 元素 | X | Y | Z | W |
| 电负性 | 2.5 | 3.5 | 2.5 | 3.0 |
| 最低化合价 | -4 | -2 | -2 | -1 |
| A.在XY2分子中只有σ键没有π键 |
| B.在ZY2分子中Z显负价 |
| C.最高价含氧酸的酸性:H2ZO4>HWO4 |
| D.XW4分子的空间结构是正四面体形 |
您最近一年使用:0次
名校
7 . NH3具有易液化、含氢密度高、应用广泛等优点,NH3的合成及应用一直是科学研究的重要课题。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为_____ 。
②我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是_____ 。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是_____ 。
②NaHCO3分解得Na2CO3., 空间结构为
空间结构为_____ 。
(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
①NH3的中心原子的杂化轨道类型为_____ 。
②比较熔点:NH3BH3_____ CH3CH3(填“>”或“<”)。
(4)NF3的结构与NH3类似,但是性质差异较大。
①NF3的空间结构名称为_____ 。
②NH3BH3具有碱性(可与H+结合)而NF3没有碱性。原因是_____ 。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为
②我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是
②NaHCO3分解得Na2CO3.,
 空间结构为
空间结构为(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
| 元素 | H | B | N | F |
| 电负性 | 2.1 | 2.0 | 3.0 | 4.0 |
②比较熔点:NH3BH3
(4)NF3的结构与NH3类似,但是性质差异较大。
①NF3的空间结构名称为
②NH3BH3具有碱性(可与H+结合)而NF3没有碱性。原因是
您最近一年使用:0次
2024-03-03更新
|
275次组卷
|
2卷引用:北京市第十九中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
8 . 下列说法正确的是
A. 和 和 分子中均含有 分子中均含有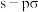 键 键 |
B. 和 和 的VSEPR模型和空间结构均一致 的VSEPR模型和空间结构均一致 |
| C.熔点:金刚石>碳化硅>晶体硅 |
D.酸性: |
您最近一年使用:0次
2024-02-24更新
|
220次组卷
|
2卷引用:北京市大兴区第一中学2023-2024学年高二下学期期中考试化学试题
名校
解题方法
9 . 下列分子的空间结构以及中心原子的杂化方式都相同的是
A. 和 和 | B. 和 和 |
C. 和 和 | D. 和 和 |
您最近一年使用:0次
名校
解题方法
10 . 水丰富而独特的性质与其结构密切相关。
(1)对于水分子中的共价键,依据原子轨道重叠的方式判断,属于___________ 键;依据О与H的电负性判断,属于___________ 共价键。
(2)水分子中,氧原子的价层电子对数为___________ ,杂化轨道类型为___________ 。
(3)水是优良的溶剂,常温常压下 极易溶于水,从微粒间相互作用的角度分析原因,请写出两条:
极易溶于水,从微粒间相互作用的角度分析原因,请写出两条:
①___________ ;
②___________ 。
(4)酸溶于水可形成 ,
, 的电子式为
的电子式为___________ 。由于成键电子对和孤电子对之间的斥力不同,会对微粒的空间结构产生影响,如 中H-N-H的键角大于
中H-N-H的键角大于 中H-O-H的键角,据此判断
中H-O-H的键角,据此判断 和
和 的键角大小:
的键角大小:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(5)我国科学家利用高分辨原子力显微镜技术,首次拍摄到质子在水层中的原子级分辨图像,发现两种结构的水合质子,其中一种结构如图所示。下列有关该水合质子的说法正确的是___________ 。

A.化学式为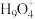
B.氢、氧原子都处于同一平面
C.氢、氧原子间均以氢键结合
(1)对于水分子中的共价键,依据原子轨道重叠的方式判断,属于
(2)水分子中,氧原子的价层电子对数为
(3)水是优良的溶剂,常温常压下
 极易溶于水,从微粒间相互作用的角度分析原因,请写出两条:
极易溶于水,从微粒间相互作用的角度分析原因,请写出两条:①
②
(4)酸溶于水可形成
 ,
, 的电子式为
的电子式为 中H-N-H的键角大于
中H-N-H的键角大于 中H-O-H的键角,据此判断
中H-O-H的键角,据此判断 和
和 的键角大小:
的键角大小:
 (填“>”或“<”)。
(填“>”或“<”)。(5)我国科学家利用高分辨原子力显微镜技术,首次拍摄到质子在水层中的原子级分辨图像,发现两种结构的水合质子,其中一种结构如图所示。下列有关该水合质子的说法正确的是

A.化学式为
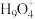
B.氢、氧原子都处于同一平面
C.氢、氧原子间均以氢键结合
您最近一年使用:0次



