名校
解题方法
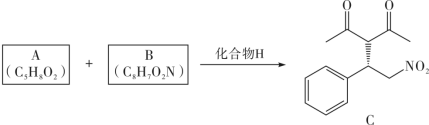
1 . 溶剂是影响化学反应的重要因素之一,当反应在无溶剂条件下进行时,具有操作简单、反应时间短、无溶剂浪费且遵循绿色化学的原理等独特优点。因此,无溶剂不对称催化已成为合成化学中的重要课题。化合物H是一种手性有机催化剂,可无溶剂催化如下迈克尔加成反应(Michael addition reaction): 、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
(1)A的化学名称为___________ ;B为反式结构,其结构简式为___________ 。
(2)已知E的核磁共振氢谱只有一个吸收峰。写出D(用 简化表示)与E反应的化学方程式
简化表示)与E反应的化学方程式___________ ,该反应类型为___________ 。
(3)G的同分异构体中,含有碳、氮环状骨架为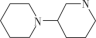 的共有
的共有___________ 种(不含立体异构)。
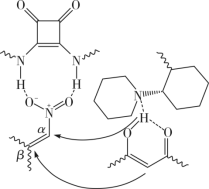
(4)推测H催化A和B反应的部分机理可能为:A异构化为烯醇(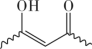 ),再和B与催化剂H结合(如图所示,
),再和B与催化剂H结合(如图所示, 表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的
表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的___________ (填标号)。
a.离子键 b.共价键 c.配位键 d.氢键___________ 。
(5)如果要合成H的类似物H′(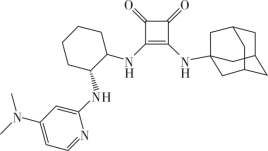 ),参照上述合成路线,写出相应的G′的结构简式
),参照上述合成路线,写出相应的G′的结构简式___________ 。以甲苯为溶剂,H′可催化A与B的迈克尔加成反应,产物主要是___________ (填“C”“C的手性异构体”或“C及其手性异构体各占50%”),判断理由是___________ 。
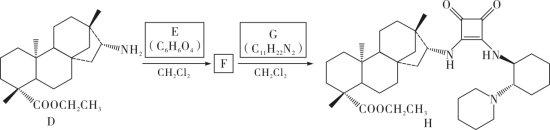
化合物H的合成路线如下( 、
、 分别表示由纸面向内、向外伸展的共价键):
分别表示由纸面向内、向外伸展的共价键):
 、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体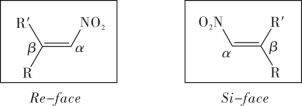
(1)A的化学名称为
(2)已知E的核磁共振氢谱只有一个吸收峰。写出D(用
 简化表示)与E反应的化学方程式
简化表示)与E反应的化学方程式(3)G的同分异构体中,含有碳、氮环状骨架为
 的共有
的共有(4)推测H催化A和B反应的部分机理可能为:A异构化为烯醇(
 ),再和B与催化剂H结合(如图所示,
),再和B与催化剂H结合(如图所示,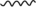 表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的
表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的a.离子键 b.共价键 c.配位键 d.氢键
(5)如果要合成H的类似物H′(
 ),参照上述合成路线,写出相应的G′的结构简式
),参照上述合成路线,写出相应的G′的结构简式
您最近一年使用:0次
名校
解题方法
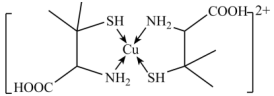
2 . 铜盐中毒可用青霉胺解毒,解毒原理如下: 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
A.比较硫化氢与氨气键角的大小: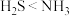 |
| B.第二周期主族元素中,第一电离能大于N的元素有1种 |
| C.该环状络合物易溶于水的主要原因是其与水可形成分子间氢键 |
| D.该环状络合物中,VSEPR模型为四面体或正四面体的非金属原子共有13个 |
您最近一年使用:0次
解题方法
3 . 下列关于物质结构和性质的说法正确的是
| A.键角:H2S>PH3>SiH4 |
| B.熔点:CsCl>KCl>NaCl |
C.NO 、NO 、NO 的VSEPR模型相同 的VSEPR模型相同 |
| D.酸性:CH3COOH>CCl3COOH>CF3COOH |
您最近一年使用:0次
解题方法
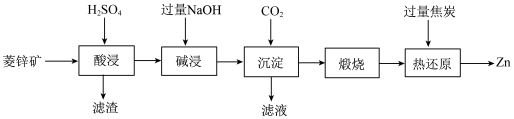
4 . 锌是一种应用广泛的金属,工业上以菱锌矿(主要成分是 、ZnO,含少量
、ZnO,含少量 和
和 )制备锌单质的流程如下:
)制备锌单质的流程如下:
已知:
a.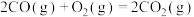

b.
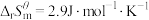
c.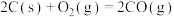
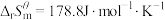
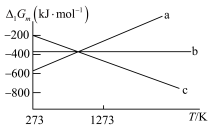
反应a,b,c的自由能变随温度的变化关系如图所示。
下列说法错误的是
 、ZnO,含少量
、ZnO,含少量 和
和 )制备锌单质的流程如下:
)制备锌单质的流程如下:
已知:
a.
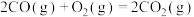

b.

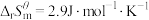
c.
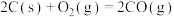
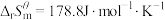
反应a,b,c的自由能变随温度的变化关系如图所示。

下列说法错误的是
| A.硫酸根离子的VSEPR模型为正四面体 |
| B.“酸浸”过程中加入食盐可增加滤渣的量 |
C.“沉淀”过程中,消耗 与 与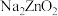 的物质的量之比为1∶1 的物质的量之比为1∶1 |
D.“热还原”过程中,发生主要反应的化学方程式为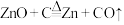 |
您最近一年使用:0次
名校
解题方法
5 . 铝和硅在地壳中含量丰富,其单质和化合物具有广泛的应用价值。请回答下列问题:
(1)①基态Si原子的价电子排布式为______ 。
②Si所在周期中的非金属元素(Si、P、S、Cl),其第一电离能由小到大的顺序为______ 。
(2) 的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物
的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物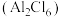 ,结构如图所示。
,结构如图所示。
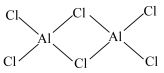
①基态Al原子核外电子的空间运动状态有______ 种,
②二聚物中Al原子的杂化轨道类型为______ 杂化。
(3)Al—空气—海水原电池的正极反应式为________________________ 。
(4)铝和白磷在一定条件下可以制备磷化铝(AlP),其晶胞如图所示:
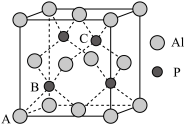
①晶胞中A1的配位数是______ ,
②若晶胞参数为apm, 为阿伏加德罗常数,则该晶胞的密度为
为阿伏加德罗常数,则该晶胞的密度为______  (列出表达式)。
(列出表达式)。
(5)以高硫铝土矿(主要成分为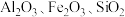 ,少量
,少量 和金属硫酸盐)为原料,获得
和金属硫酸盐)为原料,获得 的部分工艺流程如下:
的部分工艺流程如下:

①焙烧过程均会产生 ,用
,用 溶液吸收过量
溶液吸收过量 的离子方程式为
的离子方程式为__________________ 。
②“过滤”得到的滤渣中含大量的 。
。 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
______ 。
(1)①基态Si原子的价电子排布式为
②Si所在周期中的非金属元素(Si、P、S、Cl),其第一电离能由小到大的顺序为
(2)
 的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物
的相对分子质量为133.5,178℃开始升华,易溶于水、四氯化碳等,熔融时生成可挥发的二聚物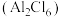 ,结构如图所示。
,结构如图所示。
①基态Al原子核外电子的空间运动状态有
②二聚物中Al原子的杂化轨道类型为
(3)Al—空气—海水原电池的正极反应式为
(4)铝和白磷在一定条件下可以制备磷化铝(AlP),其晶胞如图所示:

①晶胞中A1的配位数是
②若晶胞参数为apm,
 为阿伏加德罗常数,则该晶胞的密度为
为阿伏加德罗常数,则该晶胞的密度为 (列出表达式)。
(列出表达式)。(5)以高硫铝土矿(主要成分为
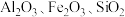 ,少量
,少量 和金属硫酸盐)为原料,获得
和金属硫酸盐)为原料,获得 的部分工艺流程如下:
的部分工艺流程如下:
①焙烧过程均会产生
 ,用
,用 溶液吸收过量
溶液吸收过量 的离子方程式为
的离子方程式为②“过滤”得到的滤渣中含大量的
 。
。 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
您最近一年使用:0次
名校
解题方法
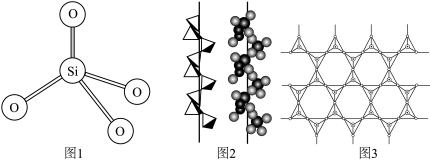
6 . 硅在自然界大部分以二氧化硅及硅酸盐的形式存在,它们的基本结构单位是硅氧四面体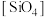 (图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
(图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
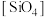 (图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
(图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
A.基态 原子的原子核外的电子有8种空间运动状态 原子的原子核外的电子有8种空间运动状态 |
| B.二氧化硅中硅原子的配位数是4 |
C.图2中Si原子的杂化轨道类型是 |
D.图3硅酸根阴离子结构中硅和氧的原子个数比为 |
您最近一年使用:0次
2023-12-01更新
|
324次组卷
|
3卷引用:安徽省江淮十校2024届高三上学期第二次联考化学试题
名校
解题方法
7 . 回答下列问题:
(1)根据价层电子对互斥理论,当价层电子对数为5时,轨道形状为三角双锥形,孤电子对数不同则分子空间结构不同,孤电子对数为1、2、3时,对应的分子或离子空间结构分别为变形四面体、 形、直线形,则
形、直线形,则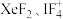 的空间构型分别为
的空间构型分别为_______ 、_______ 。
(2)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图a所示,图中用虚线标出了石墨的一个六方晶胞。若按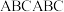 方式堆积而成,则如图
方式堆积而成,则如图 所示,图中用虚线标出了石墨的一个三方晶胞。
所示,图中用虚线标出了石墨的一个三方晶胞。 原子的分数坐标为
原子的分数坐标为_______ 。该六方石墨晶体的密度为_______  。
。
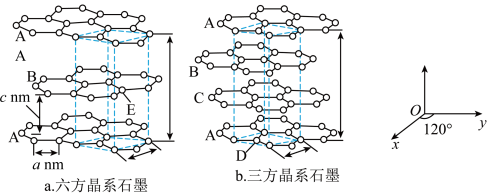
配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(3)茜草中的茜素与 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。
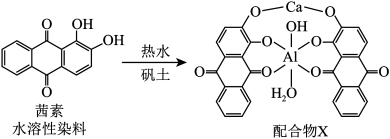
配合物 中
中 的配体除
的配体除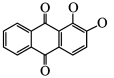 外还有
外还有_______ ,茜素水溶性较好的主要原因是_______ 。
(4)向 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶可得到
溶液后,经提纯、结晶可得到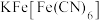 普鲁士蓝蓝色晶体。实验表明,
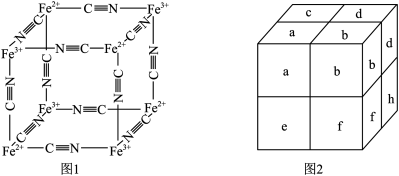
普鲁士蓝蓝色晶体。实验表明, 通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体
通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体 未标出)。
未标出)。
①可溶性氧化物(如 )有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是
)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是_______ 。
②若 位于II型立方结构的棱心和体心上,则
位于II型立方结构的棱心和体心上,则 位于II型立方结构的
位于II型立方结构的_______ 上;若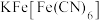 的摩尔质量为
的摩尔质量为 ,该蓝色晶体密度为
,该蓝色晶体密度为 ,II型立方结构的边长为
,II型立方结构的边长为 ,则阿伏加德罗常数的值可表示为
,则阿伏加德罗常数的值可表示为_______ 。
(1)根据价层电子对互斥理论,当价层电子对数为5时,轨道形状为三角双锥形,孤电子对数不同则分子空间结构不同,孤电子对数为1、2、3时,对应的分子或离子空间结构分别为变形四面体、
 形、直线形,则
形、直线形,则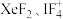 的空间构型分别为
的空间构型分别为(2)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图a所示,图中用虚线标出了石墨的一个六方晶胞。若按
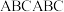 方式堆积而成,则如图
方式堆积而成,则如图 所示,图中用虚线标出了石墨的一个三方晶胞。
所示,图中用虚线标出了石墨的一个三方晶胞。 原子的分数坐标为
原子的分数坐标为 。
。
配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(3)茜草中的茜素与
 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。
配合物
 中
中 的配体除
的配体除 外还有
外还有(4)向
 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶可得到
溶液后,经提纯、结晶可得到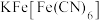 普鲁士蓝蓝色晶体。实验表明,
普鲁士蓝蓝色晶体。实验表明, 通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体
通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体 未标出)。
未标出)。
①可溶性氧化物(如
 )有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是
)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是②若
 位于II型立方结构的棱心和体心上,则
位于II型立方结构的棱心和体心上,则 位于II型立方结构的
位于II型立方结构的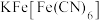 的摩尔质量为
的摩尔质量为 ,该蓝色晶体密度为
,该蓝色晶体密度为 ,II型立方结构的边长为
,II型立方结构的边长为 ,则阿伏加德罗常数的值可表示为
,则阿伏加德罗常数的值可表示为
您最近一年使用:0次
2023-11-04更新
|
350次组卷
|
2卷引用:山东省实验中学2024届高三上学期10月一诊考试化学试题
解题方法
8 . 四种短周期主族元素在元素周期表中的相对位置如图所示,且X、Y、Z和Q四种元素的p轨道电子总数为24。化学家鲍林以Y的电负性作为参照标准,得出了各元素的电负性。下列叙述错误的是
| X | Y | |||
| Z | Q |
| A.最简单氢化物的稳定性:Y>Q>Z |
B. 分子中每个原子最外层都达到8电子稳定结构 分子中每个原子最外层都达到8电子稳定结构 |
| C.最高价氧化物对应水化物的酸性: Z<Q |
D.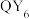 分子呈正八面体形 分子呈正八面体形 |
您最近一年使用:0次
2023-10-28更新
|
336次组卷
|
2卷引用:江西省部分高中学校2023-2024学年高三上学期10月联考化学试题
名校
解题方法
9 . 锰酸锂(LiMn2O4) 可作为某锂离子电池的正极材料,工业上利用软锰矿浆(主要成分为 MnO2,含少量 Fe2O3、FeO、Al2O3、SiO2。等杂质)吸收含硫烟气(主要成分 SO2) 制备锰酸锂,生产流程如图所示:

已知:①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强;
②在此流程中部分金属阳离子生成氢氧化物沉淀的 pH 如下表:
(1)含硫烟气中 SO2的VSEPR模型为___________ 。
(2)含硫烟气在通入软锰矿浆前需要先冷却,冷却的原因是___________ 。
(3)请写出含硫烟气在通入软锰矿浆后与 MnO2发生反应的化学方程式:___________ 。
(4)滤液1中所含金属阳离子除 以外还有
以外还有___________ (填离子符号)。
(5)由“滤液1”得到“滤液2”同时回收 Al(OH)3的实验方案如下:边搅拌边向滤液1中加入___________ ,再加入NaOH溶液调节pH范围为___________ ,过滤得到滤液 2 和滤渣,请设计实验方案由滤渣制得纯净 Al(OH)3[Al(OH)3在 pH≥12时溶解]的实验方案:___________ 。
(6)在实际生产中, Li2CO3与 MnO2按物质的量之比1:4混合均匀在 600℃~750℃制取 LiMn2O4,请写出该反应的化学方程式:___________ 。
(7)为测定锰酸锂的纯度, 取2.00g产品置于锥形瓶中, 向其中加入2.68g Na2C2O4和足量硫酸,充分反应后,用0.100mol/L KMnO4标准溶液滴定未反应完的 H2C2O4,到达滴定终点时消耗标准 KMnO4溶液20.00mL,已知:
 则该产品中锰酸锂的质量分数为
则该产品中锰酸锂的质量分数为___________ 。

已知:①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强;
②在此流程中部分金属阳离子生成氢氧化物沉淀的 pH 如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)含硫烟气中 SO2的VSEPR模型为
(2)含硫烟气在通入软锰矿浆前需要先冷却,冷却的原因是
(3)请写出含硫烟气在通入软锰矿浆后与 MnO2发生反应的化学方程式:
(4)滤液1中所含金属阳离子除
 以外还有
以外还有(5)由“滤液1”得到“滤液2”同时回收 Al(OH)3的实验方案如下:边搅拌边向滤液1中加入
(6)在实际生产中, Li2CO3与 MnO2按物质的量之比1:4混合均匀在 600℃~750℃制取 LiMn2O4,请写出该反应的化学方程式:
(7)为测定锰酸锂的纯度, 取2.00g产品置于锥形瓶中, 向其中加入2.68g Na2C2O4和足量硫酸,充分反应后,用0.100mol/L KMnO4标准溶液滴定未反应完的 H2C2O4,到达滴定终点时消耗标准 KMnO4溶液20.00mL,已知:

 则该产品中锰酸锂的质量分数为
则该产品中锰酸锂的质量分数为
您最近一年使用:0次
2023高三·全国·专题练习
名校
解题方法
10 . 偶极矩是电荷量与正、负电荷中心间的距离的乘积。用偶极矩可判断分子的极性:一般来说极性分子的偶极矩不为零;非极性分子的偶极矩为零。下列分子中偶极矩不为零的是
| A.BeCl2 | B.BF3 | C.PCl3 | D.CH4 |
您最近一年使用:0次



