名校
解题方法
1 . 研究发现,铜基催化剂可以促进二氧化碳(CO2)转换成一氧化碳(CO)、甲醛(CH2O)或乙烯(CH2=CH2)及乙醇(CH3CH2OH)等多碳化合物,对于“碳达峰”和“碳中和”目标的顺利实现具有积极推动作用。
(1)Cu基态原子核外电子排布式为___________ ,该元素位于元素周期表第___________ 族,属于___________ 区。
(2)下列说法正确的是___________ (填序号)
a.H2O、CH4、CO2的沸点:H2O>CO2>CH4
b.CH4分子中含有极性键,是极性分子
c.CH2=CH2、CH2O分子中碳原子的杂化方式不同
d.根据价层电子互斥理论,CH2O,H2O,BF3,SO3分子中,H2O的中心原子价层电子对数不同于其他分子
(3)已知具有相同价电子数和相同原子数的分子或离子具有相同的结构,这一原理称为“等电子原理”。根据等电子原理,写出两个与CO2具有相同空间构型的分子或者离子___________ 。
(4)在海洋生物作用下形成CaCO3,亦是减缓大气中CO2增加的主要途径。CaCO3中的化学键除了σ键外,还存在___________ 和大π键,CO 大π键应表示为
大π键应表示为___________ 。(大π键可用符号Π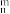 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数,如苯分子中的大π键表示为Π
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数,如苯分子中的大π键表示为Π )
)
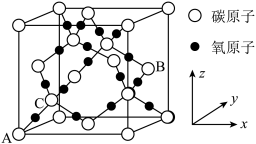
(5)铜基催化剂铁表面上铁原子吸附离解的碳原子局部示意图如图所示(图中小黑球代表碳原子,灰球代表铜原子)。则催化剂表面上C/Cu原子数比为___________ 。

(6)已和CO2在高温高压下所形成的晶体的晶胞如图所示,CO2的晶胞参数(棱长)apm,其密度为bg•cm-3,则阿伏加德罗常数为___________ (列出计算式即可)。
(1)Cu基态原子核外电子排布式为
(2)下列说法正确的是
a.H2O、CH4、CO2的沸点:H2O>CO2>CH4
b.CH4分子中含有极性键,是极性分子
c.CH2=CH2、CH2O分子中碳原子的杂化方式不同
d.根据价层电子互斥理论,CH2O,H2O,BF3,SO3分子中,H2O的中心原子价层电子对数不同于其他分子
(3)已知具有相同价电子数和相同原子数的分子或离子具有相同的结构,这一原理称为“等电子原理”。根据等电子原理,写出两个与CO2具有相同空间构型的分子或者离子
(4)在海洋生物作用下形成CaCO3,亦是减缓大气中CO2增加的主要途径。CaCO3中的化学键除了σ键外,还存在
 大π键应表示为
大π键应表示为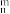 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数,如苯分子中的大π键表示为Π
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数,如苯分子中的大π键表示为Π )
)(5)铜基催化剂铁表面上铁原子吸附离解的碳原子局部示意图如图所示(图中小黑球代表碳原子,灰球代表铜原子)。则催化剂表面上C/Cu原子数比为

(6)已和CO2在高温高压下所形成的晶体的晶胞如图所示,CO2的晶胞参数(棱长)apm,其密度为bg•cm-3,则阿伏加德罗常数为

您最近一年使用:0次
名校
解题方法
2 . 我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。太阳能电池板主要材料为单晶硅或多晶硅,回答下列问题:
(1)基态硅原子的价电子排布式为_______ ,核外电子占据的最高能层符号为_____ 。
(2)硅和卤素单质反应可以得到SiX4,SiX4的熔沸点如下表所示:
0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是___________ (填化学式),它们的沸点依次升高的原因是___________ ,SiX4分子的空间构型是___________ 。
(3)1molCO2分子中存在___________ 个 键,写出与它互为等电子体的一种阴离子:
键,写出与它互为等电子体的一种阴离子:___________ 。
(1)基态硅原子的价电子排布式为
(2)硅和卤素单质反应可以得到SiX4,SiX4的熔沸点如下表所示:
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
(3)1molCO2分子中存在
 键,写出与它互为等电子体的一种阴离子:
键,写出与它互为等电子体的一种阴离子:
您最近一年使用:0次
解题方法
3 . 2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(2019-nCoV)的感染。

(1)已知磷酸氯喹的结构如图所示,则所含C、N、O三种元素电负性由大到小的顺序为___________ 。
(2)在[Cu(NH3)4]2+中∠HNH比游离的氨气分子中∠HNH___________ ,(填“大”“小”或“相等"),原因是___________ 。
(3)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有___________ 种不同运动状态的电子。
(4)如图2所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是___________ 。(填化学式)

(5)镁单质晶体中原子的堆积模型如图,它的堆积模型名称为___________ ;晶胞是图中的___________ (填a、b或c);配位数是___________ 。


(1)已知磷酸氯喹的结构如图所示,则所含C、N、O三种元素电负性由大到小的顺序为
(2)在[Cu(NH3)4]2+中∠HNH比游离的氨气分子中∠HNH
(3)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有
(4)如图2所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(5)镁单质晶体中原子的堆积模型如图,它的堆积模型名称为

您最近一年使用:0次
名校
解题方法
4 . VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是___ ;

(2)Se原子的原子序数为___ ,基态电子的排布式为[Ar]___ ;
(3)H2Se的稳定性比H2S___ (填“强”或“弱”)。SeO3分子的立体构型为___ 。
(4)下列分子中含手性碳的是___ 。
a. b.
b.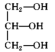 c.
c. d.CH3CHClCH2CHO
d.CH3CHClCH2CHO
(5)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因___ ;氮元素的E1呈现异常的原因是___ 。

(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(2)Se原子的原子序数为
(3)H2Se的稳定性比H2S
(4)下列分子中含手性碳的是
a.
 b.
b. c.
c. d.CH3CHClCH2CHO
d.CH3CHClCH2CHO(5)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因

您最近一年使用:0次
名校
5 . 已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的主族元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。
(1)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为___ 。
(2)A的氢化物(H2A)在乙醇中的溶解度大于H2D,其原因是___ 。
(3)A与D可形成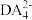 。
。
①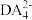 的空间构型为
的空间构型为___ (用文字描述)。
②写出一种与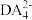 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:__ 。
(4)B、C、D、E的第一电离能由大到小的顺序是__ (写元素符号)。
(5)F的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为__ 。
(1)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为
(2)A的氢化物(H2A)在乙醇中的溶解度大于H2D,其原因是
(3)A与D可形成
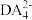 。
。①
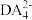 的空间构型为
的空间构型为②写出一种与
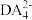 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(4)B、C、D、E的第一电离能由大到小的顺序是
(5)F的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
您最近一年使用:0次
名校
解题方法
6 . 著名化学家徐光宪在稀土化学等领域取得了卓越成就,被誉为“稀土界的袁隆平”。稀土元素包括钪、钇和镧系元素。请回答下列问题:
(1)写出基态Sc原子的核外电子排布式_________ ,其中电子占据的轨道数目为_________ 。
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3·nH2O+6HCl。
①HOOC-COOH中碳原子的杂化轨道类型为____ ,其中H、C、O的电负性由大到小的顺序为____ 。
②H2O的VSEPR模型为_____ ,写出与H2O互为等电子体的一种阴离子的化学式_____ 。
③HCl和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl·2H2O,HCl·2H2O中含有H5O ,结构为
,结构为 ,在该离子中,存在的作用力有
,在该离子中,存在的作用力有__________ 。
a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f.氢键 g.范德华力 h.π键 i.σ键
(3)据报道,在MnO2的催化下,甲醛(HCHO)可被氧化成CO2,则甲醛(HCHO)中的键角____ CO2中的键角(填“=”“>”或“<”)
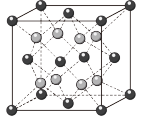
(4)PrO2(二氧化镨)的晶胞结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点。Pr(镨)的配位数________ 。假设相距最近的Pr原子与O原子之间的距离为a pm,则该晶体的密度为____ g⋅cm−3(用NA表示阿伏加 德罗常数的值,不必计算出结果)。已知M(Pr)=141g/mol,M(O)=16g/mol
(1)写出基态Sc原子的核外电子排布式
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3·nH2O+6HCl。
①HOOC-COOH中碳原子的杂化轨道类型为
②H2O的VSEPR模型为
③HCl和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl·2H2O,HCl·2H2O中含有H5O
 ,结构为
,结构为 ,在该离子中,存在的作用力有
,在该离子中,存在的作用力有a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f.氢键 g.范德华力 h.π键 i.σ键
(3)据报道,在MnO2的催化下,甲醛(HCHO)可被氧化成CO2,则甲醛(HCHO)中的键角
(4)PrO2(二氧化镨)的晶胞结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点。Pr(镨)的配位数

您最近一年使用:0次
解题方法
7 . 氯仿(CHCl3)不溶于水,但在一定条件下水解生成两种酸,其中一种是甲酸(HCOOH)。在19世纪氯仿广泛用于麻醉,可由“乙醛漂白粉法”制得。在光照条件下,氯仿易被空气氧化生成剧毒光气(COCl2)和一种化合物。因此氯仿需要小口钢罐贮存运输,使用前要检验其是否变质。
(1)CHCl3的电子式为____ ,COCl2的分子构型为____ ,HCOOH中C的杂化方式为____ ;
(2)漂白粉中三种元素的简单离子的半径的大小顺序为____ (用离子符号表示);
(3)为了检验氯仿是否变质,可向其中加入____ ,观察到 的现象,即可确认其已变质;
(4)Fe2+的外围电子排布图为____ ;
(5)纯铁的一种同素异形体的晶胞为面心立方晶胞,该晶体中原子的配位数为____ ,若铁原子的半径为a cm,则该晶体的密度为____ 。
(1)CHCl3的电子式为
(2)漂白粉中三种元素的简单离子的半径的大小顺序为
(3)为了检验氯仿是否变质,可向其中加入
(4)Fe2+的外围电子排布图为
(5)纯铁的一种同素异形体的晶胞为面心立方晶胞,该晶体中原子的配位数为
您最近一年使用:0次



