解题方法
1 . 下列各组粒子的中心原子杂化类型相同,其键角不相等的是
A. | B. |
C. 、环己烷 、环己烷 | D. (苯)、 (苯)、 |
您最近半年使用:0次
2 . 下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是
① ②
② ③
③ ④
④ ⑤
⑤
①
 ②
② ③
③ ④
④ ⑤
⑤
| A.①③④⑤ | B.①②③⑤ | C.①③⑤ | D.①②③④⑤ |
您最近半年使用:0次
名校
解题方法
3 . 下表中各粒子对应的空间结构及解释均正确的是
| 选项 | 粒子 | 空间结构 | 解释 |
| A | 氨基负离子( ) ) | 直线形 | N原子采取 杂化 杂化 |
| B | 二氧化硫( ) ) | V形 | S原子采取 杂化 杂化 |
| C | 碳酸根离子( ) ) | 三角锥形 | C原子采取 杂化 杂化 |
| D | 乙炔( ) ) | 直线形 | C原子采取 杂化且C原子的价电子均参与成键 杂化且C原子的价电子均参与成键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-04-07更新
|
284次组卷
|
26卷引用:(人教版2019)选择性必修2 第二章 分子结构与性质 B素养拓展区
(人教版2019)选择性必修2 第二章 分子结构与性质 B素养拓展区河南省名校联盟2020-2021学年高二下学期开学考试化学试题(已下线)2.2 分子的空间结构(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)山东省泰安市宁阳一中2020-2021学年高二下学期3月月考化学试题(已下线)作业04 分子的空间结构-2021年高二化学暑假作业(人教版2019)2015-2016学年江苏省泰州中学高二下期中化学试卷四川省新津中学2019-2020学年高二下学期4月月考(入学)化学试题四川省成都外国语学校2019-2020学年高二下学期期中考试化学试题陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题四川绵阳南山中学双语学校2020-2021学年高二上学期10月月考化学试题湖南师范大学附属中学2020-2021学年高二上学期第三次大练习化学试题(已下线)2.2.2 杂化轨道理论(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)第2.2.2讲 杂化轨道理论-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)(已下线)第2章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)专题4 分子空间结构与物质性质 专题强化练5 分子(离子)的空间结构与杂化轨道类型的判断第二节 分子的空间结构 第2课时 杂化轨道理论湖南省邵阳市新邵县2021-2022学年高二上学期期末考试化学试题福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(1卷)试题天津市耀华中学2022-2023学年高二上学期期末考试化学试题陕西省武功县普集高级中学2022-2023学年高二下学期第一次月考化学试题广东省阳山县南阳中学2022-2023学年高二下学期第一次月考化学试题广东省深圳龙岗四校2022--2023学年高二下学期期中考试化学试题安徽省颍上第一中学2022-2023学年高二下学期5月月考化学试题黑龙江省大庆市肇州县第二中学2023-2024学年高二上学期12月月考化学试题湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题四川省内江市威远县威远中学校2023-2024学年高二下学期第一次月考化学试卷
名校
解题方法
4 . 下列图像正确的是
A. 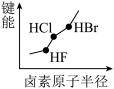 | B. 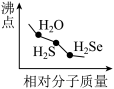 |
C. 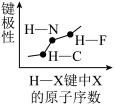 | D. 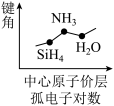 |
您最近半年使用:0次
2023-03-26更新
|
408次组卷
|
7卷引用:江苏省泰州中学2020-2021学年高一下学期期末考试化学试题
江苏省泰州中学2020-2021学年高一下学期期末考试化学试题山东省济宁市兖州区2019-2020学年高二5月阶段性测试化学试题(已下线)第2章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)河北省沧州市2021-2022学年高二下学期期末考试化学试题黑龙江省佳木斯市第十二中学2021-2022学年高二下学期期中考试化学试题河南省洛阳强基联盟2022-2023学年高二下学期3月联考化学试题湖北省宜昌市协作体2022-2023学年高二下学期期中考试化学试题
2022高三·全国·专题练习
5 . 下列符号表征或说法正确的是
A. 电离:H2S=HS- + H+ 电离:H2S=HS- + H+ | B. 位于元素周期表p区 位于元素周期表p区 |
C. 空间结构:平面三角形 空间结构:平面三角形 | D. 电子式: 电子式: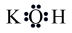 |
您最近半年使用:0次
2023-03-04更新
|
927次组卷
|
20卷引用:专题九 物质结构与性质-实战高考·二轮复习核心突破
(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破(已下线)专题01 STSE化学用语-2022年高考真题模拟题分项汇编(已下线)2022年辽宁省高考真题化学试题(部分试题)2022年辽宁高考真题化学试题辽宁省名校联盟2022-2023学年高三上学期9月联合考试化学试题辽宁省名校联盟2022-2023学年高三9月联合考试化学试题(已下线)2022年辽宁省高考真题变式题(1-10)(已下线)第30讲 分子结构与性质(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点01 化学用语-备战2023年高考化学考试易错题(已下线)第37讲 分子结构与性质(练)-2023年高考化学一轮复习讲练测(全国通用)江西省宜春市铜鼓中学2022-2023学年高二下学期第一次段考化学试题(已下线)专题卷03 物质基本组成化学用语-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)2022年辽宁高考真题化学试题变式题(选择题1-5)(已下线)专题02 化学用语(已下线)专题02 化学用语(已下线)第02练 化学用语-2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点06 原子结构(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题02 化学用语及其应用-2023年高考化学真题题源解密(新高考专用)(已下线)第29讲弱电解质的电离
名校
解题方法
6 . 我国科学家发现了一类由Fe-Se-As-F-O组成的磁性超导材料。下列说法正确的是
A.Fe变成 时首先失去3d轨道电子 时首先失去3d轨道电子 |
B.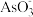 的空间构型为平面正三角形 的空间构型为平面正三角形 |
C.通过化学变化可以实现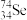 与 与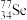 的相互转化 的相互转化 |
| D.基态F原子的核外电子最高能级为3p |
您最近半年使用:0次
2021高三·全国·专题练习
解题方法
7 . 根据所学知识回答问题
(1)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是___________ 。Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为___________ ,微粒之间存在的作用力是___________ 。比较下列锗卤化物的熔点和沸点,分析其变化规律及原因___________ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是___________ 。在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为___________ ,提供孤电子对的成键原子是___________ 。氨的沸点___________ (填“高于”或“低于”)膦(PH3),原因是___________ ;氨是___________ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为___________ 。
(3) AsCl3分子的立体构型为___________ ,其中As的杂化轨道类型为___________ 。
(1)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是
(3) AsCl3分子的立体构型为
您最近半年使用:0次
解题方法
8 . 下列分子的VSEPR模型与分子立体结构模型一致的是
| A.NH3 | B.CCl4 | C.H2O | D.PCl3 |
您最近半年使用:0次
2022-12-20更新
|
591次组卷
|
3卷引用:四川省宜宾市南溪区第二中学校2021-2022学年高二上学期12月月考化学试题
解题方法
9 . 按要求回答下列问题。
(1)下列基态原子或离子的电子排布式或轨道表示式正确的是_______ (填序号,下同),违反能量最低原理的是_______ ,违反泡利不相容原理的是_______ ,违反洪特规则的是_______ 。
①Si:
②Al:
③Co3+最外层:
④Mg2+:1s22s22p6
⑤Sc:1s22s22p63s23p63d3
⑥Cr:1s22s22p63s23p63d54s1
(2)物质:①甲烷 ②硫化氢 ③氢氧化镁 ④氨气 ⑤乙烯
(1)下列基态原子或离子的电子排布式或轨道表示式正确的是
①Si:

②Al:

③Co3+最外层:

④Mg2+:1s22s22p6
⑤Sc:1s22s22p63s23p63d3
⑥Cr:1s22s22p63s23p63d54s1
(2)物质:①甲烷 ②硫化氢 ③氢氧化镁 ④氨气 ⑤乙烯
| 条件 | 符合条件物质的序号 |
| 既含极性键又含非极性键 | |
| 含有极性键的极性分子 | |
| 上述分子中键角由大到小的顺序 |
您最近半年使用:0次
10 . 三氟化氮(NF3)是常见的蚀刻剂,用F2制备NF3的反应为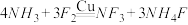 。下列说法错误的是
。下列说法错误的是
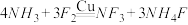 。下列说法错误的是
。下列说法错误的是| A.NF3空间构型为三角锥形 |
| B.Cu是过渡元素,位于元素周期表的ds区 |
C.NF3和NH 中氮原子的轨道杂化类型不相同 中氮原子的轨道杂化类型不相同 |
| D.若有0.4molNH3参加反应,转移电子的物质的量为0.6mol |
您最近半年使用:0次
2022-12-14更新
|
134次组卷
|
2卷引用:山东省高密市第三中学2021-2022学年高二上学期冬学竞赛化学试题



