名校
解题方法
1 . Ⅰ.物质的光学性质在科研中有重要的用途,回答下列问题:
一种比率光声探针M与 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如图所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如图所示:________  中键角F-B-F(填“>”、“<”或“=”);基态
中键角F-B-F(填“>”、“<”或“=”);基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为________ 。
(2)均为平面结构的吡咯( )和吡啶(
)和吡啶(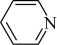 )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为________ ,原因是________ 。
Ⅱ.分析如图晶胞结构特点,回答下列问题:
(3)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。已知:立方氮化硼密度为 ,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为
,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为 ,则该晶胞中原子的空间利用率(晶胞中原子的体积占晶胞体积的百分率)为
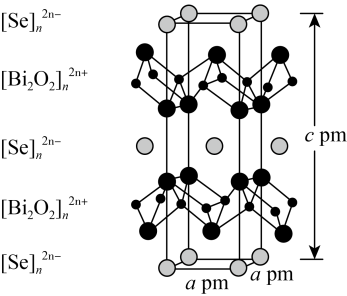
,则该晶胞中原子的空间利用率(晶胞中原子的体积占晶胞体积的百分率)为________ (列出计算式即可,不用化简)。 层与带负电的
层与带负电的 层交替堆积。据此推断硒氧化铋的化学式为
层交替堆积。据此推断硒氧化铋的化学式为________ 。晶胞棱边夹角均为90°,则晶体密度的计算式为________  。
。
一种比率光声探针M与
 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如图所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如图所示: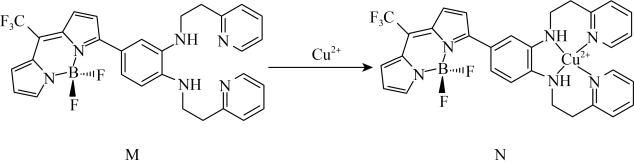
 中键角F-B-F(填“>”、“<”或“=”);基态
中键角F-B-F(填“>”、“<”或“=”);基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为(2)均为平面结构的吡咯(
 )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为Ⅱ.分析如图晶胞结构特点,回答下列问题:
(3)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。已知:立方氮化硼密度为
 ,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为
,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为 ,则该晶胞中原子的空间利用率(晶胞中原子的体积占晶胞体积的百分率)为
,则该晶胞中原子的空间利用率(晶胞中原子的体积占晶胞体积的百分率)为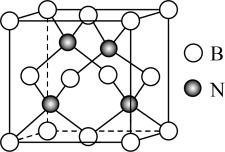
 层与带负电的
层与带负电的 层交替堆积。据此推断硒氧化铋的化学式为
层交替堆积。据此推断硒氧化铋的化学式为 。
。
您最近一年使用:0次
解题方法
2 . W、X、Y、Z、R为原子序数依次增大的短周期主族元素,W的核外电子只有一种自旋方向;Y、Z、R在元素周期表中相邻,X的核外电子数与Y的价层电子数相等,R2是氧化性最强的单质,回答下列问题:
(1)由X原子核形成的三种微粒,电子排布式分别为:①1s22s2、②1s22s22p1、③1s22s12p2,有关这些微粒的叙述正确的是___________ (填标号)。
a.得电子能力:②>① b.表示基态原子(或离子)的是:①②
c.微粒半径:①>② d.电离一个电子所需最低能量:①>②>③
(2)YR3是一种重要的电子工业材料。分子的极性:YR3___________ XR3(填“>”或“<”或“=”);YR3与YW3结构相似,YW3易与过渡金属阳离子形成配离子而YR3不能,原因是___________ 。
(3)同周期元素中,第一电离能比Z大的元素有_________ 种;Z与Y形成的固态Y2Z5由YZ 和YZ
和YZ 两种离子组成,固态Y2Z5中Y原子的杂化方式为
两种离子组成,固态Y2Z5中Y原子的杂化方式为_________ ,YZ 的电子式为
的电子式为_________ 。
(4)X与Z可形成多种结构形式的阴离子,已知阴离子X3Z 结构中只有一个正六元环,则n=
结构中只有一个正六元环,则n=___________ ,该阴离子的结构式为___________ 。
(1)由X原子核形成的三种微粒,电子排布式分别为:①1s22s2、②1s22s22p1、③1s22s12p2,有关这些微粒的叙述正确的是
a.得电子能力:②>① b.表示基态原子(或离子)的是:①②
c.微粒半径:①>② d.电离一个电子所需最低能量:①>②>③
(2)YR3是一种重要的电子工业材料。分子的极性:YR3
(3)同周期元素中,第一电离能比Z大的元素有
 和YZ
和YZ 两种离子组成,固态Y2Z5中Y原子的杂化方式为
两种离子组成,固态Y2Z5中Y原子的杂化方式为 的电子式为
的电子式为(4)X与Z可形成多种结构形式的阴离子,已知阴离子X3Z
 结构中只有一个正六元环,则n=
结构中只有一个正六元环,则n=
您最近一年使用:0次
名校
解题方法
3 . 周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,其次外层所有轨道均是全满状态。回答下列问题:
(1)b、c、d的简单离子半径最大的是___________ (填离子符号),e的晶胞结构中e配位数为___________ 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的电子式为___________ ;分子中既含有极性共价键、又含有非极性共价键的化合物是___________ (填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是___________ (任写一种);酸根呈三角锥结构的酸是___________ (填化学式)。
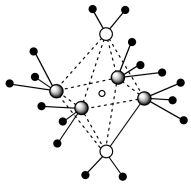
(4)e和c形成的一种离子化合物的晶体结构如图所示,则e离子的电荷为___________ 。

(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构。该化合物中,阴离子为___________ ,阳离子中存在的化学键类型有___________ 。
(1)b、c、d的简单离子半径最大的是
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的电子式为
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是
(4)e和c形成的一种离子化合物的晶体结构如图所示,则e离子的电荷为

(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构。该化合物中,阴离子为

您最近一年使用:0次
名校
解题方法
4 . X、Y、Z、W、Q五种元素位于元素周期表前四周期,原子序数依次增大。基态X原子价电子排布式为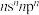 ;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素;基态Q原子有四个未成对电子。
;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素;基态Q原子有四个未成对电子。
(1)W核外电子空间运动状态共有_______ 种。
(2)阴离子 、
、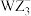 的空间构型分别是
的空间构型分别是_______ 、_______ 。
(3)基态Q原子中,核外电子占据最高能层的符号是_______ , 的价电子排布式为
的价电子排布式为_______ ,Q在周期表中的位置是_______ 区。
(4) 分子中各原子都满足最外层8电子结构,分子中
分子中各原子都满足最外层8电子结构,分子中 键与
键与 键数目之比为
键数目之比为_______ 。
(5)Y与W可形成化合物YW3。资料显示:Y元素电负性略大于W;YW3可溶于水发生水解反应。试判断YW3可能的水解产物为_______ (写化学式)。
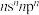 ;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素;基态Q原子有四个未成对电子。
;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素;基态Q原子有四个未成对电子。(1)W核外电子空间运动状态共有
(2)阴离子
 、
、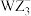 的空间构型分别是
的空间构型分别是(3)基态Q原子中,核外电子占据最高能层的符号是
 的价电子排布式为
的价电子排布式为(4)
 分子中各原子都满足最外层8电子结构,分子中
分子中各原子都满足最外层8电子结构,分子中 键与
键与 键数目之比为
键数目之比为(5)Y与W可形成化合物YW3。资料显示:Y元素电负性略大于W;YW3可溶于水发生水解反应。试判断YW3可能的水解产物为
您最近一年使用:0次
12-13高二上·四川遂宁·期中
名校
解题方法
5 . 下列说法错误的是
A.从CH4、 、 、 为正四面体结构,可推测PH 为正四面体结构,可推测PH 、 、 也为正四面体结构 也为正四面体结构 |
| B.1mol金刚石晶体中,平均含有2molC-C键 |
| C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 |
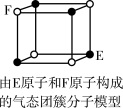
| D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
您最近一年使用:0次
2022-10-31更新
|
245次组卷
|
8卷引用:山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题
解题方法
6 . X、Y、Z、W、M、N、R是原子序数依次增大的前四周期元素,基态M原子的电子填充了3个能级,其中有2个未成对电子,N的最高正价与最低负价的代数和为6,基态R2+的d轨道半充满。由上述元素中的五种组成的某多孔储氢材料前驱体结构如图所示。

回答下列问题:
(1)基态Y原子的价电子排布图为_______ ,其中电子占据最高能级的电子云轮廓图为_______ 形;第一电离能介于Y和M之间的同周期元素有_______ 种。
(2)键角比较:
_______  (填“>”或“<”),理由是
(填“>”或“<”),理由是_______ 。
(3) R2+能形成配离子为八面体的配合物RNm∙nWX3,在该配合物中, 位于八面体的中心。若含0.5mol该配合物的溶液与足量
位于八面体的中心。若含0.5mol该配合物的溶液与足量 溶液反应可生成71.75g白色沉淀,则该配离子的化学式为
溶液反应可生成71.75g白色沉淀,则该配离子的化学式为_______ ;该配合物中心原子的价层电子对数为_______ ;下列对该配合物中心原子杂化方式推断合理的是_______ (填标号)。
a. b.
b. c.
c. d.
d.

回答下列问题:
(1)基态Y原子的价电子排布图为
(2)键角比较:

 (填“>”或“<”),理由是
(填“>”或“<”),理由是(3) R2+能形成配离子为八面体的配合物RNm∙nWX3,在该配合物中,
 位于八面体的中心。若含0.5mol该配合物的溶液与足量
位于八面体的中心。若含0.5mol该配合物的溶液与足量 溶液反应可生成71.75g白色沉淀,则该配离子的化学式为
溶液反应可生成71.75g白色沉淀,则该配离子的化学式为a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
2022-09-05更新
|
383次组卷
|
2卷引用:山东省临沂市2021-2022学年高二下学期期末考试化学试题
解题方法
7 . 随着环境污染及能源短缺的日益严重,汽车行业掀起了电动车热潮。2020年全球新能源汽车领导者比亚迪推出了“刀片电池”,大幅度提高了续航里程。刀片电池称为超级磷酸铁锂电池,其正极材料为 ,总反应式为:
,总反应式为: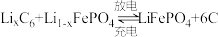 。回答下列问题:
。回答下列问题:
(1)Fe在元素周期表中的位置为___________ 。基态 比
比 结构稳定的原因可解释为
结构稳定的原因可解释为___________ 。
(2) 中Fe的化合价为
中Fe的化合价为___________ ,其离子常用___________ 试剂检验, 的空间构型为
的空间构型为___________ 。
(3)电池负极为嵌入Li的石墨烯层,其晶胞结构如下图。

①石墨烯是由碳原子形成的六元环状二维空间结构,其中C原子的杂化方式为___________ 。
②设 为阿伏加德罗常数的数值,该晶胞密度为
为阿伏加德罗常数的数值,该晶胞密度为___________  (列出计算式即可)。
(列出计算式即可)。
 ,总反应式为:
,总反应式为: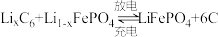 。回答下列问题:
。回答下列问题:(1)Fe在元素周期表中的位置为
 比
比 结构稳定的原因可解释为
结构稳定的原因可解释为(2)
 中Fe的化合价为
中Fe的化合价为 的空间构型为
的空间构型为(3)电池负极为嵌入Li的石墨烯层,其晶胞结构如下图。

①石墨烯是由碳原子形成的六元环状二维空间结构,其中C原子的杂化方式为
②设
 为阿伏加德罗常数的数值,该晶胞密度为
为阿伏加德罗常数的数值,该晶胞密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
名校
解题方法
8 . 2022年春晚节目《只此青绿》取材于宋代名画《千里江山图》,该画描绘了山清水秀的美丽景色,历经千年色彩依然,其中青色来自蓝铜矿颜料[主要成分为Cu3(CO3)2(OH)2]。请回答下列问题:
(1)基态铜原子价电子排布式为_______ 。从原子结构角度分析,第二电离能I2(Fe)与I2(Cu)的关系是I2(Fe)_______ I2(Cu) (填“>”“<”或“=”),并解释有关原因_______ 。
(2) 的空间构型为
的空间构型为_______ 。
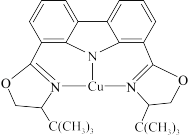
(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是_______ (填元素符号),该配合物中采用sp2杂化的碳原子与sp3杂化的碳原子个数比为_______ 。
(4)黄铜矿是主要的炼铜原料,晶胞结构如下图1所示,晶胞中S原子的投影位置如图2所示。
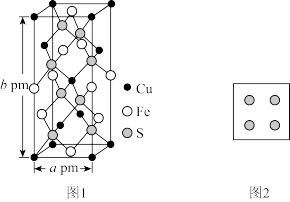
①Fe3+周围距离最近的S2-的个数为_______ 。
②该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,晶胞的密度为ρ g/cm3,则阿伏加德罗常数(NA)为_______ mol-1(用a、b、ρ表示,并化成最简)。
(1)基态铜原子价电子排布式为
(2)
 的空间构型为
的空间构型为(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素电负性由大到小的顺序是

(4)黄铜矿是主要的炼铜原料,晶胞结构如下图1所示,晶胞中S原子的投影位置如图2所示。

①Fe3+周围距离最近的S2-的个数为
②该晶胞上下底面均为正方形,侧面与底面垂直,晶胞参数如图所示,晶胞的密度为ρ g/cm3,则阿伏加德罗常数(NA)为
您最近一年使用:0次
2022-05-04更新
|
736次组卷
|
4卷引用:山东省菏泽市单县第二中学2021-2022学年高二下学期慧光班段考化学试题
山东省菏泽市单县第二中学2021-2022学年高二下学期慧光班段考化学试题四川省南充高级中学2021-2022学年高二下学期期中考试化学试题安徽省淮北市2022届高三第二次模拟考试理科综合化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)
名校
解题方法
9 . 钛(Ti)和锆(Zr)是同一副族的相邻元素,它们的化合物在生产、生活中有着广泛的用途。回答下列问题:
(1)钛和锆的价层电子结构相同,基态锆原子的价电子排布式为_______ ;与钛位于同一周期且基态原子单电子数与钛相同的元素,第一电离能由大到小的顺序为_______ (用元素符号填空)。
(2)Ti(BH4)2是一种储氢材料。BH 的空间构型是
的空间构型是_______ 。
(3)下列各组微粒互为等电子体的是_______(填字母标号)。
(4)ZrCl4可以与乙二胺形成配合物[ZrCl4(H2NCH2CH2NH2)]。
①1mol [ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为_______ mol。
②H2NCH2CH2NH2形成[ZrCl4(H2NCH2CH2NH2)]后,H-N-H键角将_______ (填“变大”、“变小”或“不变”),原因是_______ 。
(5)已知TiO2晶胞中Ti4+位于O2-所构成的正八面体的体心,ZrO2晶胞中Zr4+位于O2-所构成的立方体的体心,其晶胞结构如下图所示。

①TiO2晶胞中O2-的配位数是_______ 。
②TiO2晶胞中A、B的原子坐标为(0.69,0.69,1),(0.19,0.81,0.5),则C原子坐标为_______ 。
③已知二氧化锆晶胞的密度为ρ g·cm-3,则晶体中Zr原子和O原子之间的最短距离_______ pm(列出表达式,NA为阿伏加德罗常数的值,ZrO2的摩尔质量为M g/mol)。
(1)钛和锆的价层电子结构相同,基态锆原子的价电子排布式为
(2)Ti(BH4)2是一种储氢材料。BH
 的空间构型是
的空间构型是(3)下列各组微粒互为等电子体的是_______(填字母标号)。
| A.H2O与SO2 | B.CO2与N2O | C.CH2O与BF3 | D.C6H6与B3N3H6 |
①1mol [ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为
②H2NCH2CH2NH2形成[ZrCl4(H2NCH2CH2NH2)]后,H-N-H键角将
(5)已知TiO2晶胞中Ti4+位于O2-所构成的正八面体的体心,ZrO2晶胞中Zr4+位于O2-所构成的立方体的体心,其晶胞结构如下图所示。

①TiO2晶胞中O2-的配位数是
②TiO2晶胞中A、B的原子坐标为(0.69,0.69,1),(0.19,0.81,0.5),则C原子坐标为
③已知二氧化锆晶胞的密度为ρ g·cm-3,则晶体中Zr原子和O原子之间的最短距离
您最近一年使用:0次
名校
解题方法
10 . 根据所学物质结构与性质的知识回答下列问题。
(1)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
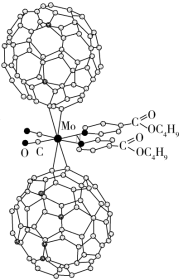
①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布图是___________ ,该超分子中存在的化学键类型有___________ (填选项字母)。
A.离子键B.氢键C.σ键D.π键
②该超分子中,配体CO提供孤电子对的原子是___________ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有___________ 。
(2)氟及其化合物用途非常广泛。
①聚四氟乙烯是一种准晶体,可通过___________ 方法区分晶体、准晶体和非晶体。
②AsF3、IF 、OF2,BeF2中价层电子对数不同于其它微粒的是
、OF2,BeF2中价层电子对数不同于其它微粒的是___________ (填化学式,下同),其立体构型为___________ 。
③室温氟穿梭电池的电解质为氟氢离子液体,含HF 、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式
、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式___________ 。
④基于CaF2设计的Born-Haber循环如图所示。
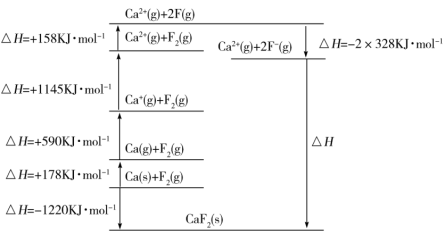
钙的第一电离能为___________ kJ·mol-1;F-F键的键能为___________ kJ·mol-1。
(1)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。

①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布图是
A.离子键B.氢键C.σ键D.π键
②该超分子中,配体CO提供孤电子对的原子是
(2)氟及其化合物用途非常广泛。
①聚四氟乙烯是一种准晶体,可通过
②AsF3、IF
 、OF2,BeF2中价层电子对数不同于其它微粒的是
、OF2,BeF2中价层电子对数不同于其它微粒的是③室温氟穿梭电池的电解质为氟氢离子液体,含HF
 、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式
、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式④基于CaF2设计的Born-Haber循环如图所示。

钙的第一电离能为
您最近一年使用:0次
2021-08-30更新
|
319次组卷
|
2卷引用:山东省济宁市2020-2021学年高二下学期期末考试化学试题



