名校
解题方法
1 . 二茂铁(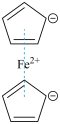 )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
(1)Fe在周期表中的___________ 区,Fe变为Fe2+时是失去___________ 轨道电子;若受热后Fe的1个4s电子会跃迁至4p轨道,写出Fe的该激发态电子排布式:[Ar]___________ 。
(2)羰基铁粉【Fe(CO)5】中铁元素的配位数是___________ ,配位原子为___________ 。
(3)二茂铁的衍生物可和H3O+等微粒产生静电作用,H、O和C的电负性由大到小的顺序为___________ ;H3O+中氧原子的杂化方式为___________ ,H3O+空间构型为___________ 。
(4)T-碳是碳的一种同素异形体,其晶体结构可以看成是金刚石晶体(如图甲)中每 个碳原子被一个由四个碳原子组成的正四面体结构单元( )所取代(如图乙)。
)所取代(如图乙)。

一个T-碳晶胞中含有___________ 个碳原子,已知T-碳的密度约为金刚石的一半。则T-碳晶胞的边长和金刚石晶胞的边长之比为___________ 。
 )分子式为
)分子式为 ,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。
,是具有导电性的有机配合物,其衍生物一直是科学研究的前沿。(1)Fe在周期表中的
(2)羰基铁粉【Fe(CO)5】中铁元素的配位数是
(3)二茂铁的衍生物可和H3O+等微粒产生静电作用,H、O和C的电负性由大到小的顺序为
(4)T-碳是碳的一种同素异形体,其晶体结构可以看成是金刚石晶体(如图甲)中每 个碳原子被一个由四个碳原子组成的正四面体结构单元(
 )所取代(如图乙)。
)所取代(如图乙)。
一个T-碳晶胞中含有
您最近一年使用:0次
名校
解题方法
2 . 我国在新材料领域的研究有重大突破,为“天宫”空间站的建设提供了物质基础。“天宫”空间站使用的材料中含有C、N、Si、P、Fe等元素。回答下列问题:
(1)基态硅原子的价电子排布式为___________ ,其基态原子核外有___________ 种不同空间运动状态的电子。
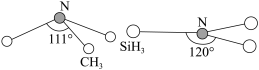
(2)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物的结构和性质存在较大差异。化合物 (三角锥形)和
(三角锥形)和 (平面形)的结构如图所示,则二者中N的杂化方式分别为
(平面形)的结构如图所示,则二者中N的杂化方式分别为___________ ,更易形成配合物的是___________ 。
(3)白磷在氯气中燃烧可以得到 和
和 ,其中气态
,其中气态 分子的空间结构为
分子的空间结构为________ 。
(4) 晶体的晶胞如图所示,晶胞边长为a nm。设
晶体的晶胞如图所示,晶胞边长为a nm。设 为阿伏加德罗常数的值,则晶体密度的计算表达式为
为阿伏加德罗常数的值,则晶体密度的计算表达式为___________  ;晶胞中
;晶胞中 位于
位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为___________ nm。

(1)基态硅原子的价电子排布式为
(2)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物的结构和性质存在较大差异。化合物
 (三角锥形)和
(三角锥形)和 (平面形)的结构如图所示,则二者中N的杂化方式分别为
(平面形)的结构如图所示,则二者中N的杂化方式分别为
(3)白磷在氯气中燃烧可以得到
 和
和 ,其中气态
,其中气态 分子的空间结构为
分子的空间结构为(4)
 晶体的晶胞如图所示,晶胞边长为a nm。设
晶体的晶胞如图所示,晶胞边长为a nm。设 为阿伏加德罗常数的值,则晶体密度的计算表达式为
为阿伏加德罗常数的值,则晶体密度的计算表达式为 ;晶胞中
;晶胞中 位于
位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
名校
解题方法
3 .  具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用一直是科学研究的重要课题。
的合成及应用一直是科学研究的重要课题。
(1)以 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。
①基态Fe原子的电子排布式为___________ 。
②实际生产中采用铁的氧化物 、
、 ,使用前用
,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
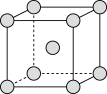
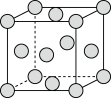
ⅰ.两种晶胞所含铁原子个数比为___________ 。
ⅱ.图1晶胞的棱长为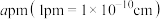 ,则其密度
,则其密度
___________  。
。
③我国科学家开发出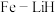 等双中心催化剂,在合成
等双中心催化剂,在合成 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能 :
: ,从原子结构角度解释原因
,从原子结构角度解释原因___________ 。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。

①1体积水可溶解1体积 ,1体积水可溶解约700体积
,1体积水可溶解约700体积 。
。 极易溶于水的原因是
极易溶于水的原因是___________ 。
②反应时,向饱和 溶液中先通入
溶液中先通入___________ 。
③ 分解得
分解得 。
。 空间结构为
空间结构为___________ 。
(3) 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
① 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为___________ 。
② 存在配位键,写出其体现配位键的结构式
存在配位键,写出其体现配位键的结构式___________ 。
③比较熔点:
___________  (填“>”或“<”)。
(填“>”或“<”)。
 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用一直是科学研究的重要课题。
的合成及应用一直是科学研究的重要课题。
(1)以
 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。①基态Fe原子的电子排布式为
②实际生产中采用铁的氧化物
 、
、 ,使用前用
,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:

ⅰ.两种晶胞所含铁原子个数比为
ⅱ.图1晶胞的棱长为
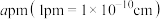 ,则其密度
,则其密度
 。
。③我国科学家开发出
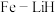 等双中心催化剂,在合成
等双中心催化剂,在合成 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能 :
: ,从原子结构角度解释原因
,从原子结构角度解释原因(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。

①1体积水可溶解1体积
 ,1体积水可溶解约700体积
,1体积水可溶解约700体积 。
。 极易溶于水的原因是
极易溶于水的原因是②反应时,向饱和
 溶液中先通入
溶液中先通入③
 分解得
分解得 。
。 空间结构为
空间结构为(3)
 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。| 元素 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为②
 存在配位键,写出其体现配位键的结构式
存在配位键,写出其体现配位键的结构式③比较熔点:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
名校
解题方法
4 . 合成氨是人类科学技术上的一项重大突破,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①氮原子的价电子轨道表示式为___________ 。
②自然固氮过程中生成的 的VSEPR模型名称为
的VSEPR模型名称为___________ 。
(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是_______ 。
②下列比较正确的是_______ 。
A.第一电离能Al>Mg>Na B.熔点:MgO>CaO
C.离子半径: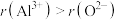 D.键角:H2O>NH3
D.键角:H2O>NH3
③ⅤA族元素的气态氢化物中NH3沸点最高的原因是_______ 。
④ 中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是
中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是_______ 、_______ 。

(3)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是___________ 原子。该晶体密度为___________  (写出表达式)。(底边长为anm,高为cnm,设阿伏加德罗常数的值为
(写出表达式)。(底边长为anm,高为cnm,设阿伏加德罗常数的值为 ,
, )
)

(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①氮原子的价电子轨道表示式为
②自然固氮过程中生成的
 的VSEPR模型名称为
的VSEPR模型名称为(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②下列比较正确的是
A.第一电离能Al>Mg>Na B.熔点:MgO>CaO
C.离子半径:
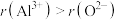 D.键角:H2O>NH3
D.键角:H2O>NH3③ⅤA族元素的气态氢化物中NH3沸点最高的原因是
④
 中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是
中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是
(3)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是
 (写出表达式)。(底边长为anm,高为cnm,设阿伏加德罗常数的值为
(写出表达式)。(底边长为anm,高为cnm,设阿伏加德罗常数的值为 ,
, )
)
您最近一年使用:0次
名校
解题方法
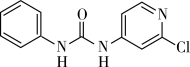
5 . 氯吡苯脲是一种常用的膨大剂,其结构简式如图,它是经国家批准使用的植物生长调节剂。
(1)氯元素基态原子核外电子的未成对电子数为_______ 。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为_______ 。
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲,其反应方程式如图:

反应过程中,每生成1mol氯吡苯脲,断裂_______ 个 键,断裂
键,断裂_______ 个 键。
键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为_______
②NH3分子的空间结构是_______ ,H2O中心原子的杂化类型是_______

(1)氯元素基态原子核外电子的未成对电子数为
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲,其反应方程式如图:

反应过程中,每生成1mol氯吡苯脲,断裂
 键,断裂
键,断裂 键。
键。(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为
②NH3分子的空间结构是
您最近一年使用:0次
名校
解题方法
6 . 磷、氮和硫的相关化合物在药物化学及农业化学领域应用广泛。回答下列问题:
(1) 分子空间结构为
分子空间结构为___________ , 与
与 反应生成
反应生成 ,
, 结构为
结构为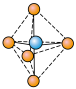 ,
, 是
是___________ (填“极性”或“非极性”)分子。
(2)氯吡苯脲是一种常用的膨大剂,其结构简式为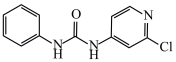 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。
①氯吡苯脲分子___________ (填“是”或“不是”)手性分子。
②氯吡苯脲分子中存在的作用力包括___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D. 键 E.配位键
键 E.配位键
(3)胆矾 可写成
可写成 ,其结构示意图如下:
,其结构示意图如下:
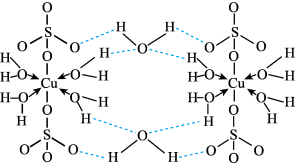
⑤该配合物的中心离子是___________ 。
②下列关于胆矾的说法正确的是___________ (填字母)。
A.基态 的价层电子排布式为
的价层电子排布式为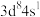
B.胆矾在不同温度下分步失去结晶水
C.根据结构图显示,胆矾在微观层次是平面结构
D.胆矾中的水分子间存在氢键
(1)
 分子空间结构为
分子空间结构为 与
与 反应生成
反应生成 ,
, 结构为
结构为 ,
, 是
是(2)氯吡苯脲是一种常用的膨大剂,其结构简式为
 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。①氯吡苯脲分子
②氯吡苯脲分子中存在的作用力包括
A.离子键 B.极性键 C.非极性键 D.
 键 E.配位键
键 E.配位键(3)胆矾
 可写成
可写成 ,其结构示意图如下:
,其结构示意图如下:
⑤该配合物的中心离子是
②下列关于胆矾的说法正确的是
A.基态
 的价层电子排布式为
的价层电子排布式为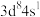
B.胆矾在不同温度下分步失去结晶水
C.根据结构图显示,胆矾在微观层次是平面结构
D.胆矾中的水分子间存在氢键
您最近一年使用:0次
2023-05-19更新
|
172次组卷
|
2卷引用:山西省运城市教育联盟2022-2023学年高二下学期5月月考化学试题
名校
解题方法
7 . 短周期主族元素X、Y、Z、G、T的原子序数依次增大,Z、G是金属元素且G的氧化物属于两性氧化物,T的原子序数是Y的2倍且T、Y的最低化合价相同。这5种元素的价电子数之和等于20,含Z元素的物质的焰色呈黄色。回答下列问题:
(1)X的最高价氧化物对应水化物的化学式为___________ 。位于元素周期表中s区的元素为___________ (填元素符号)。
(2)Y、Z、G、T的电负性由小到大的顺序为___________ (填元素符号)。
(3) 分子是
分子是___________ (填“极性”或“非极性”)分子。 分子中T的价层电子对数为
分子中T的价层电子对数为___________ 。
(4)Y和Z能形成既含离子键,又含共价键的化合物,其化学式为___________ 。
(5)V是由Y、Z、T组成的化合物,V的水溶液呈中性。则V的阴离子的空间构型___________ 。
(6)T的一种单质的结构如图所示: ,T原子杂化类型是
,T原子杂化类型是________ 。32gT的这种单质含σ键的数目为________ 。这种单质易溶于 ,不溶于水,其原因是
,不溶于水,其原因是_________ 。
(1)X的最高价氧化物对应水化物的化学式为
(2)Y、Z、G、T的电负性由小到大的顺序为
(3)
 分子是
分子是 分子中T的价层电子对数为
分子中T的价层电子对数为(4)Y和Z能形成既含离子键,又含共价键的化合物,其化学式为
(5)V是由Y、Z、T组成的化合物,V的水溶液呈中性。则V的阴离子的空间构型
(6)T的一种单质的结构如图所示:
 ,T原子杂化类型是
,T原子杂化类型是 ,不溶于水,其原因是
,不溶于水,其原因是
您最近一年使用:0次
2023-04-28更新
|
180次组卷
|
3卷引用:江西省南昌市等5地2022-2023学年高二下学期4月期中考试化学试题
解题方法
8 . 第四周期某些过渡元素在工业生产中有着极其重要的作用。
(1)铬是最硬的金属单质,被称为“不锈钢的添加剂”。写出Cr原子价电子排布图___________ 。
(2)钒广泛用于催化及钢铁工业,被称之为“工业的味精”。 常用作
常用作 转化为
转化为 的催化剂。
的催化剂。 分子VSEPR模型是
分子VSEPR模型是___________ ; 气态为单分子,
气态为单分子, 的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为
的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为___________ ;该结构中S-O键长有两类,一类键长约140pm,另一类键长约为160pm,较长的键为___________ (填图中字母a或者b)。

(3)镍是一种优良的有机反应催化剂,Ni能与CO形成正四面体形的配合物 ,其中配原子是C,原因是
,其中配原子是C,原因是___________ 。
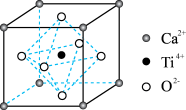
(4)钛称之为21世纪金属,具有一定的生物功能。钙钛矿( )晶体是工业获取钛的重要原料。
)晶体是工业获取钛的重要原料。 晶胞如图,晶胞参数为a nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为
晶胞如图,晶胞参数为a nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为___________ nm,与Ti紧邻的O个数为___________ 。

(5)在 晶胞结构的另一种表示形式中,Ti处于体心位置,则Ca处于
晶胞结构的另一种表示形式中,Ti处于体心位置,则Ca处于___________ 位置,O处于___________ 位置。
(1)铬是最硬的金属单质,被称为“不锈钢的添加剂”。写出Cr原子价电子排布图
(2)钒广泛用于催化及钢铁工业,被称之为“工业的味精”。
 常用作
常用作 转化为
转化为 的催化剂。
的催化剂。 分子VSEPR模型是
分子VSEPR模型是 气态为单分子,
气态为单分子, 的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为
的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为
(3)镍是一种优良的有机反应催化剂,Ni能与CO形成正四面体形的配合物
 ,其中配原子是C,原因是
,其中配原子是C,原因是(4)钛称之为21世纪金属,具有一定的生物功能。钙钛矿(
 )晶体是工业获取钛的重要原料。
)晶体是工业获取钛的重要原料。 晶胞如图,晶胞参数为a nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为
晶胞如图,晶胞参数为a nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为
(5)在
 晶胞结构的另一种表示形式中,Ti处于体心位置,则Ca处于
晶胞结构的另一种表示形式中,Ti处于体心位置,则Ca处于
您最近一年使用:0次
解题方法
9 . 胆矾(CuSO4·5H2O)可用于泳池杀菌消毒。回答下列问题:
(1)铜元素位于元素周期表的_____ 区,基态Cu原子的核外电子排布式为_____ 。
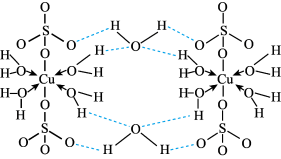
(2)CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如图:
① 的空间构型为
的空间构型为_____ ,其中硫原子的杂化方式为_____ 。
②硫酸铜晶体中Cu2+的配位数为_____ ,[Cu(H2O)4]2+中配位原子是_____ 。
③在上述结构示意图中,存在的化学键有_____ 。
(3)向CuSO4溶液中逐滴加入氨水,溶液最终变为深蓝色,原因是_____ 。
(1)铜元素位于元素周期表的
(2)CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如图:

①
 的空间构型为
的空间构型为②硫酸铜晶体中Cu2+的配位数为
③在上述结构示意图中,存在的化学键有
(3)向CuSO4溶液中逐滴加入氨水,溶液最终变为深蓝色,原因是
您最近一年使用:0次
2023-04-06更新
|
180次组卷
|
2卷引用:贵州省石阡县民族中学2022-2023学年高二下学期3月月考化学试题
名校
解题方法
10 . 周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,其次外层所有轨道均是全满状态。回答下列问题:
(1)b、c、d的简单离子半径最大的是___________ (填离子符号),e的晶胞结构中e配位数为___________ 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的电子式为___________ ;分子中既含有极性共价键、又含有非极性共价键的化合物是___________ (填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是___________ (任写一种);酸根呈三角锥结构的酸是___________ (填化学式)。
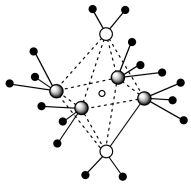
(4)e和c形成的一种离子化合物的晶体结构如图所示,则e离子的电荷为___________ 。

(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构。该化合物中,阴离子为___________ ,阳离子中存在的化学键类型有___________ 。
(1)b、c、d的简单离子半径最大的是
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的电子式为
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是
(4)e和c形成的一种离子化合物的晶体结构如图所示,则e离子的电荷为

(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构。该化合物中,阴离子为

您最近一年使用:0次



