名校
解题方法
1 . 三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示。___________ 原子提供孤电子对。
(2)此配离子中碳原子的杂化轨道类型有___________ 。

(2)此配离子中碳原子的杂化轨道类型有
您最近一年使用:0次
名校
解题方法
2 . 我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为_____ 。SiCl4可发生水解反应,机理如下: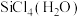 中Si采取的杂化类型为
中Si采取的杂化类型为_____ (填标号)。
(2)CO2分子中σ键和π键的比值_____ 。
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是_____ 。
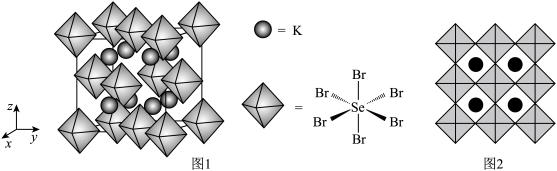
(4)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2._____ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为_____ nm(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为

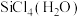 中Si采取的杂化类型为
中Si采取的杂化类型为(2)CO2分子中σ键和π键的比值
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(4)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2.
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
解题方法
3 . 已知: 与
与 在一定条件下可以发生如下反应,
在一定条件下可以发生如下反应,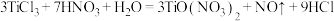 .回答下列问题:
.回答下列问题:
(1)基态钛原子的核外电子排布式为_____________ .
(2)N、H、O三种元素的电负性由大到小的顺序为_____________ .
(3)上述方程式中涉及的元素中属于P区元素的是_____________ (填元素符号).
(4) 的空间结构为
的空间结构为_____________ .
(5)肼 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被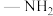 (氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下:
(氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下: .若该反应中有
.若该反应中有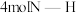 键断裂,则形成的
键断裂,则形成的 键有
键有_____________  .
.
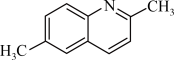
(6)由C、H、N三种元素形成的一种有机物的结构简式如下,则该物质中N原子的杂化方式为_____________ ,C原子的杂化方式为_____________ .
 与
与 在一定条件下可以发生如下反应,
在一定条件下可以发生如下反应,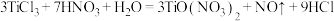 .回答下列问题:
.回答下列问题:(1)基态钛原子的核外电子排布式为
(2)N、H、O三种元素的电负性由大到小的顺序为
(3)上述方程式中涉及的元素中属于P区元素的是
(4)
 的空间结构为
的空间结构为(5)肼
 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被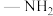 (氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下:
(氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下: .若该反应中有
.若该反应中有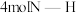 键断裂,则形成的
键断裂,则形成的 键有
键有 .
.(6)由C、H、N三种元素形成的一种有机物的结构简式如下,则该物质中N原子的杂化方式为
您最近一年使用:0次
名校
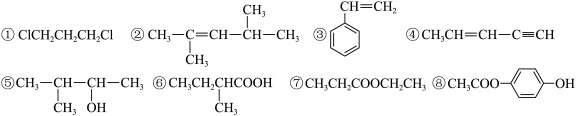
4 . 依据下列①~⑧有机物回答问题。________ 。
(2)①~④中,碳原子杂化类型均为 杂化的是
杂化的是________ (填数字序号)。分子②中最多有________ 个碳原子共平面。
(3)与⑤互为同系物且碳原子数最少的有机物的结构简式为________ 。
(4)⑤~⑧中互为同分异构体的是________ (填数字序号)。
(5)与⑦含有相同官能团且能发生银镜反应的同分异构体有________ 种(不考虑立体异构),其中含有3个甲基( )的同分异构体的结构简式为
)的同分异构体的结构简式为________ 。
(6)①在氢氧化钠溶液中发生水解反应的方程式为________ 。
(7)1mol⑧与足量氢氧化钠溶液共热,反应的化学方程式为________ 。
(2)①~④中,碳原子杂化类型均为
 杂化的是
杂化的是(3)与⑤互为同系物且碳原子数最少的有机物的结构简式为
(4)⑤~⑧中互为同分异构体的是
(5)与⑦含有相同官能团且能发生银镜反应的同分异构体有
 )的同分异构体的结构简式为
)的同分异构体的结构简式为(6)①在氢氧化钠溶液中发生水解反应的方程式为
(7)1mol⑧与足量氢氧化钠溶液共热,反应的化学方程式为
您最近一年使用:0次
5 . 甘氨酸(分子式C2H5NO2)分子中,共有___________ 个σ键。甘氨酸分子中C原子的杂化方式为___________ 。
A. sp B. sp2 C. sp3
甘氨酸钠中第一电离能最小的元素为___________ 。
A. C B. O C. Na D. N
A. sp B. sp2 C. sp3
甘氨酸钠中第一电离能最小的元素为
A. C B. O C. Na D. N
您最近一年使用:0次
6 . 2021年9月Science杂志发表了我国科学家利用CO2合成人工淀粉(ASAP)的论文。据介绍,该方法合成速率是玉米的8.5倍,能量转化效率是玉米的3.5倍。
已知人工合成淀粉的代谢途径(ASAP)可以简化表示为:
(2)写出符合下列条件的DHA的一种同分异构体_____ 。
①属于链状化合物②含有两种官能团③含有手性碳原子
已知人工合成淀粉的代谢途径(ASAP)可以简化表示为:
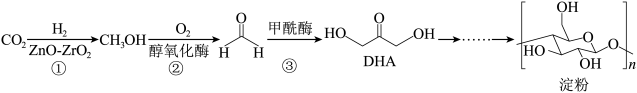
| A.碳原子采用sp3、sp2杂化 |
| B.每个链节含一个平面六边形 |
| C.每个链节中含有的官能团为羟基和醚键 |
| D.淀粉可以发生酯化反应 |
(2)写出符合下列条件的DHA的一种同分异构体
①属于链状化合物②含有两种官能团③含有手性碳原子
您最近一年使用:0次
名校
解题方法
7 . 完成下列问题。
(1)现有下列各组物质: 和
和
⑦ 和
和
互为同分异构体的是_______ ,属于同一种物质的是______ ,互为同系物的是_______ 。 (填序号)
(2)请按照官能团的种类不同将下列有机化合物进行分类:_____ ,属于醛的是_____ ,属于酯的是_____ 。
(3)有机物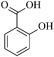 中官能团的名称为
中官能团的名称为_____ 、_____ 。
(4)某新型有机物M的结构如图所示。有关M的说法错误的是______。
(1)现有下列各组物质:
① 和
和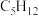 ②
② 和
和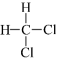 ③
③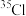 和
和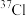 ④石墨和金刚石
④石墨和金刚石
⑤ 和
和
 和
和
⑦
 和
和
互为同分异构体的是
(2)请按照官能团的种类不同将下列有机化合物进行分类:
A.HC≡C—CH2CH3 B.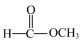 C.
C.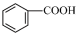 D.
D. E.
E. F.
F.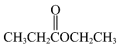 G.
G. H.
H.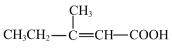
(3)有机物
 中官能团的名称为
中官能团的名称为(4)某新型有机物M的结构如图所示。有关M的说法错误的是______。
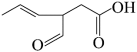
A.M的分子式为 C7H12O3 C7H12O3 | B.M中含有三种官能团 |
| C.M分子中含有手性碳原子 | D.M中碳原子杂化方式有两种 |
您最近一年使用:0次
名校
解题方法
8 . 有机物是生命产生的物质基础,所有的生命体都含有机化合物,按要求回答下列问题。
(1)下列有机物互为同分异构体的是___________ ,互为同系物的是___________ 。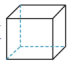 )中的碳原子的杂化类型为
)中的碳原子的杂化类型为___________ 。
(3)有机物的沸点: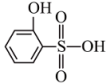
___________ 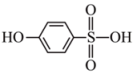 (填“>”、“<”或“=”),有机物
(填“>”、“<”或“=”),有机物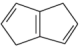 中σ键和π键的数目比为
中σ键和π键的数目比为___________ ,其一氯代物有___________ 种。
(4)碳酸H2CO3虽含有碳元素,但不是有机物。已知它的钾盐K2CO3在水中的溶解度大于KHCO3在水中的溶解度,根据其结构分析可能的原因是___________ 。
(1)下列有机物互为同分异构体的是
①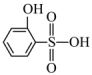 与
与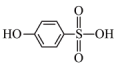 ②
②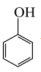 与
与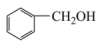 ③
③ 与
与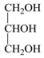
④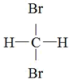 和
和 ⑤CH3COOH与CH3CH2CH2COOH
⑤CH3COOH与CH3CH2CH2COOH
 )中的碳原子的杂化类型为
)中的碳原子的杂化类型为(3)有机物的沸点:

 (填“>”、“<”或“=”),有机物
(填“>”、“<”或“=”),有机物 中σ键和π键的数目比为
中σ键和π键的数目比为(4)碳酸H2CO3虽含有碳元素,但不是有机物。已知它的钾盐K2CO3在水中的溶解度大于KHCO3在水中的溶解度,根据其结构分析可能的原因是
您最近一年使用:0次
名校
解题方法
9 . 原子是肉眼和一般仪器都看不到的微粒,科学家们是根据可观察、可测量的宏观实验事实,经过分析和推理,揭示了原子结构的奥秘。
(1)下列说法中正确的个数是___________。
①同一原子中,s电子的能量总是低于p电子的能量
②任何s轨道形状均是球形,只是能层不同,球的半径大小不同而己
③2p、3p、4p能级的轨道数依次增多
④原子核外电子排布,先排满K层再排L层,排满M层再排N层
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ 、___________ 。___________ 光谱(选填“发射”或“吸收”)。
(4)镍铬钢抗腐蚀性能强,基态铬原子的价层电子排布式为___________ 。
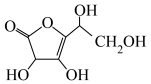
(5)已知维生素C的一种同分异构体结构简式如图,则该分子中碳原子的轨道杂化类型为___________ ;分子中有___________ 个σ键和___________ 个π键。
(1)下列说法中正确的个数是___________。
①同一原子中,s电子的能量总是低于p电子的能量
②任何s轨道形状均是球形,只是能层不同,球的半径大小不同而己
③2p、3p、4p能级的轨道数依次增多
④原子核外电子排布,先排满K层再排L层,排满M层再排N层
⑤基态碳原子的轨道表示式: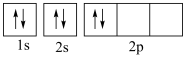
⑦用电子式表示 的形成过程:
的形成过程: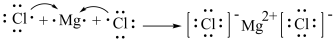
⑧基态钒原子的结构示意图为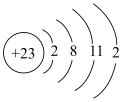
| A.2 | B.3 | C.4 | D.5 |
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.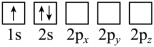 B.
B.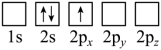
C. 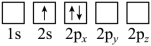 D.
D.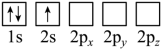
(4)镍铬钢抗腐蚀性能强,基态铬原子的价层电子排布式为
(5)已知维生素C的一种同分异构体结构简式如图,则该分子中碳原子的轨道杂化类型为
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)羰基硫( )与
)与 的结构相似,羰基硫(
的结构相似,羰基硫( )分子的结构式为
)分子的结构式为________ ;
(2) 中
中 的空间结构呈
的空间结构呈________ ,与 空间结构相同的一种阴离子的化学式
空间结构相同的一种阴离子的化学式________ 。
(3) 是储氢材料,其由
是储氢材料,其由 和
和 (H为-1价)构成,
(H为-1价)构成, 中心原子B杂化轨道方式为
中心原子B杂化轨道方式为________ 。 中不存在的作用力有
中不存在的作用力有________ 。
A.离子键 B.极性共价键 C.非极性共价键 D.分子间作用力
(4)已知双键成键电子对之间的排斥作用大于单键成键电子对之间的排斥作用, 分子结构如图
分子结构如图 所示,键角大小关系为:
所示,键角大小关系为:
________  (填“>”或“<”)。
(填“>”或“<”)。
(1)羰基硫(
 )与
)与 的结构相似,羰基硫(
的结构相似,羰基硫( )分子的结构式为
)分子的结构式为(2)
 中
中 的空间结构呈
的空间结构呈 空间结构相同的一种阴离子的化学式
空间结构相同的一种阴离子的化学式(3)
 是储氢材料,其由
是储氢材料,其由 和
和 (H为-1价)构成,
(H为-1价)构成, 中心原子B杂化轨道方式为
中心原子B杂化轨道方式为 中不存在的作用力有
中不存在的作用力有A.离子键 B.极性共价键 C.非极性共价键 D.分子间作用力
(4)已知双键成键电子对之间的排斥作用大于单键成键电子对之间的排斥作用,
 分子结构如图
分子结构如图 所示,键角大小关系为:
所示,键角大小关系为:
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次



