解题方法
1 . (1)氮化硼(BN)是一种用途广泛的无机非金属材料,常见有立方氮化硼与六方氮化硼两种结构。六方氮化硼是一种白色难熔的耐高温物质,它具有类似石墨层状结构,被成为白石墨,常用作润滑剂,虽然六方氮化硼结构与石墨相似,但六方氮化硼却并不导电,具有优良的绝缘性能。立方氮化硼是棕色或暗红色的晶体,为闪锌矿结构,硬度仅次于金刚石,具有很高的热稳定性和化学惰性,因此,立方氮化硼磨具的磨削性能十分优异。
①写出氮化硼中B和N的基态电子排布式_______ 。
②氮化硼非常稳定,在红热时才能与水蒸气发生水解反应,写出该化学方程式_______ 。
③H3BO3是一元酸,试从分子结构角度解释原因_______ 。
④判断六方氮化硼中B与N的杂化类型_______ 、_______ 。
⑤从化学键角度解释为什么六方氮化硼的结构与石墨相似,但六方氮化硼却并不导电_______ 。
(2)PH3可由白磷(P4)和氢气反应生成。已知键能:P-P:213kJ·mol-1,H-H:435kJ·mol-1,P-H:326kJ·mol-1。
①画出白磷的结构式(空间结构)_______ 。
②写出所对应反应的化学方程式_______ 。
③根据键能计算该反应的焓变(反应物和产物均为气态,写出简要的计算过程)_______ 。
(3)锡的利用在我国有几千年历史,青铜器中就含有锡,殷墟中还出土过锡制品。锡的熔点232℃,有两种常见的同素异形体一白锡和灰锡,二者在一定温度下可以相互转化。
①锡的密度为7.28g·cm-3,晶胞参数a=583pmc=318pm,延展性好,质软。通过计算求出一个白锡晶胞中的锡原子数_______ 。
②灰锡的密度为5.75g·cm-3,有金刚石的结构。灰锡和白锡的部分热力学数据如下:
通过计算说明常温(25℃)时,灰锡和白锡哪种更稳定_______ ;
③锡做的茶叶罐不能放在冰箱中冷冻保存,通过计算说明原因_______ 。
①写出氮化硼中B和N的基态电子排布式
②氮化硼非常稳定,在红热时才能与水蒸气发生水解反应,写出该化学方程式
③H3BO3是一元酸,试从分子结构角度解释原因
④判断六方氮化硼中B与N的杂化类型
⑤从化学键角度解释为什么六方氮化硼的结构与石墨相似,但六方氮化硼却并不导电
(2)PH3可由白磷(P4)和氢气反应生成。已知键能:P-P:213kJ·mol-1,H-H:435kJ·mol-1,P-H:326kJ·mol-1。
①画出白磷的结构式(空间结构)
②写出所对应反应的化学方程式
③根据键能计算该反应的焓变(反应物和产物均为气态,写出简要的计算过程)
(3)锡的利用在我国有几千年历史,青铜器中就含有锡,殷墟中还出土过锡制品。锡的熔点232℃,有两种常见的同素异形体一白锡和灰锡,二者在一定温度下可以相互转化。
①锡的密度为7.28g·cm-3,晶胞参数a=583pmc=318pm,延展性好,质软。通过计算求出一个白锡晶胞中的锡原子数
②灰锡的密度为5.75g·cm-3,有金刚石的结构。灰锡和白锡的部分热力学数据如下:
 /kJ·mol-1 /kJ·mol-1 |  J/-1·K-1·mol-1 J/-1·K-1·mol-1 | |
| Sn(灰) Sn(白) | -2.12 0 | 44.15 51.55 |
通过计算说明常温(25℃)时,灰锡和白锡哪种更稳定
③锡做的茶叶罐不能放在冰箱中冷冻保存,通过计算说明原因
您最近一年使用:0次
真题
解题方法
2 . KH2PO4晶体具有优异的非线性光学性能。我国科学工作者制备的超大KH2PO4晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是__ (填离子符号)。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为___ 。
(3)已知有关氮、磷的单键和三键的键能(kJ•mol-1)如表:
___ ,其中P采取___ 杂化方式。
(5)与PO 电子总数相同的等电子体的分子式为
电子总数相同的等电子体的分子式为__ 。
(6)磷酸通过分子间脱水缩合形成多磷酸,如:___ 。
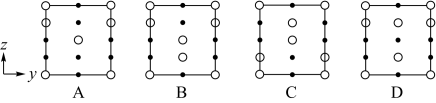
(7)分别用○、●表示H2PO 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置:
、K+在晶胞xz面、yz面上的位置:__ g•cm-3(写出表达式)。
②晶胞在x轴方向的投影图为__ (填标号)。
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为(3)已知有关氮、磷的单键和三键的键能(kJ•mol-1)如表:
| N—N | N≡N | P—P | P≡P |
| 193 | 946 | 197 | 489 |
从能量角度看,氮以N2、而白磷以P4(结构式可表示为 )形式存在的原因是
)形式存在的原因是
(5)与PO
 电子总数相同的等电子体的分子式为
电子总数相同的等电子体的分子式为(6)磷酸通过分子间脱水缩合形成多磷酸,如:

(7)分别用○、●表示H2PO
 和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 、K+在晶胞xz面、yz面上的位置:
、K+在晶胞xz面、yz面上的位置:
②晶胞在x轴方向的投影图为
您最近一年使用:0次
2021-06-09更新
|
10102次组卷
|
12卷引用:2021年新高考河北化学高考真题
2021年新高考河北化学高考真题(已下线)专题14 物质结构与性质-备战2022年高考化学学霸纠错(全国通用)2021年河北省高考化学试卷变式题10-18题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷15题 物质结构与性质综合题-备战2022年高考化学临考题号押题(新高考通版)广东省广州市天河区2022届高三第三次模拟考试化学试题(已下线)专题18 物质结构与性质(综合题)-三年(2020-2022)高考真题分项汇编(已下线)专题20 结构与性质(已下线)专题20 结构与性质
解题方法
3 . 元素B、Ti、Fe等形成的材料在工业、生活、国防中有很大的作用。
(1)基态Fe原子的核外空间运动状态有___________ 种,实验室常用邻二氮菲( )检验Fe2+,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子成键原子轨道为
)检验Fe2+,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子成键原子轨道为___________ ,若用邻二氮菲检验Fe2+,选择pH范围为2~9的原因是___________ 。
(2)2019年中国科学家合成了白光材料Ba2[Sn(OH)6][B(OH)4]2,其所含的化学键有___________ (填字母),B的价层电子对数为___________ ,B、O、Sn、Ba的电负性大小顺序是___________ 。
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键 F.π
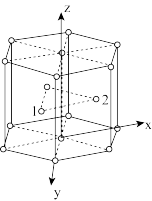
(3)“21世纪金属”钛(Ti)在常温下以六方最密堆积方式连接,结构如图所示,原子1的配位数为___________ ,原子2的分数坐标为___________ ,若原子1和原子2间距为dpm,令阿伏加德罗常数的值为NA,则该晶体密度为___________ g/cm3 (列出计算式)。
(1)基态Fe原子的核外空间运动状态有
 )检验Fe2+,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子成键原子轨道为
)检验Fe2+,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子成键原子轨道为(2)2019年中国科学家合成了白光材料Ba2[Sn(OH)6][B(OH)4]2,其所含的化学键有
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键 F.π
(3)“21世纪金属”钛(Ti)在常温下以六方最密堆积方式连接,结构如图所示,原子1的配位数为

您最近一年使用:0次
名校
解题方法
4 . 银离子导体是发现最早的固体电解质,同时也是应用面最广的固体电解质,如制作库仑计、电子开关、压敏元件、气敏传感器、记忆元件、电容器等电化学器件。
回答以下问题:
(1)Ag+的价层电子排布式为4d10,写出Ag在周期表中的位置___ 。
(2)第三周期各元素的氯化物熔点、沸点数据如下:
请解释第三周期氯化物沸点从左到右变化的原因:___ 。
(3)偏高碘酸HIO4是无机非混合酸中氧化性极强的酸之一,可将Mn氧化为HMnO4,将Fe2+氧化为H2FeO4。HIO4的中心原子杂化形式是__ ,构成HIO4的三种元素电负性大小顺序是___ ,在HIO4晶体中存在___ (填字母)
A.离子键 B.极性共价键 C.非极性共价键 D.分子间作用力 E.σ键 F.π键
(4)室温下,AgI属于六方ZnS结构,其中S原子作六方密堆积,Zn原子填充在半数的四面体空隙中。则AgI晶体中I原子的配位数是___ 。
(5)400℃以上AgI固体的导电能力是室温的上万倍,可与电解质溶液媲美,经研究发现其在146℃以上转化为一种奇特结构:α—AgI,I-作体心立方堆积,而Ag+则选择性填入I-构成的三类孔隙中:八面体孔隙(O)、四面体孔隙(T)和三角形孔隙(Tr),则平均每个α—AgI晶胞中的Ag+数是___ ,I-与I-构成的三类孔隙堆积之比为I-:O:T:Tr=1:__ :__ :12。

回答以下问题:
(1)Ag+的价层电子排布式为4d10,写出Ag在周期表中的位置
(2)第三周期各元素的氯化物熔点、沸点数据如下:
| NaCl | MgCl2 | AlCl3 | SiCl4 | PCl3 | S2Cl2 | |
| 熔点/K | 1074 | 987 | 465 | 205 | 181 | 193 |
| 沸点/K | 1686 | 1691 | 453(升华) | 216 | 349 | 411 |
请解释第三周期氯化物沸点从左到右变化的原因:
(3)偏高碘酸HIO4是无机非混合酸中氧化性极强的酸之一,可将Mn氧化为HMnO4,将Fe2+氧化为H2FeO4。HIO4的中心原子杂化形式是
A.离子键 B.极性共价键 C.非极性共价键 D.分子间作用力 E.σ键 F.π键
(4)室温下,AgI属于六方ZnS结构,其中S原子作六方密堆积,Zn原子填充在半数的四面体空隙中。则AgI晶体中I原子的配位数是
(5)400℃以上AgI固体的导电能力是室温的上万倍,可与电解质溶液媲美,经研究发现其在146℃以上转化为一种奇特结构:α—AgI,I-作体心立方堆积,而Ag+则选择性填入I-构成的三类孔隙中:八面体孔隙(O)、四面体孔隙(T)和三角形孔隙(Tr),则平均每个α—AgI晶胞中的Ag+数是

您最近一年使用:0次
2021-05-18更新
|
645次组卷
|
3卷引用:宁夏银川一中等17校2021届高三下学期5月联考理综化学试题
20-21高三上·四川自贡·阶段练习
解题方法
5 . 氮化物应用广泛,如叠氮化钠(NaN3)是典型的高能量密度含能材料,氮化硼是特殊的耐磨和切削材料,氮化铬、氮化钼等过渡金属氮化物常用作高强度材料。回答下列问题:
(1)Na、N、B中,原子半径由大到小的顺序是___________ 。
(2)基态N原子价层电子的电子排布图为___________ 。基态铬原子核外未成对电子数为___________ 。
(3)NaN3中阴离子N 是直线型离子。1个N
是直线型离子。1个N 中的σ键数目为
中的σ键数目为___________ 。分子或离子中的大π键可用符号Π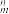 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π ),则N
),则N 中的大π键应表示为
中的大π键应表示为___________ 。
(4)石墨型(BN)x转变为金刚石型(BN)x时,B原子的杂化轨道类型由___________ 变为___________ 。金刚石型(BN)x的硬度比金刚石大,推测其原因是___________ 。
(5)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。
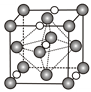
氮化钼的化学式为___________ ,如果让Li+填入氮化钼晶体的八面体空隙,一个晶胞最多可以填入___________ 个Li+。氮化钼晶胞边长为a nm,晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)Na、N、B中,原子半径由大到小的顺序是
(2)基态N原子价层电子的电子排布图为
(3)NaN3中阴离子N
 是直线型离子。1个N
是直线型离子。1个N 中的σ键数目为
中的σ键数目为 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π ),则N
),则N 中的大π键应表示为
中的大π键应表示为(4)石墨型(BN)x转变为金刚石型(BN)x时,B原子的杂化轨道类型由
(5)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。

氮化钼的化学式为
您最近一年使用:0次
18-19高二下·山西忻州·期中
6 . 碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:

回答下列问题:
(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为_________ 。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________ 、________ 。
(3)C60属于_________ 晶体,石墨属于________ 晶体。
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154 pm,其原因是金刚石中只存在C—C间的________ 共价键,而石墨层内的C—C间不仅存在_________ 共价键,还有_________ 键。
(5)金刚石晶胞含有________ 个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=________ a,列式表示碳原子在晶胞中的空间占有率________ (用含π分数形式表示,不要求写成百分数)。

回答下列问题:
(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为
(3)C60属于
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154 pm,其原因是金刚石中只存在C—C间的
(5)金刚石晶胞含有
您最近一年使用:0次
2018·河北衡水·模拟预测
名校
解题方法
7 . 铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4[UO2(CO3)3]等。
回答下列问题:
(1)UF4用Mg 或Ca还原可得金属铀。与钙同周期基态原子的未成对电子数为2 的元素共有___ 种;原子序数为镁元素的二倍的元素的基态原子价电子排布图为_______ 。
(2)已知:2UO2+5NH4HF2 2UF4·NH4F+3NH3↑+ 4H2O ↑
2UF4·NH4F+3NH3↑+ 4H2O ↑
HF2-的结构为[F-H…F]-
①NH4HF2中含有的化学键有__ (填选项字母)。
A.氢键 B.配位键 C.共价键 D.离子键 E.金属键
②与氧同周期,且第一电离能比氧大的元素有______ 种。
(3)已知:3(NH4)4[UO2(CO3)3] 3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
①写出与NH4+互为等电子体的一种分子和一种离子的化学式______ 、_______ 。
②物质 中与CO
中与CO 的碳原子杂化类型相同和不同的碳原子的个数比为
的碳原子杂化类型相同和不同的碳原子的个数比为______ 。
③分解所得的气态化合物的分子键角由小到大的顺序为__ (填化学式)
(4)C元素与N元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4 个碳原子位于立方体的面心,4 个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。

①晶胞中C 原子的配位数为______ 。该晶体硬度超过金刚石的原因是_________ 。
②已知该晶胞的密度为d g/cm3,N原子的半径为r1cm,C原子的半径为r2cm,设NA为阿伏伽德罗常数,则该晶胞的空间利用率为_______ (用含d、r1、r2、NA的代数式表示,不必化简)。
回答下列问题:
(1)UF4用Mg 或Ca还原可得金属铀。与钙同周期基态原子的未成对电子数为2 的元素共有
(2)已知:2UO2+5NH4HF2
 2UF4·NH4F+3NH3↑+ 4H2O ↑
2UF4·NH4F+3NH3↑+ 4H2O ↑HF2-的结构为[F-H…F]-
①NH4HF2中含有的化学键有
A.氢键 B.配位键 C.共价键 D.离子键 E.金属键
②与氧同周期,且第一电离能比氧大的元素有
(3)已知:3(NH4)4[UO2(CO3)3]
 3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑
3UO2+10NH3↑+9CO2↑+N2↑+9H2O ↑①写出与NH4+互为等电子体的一种分子和一种离子的化学式
②物质
 中与CO
中与CO 的碳原子杂化类型相同和不同的碳原子的个数比为
的碳原子杂化类型相同和不同的碳原子的个数比为③分解所得的气态化合物的分子键角由小到大的顺序为
(4)C元素与N元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4 个碳原子位于立方体的面心,4 个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。

①晶胞中C 原子的配位数为
②已知该晶胞的密度为d g/cm3,N原子的半径为r1cm,C原子的半径为r2cm,设NA为阿伏伽德罗常数,则该晶胞的空间利用率为
您最近一年使用:0次
2018-04-16更新
|
1703次组卷
|
3卷引用:第1周 晚练题-备战2022年高考化学周测与晚练(新高考专用)
8 . 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式:______________________________ 。
(2)B元素基态原子中能量最高的电子,其电子云在空间有__________ 个方向,原子轨道呈_______ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背
该同学所画的电子排布图违背___________________ 。
(4)G位于________ 族________ 区,该元素的核外电子排布式为_________________ 。
(5)DE3中心原子的杂化方式为____________ ,用价层电子对互斥理论推测其空间构型为__________ 。
(6)检验F元素的方法是____________ ,请用原子结构的知识解释产生此现象的原因:_____________ 。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738 kJ·mol-1 I2=1451 kJ·mol-1 I3=7733 kJ·mol-1 I4=10540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B元素基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 该同学所画的电子排布图违背
该同学所画的电子排布图违背(4)G位于
(5)DE3中心原子的杂化方式为
(6)检验F元素的方法是
您最近一年使用:0次
2016-12-09更新
|
500次组卷
|
2卷引用:山西省忻州市岢岚县中学2020-2021学年高二下学期4月月考化学试题



