名校
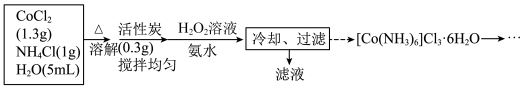
1 . 三氯化六氨合钴(III)([Co(NH3)6]Cl3)是一种重要的含钴配合物,由CoCl2制备它的流程如下:
回答下列问题:
(1)制备装置如图所示,装混合液的仪器名称是___________ ;___________ 。
(3)实验开始,向混合液加入H2O2溶液与氨水时,应最先打开活塞___________ (填字母代号);原料中加入NH4Cl有利于后续钴离子的络合反应,其原因是___________ 。加入所有试剂后,水浴的温度控制在55℃左右,反应约30分钟,温度控制在55℃左右的原因是___________ ;
(4)CoCl2制备[Co(NH3)6]Cl3的总反应化学方程式为___________ 。
(5)由滤渣获取[Co(NH3)6]Cl3•6H2O的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥,得到产品2.14g。
①下列选项合理的是___________ (填标号)。
A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为水 C.甲为浓盐酸,乙为乙醇
②该反应的产率为___________
回答下列问题:
(1)制备装置如图所示,装混合液的仪器名称是

(3)实验开始,向混合液加入H2O2溶液与氨水时,应最先打开活塞
(4)CoCl2制备[Co(NH3)6]Cl3的总反应化学方程式为
(5)由滤渣获取[Co(NH3)6]Cl3•6H2O的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥,得到产品2.14g。
①下列选项合理的是
A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为水 C.甲为浓盐酸,乙为乙醇
②该反应的产率为
您最近半年使用:0次
2023-11-11更新
|
180次组卷
|
2卷引用:福建省福州市八县一中2023-2024学年高三上学期11月期中化学试题
名校
解题方法
2 . 实验室以 为原料制备
为原料制备 并进行定量分析。
并进行定量分析。
已知:
 。
。
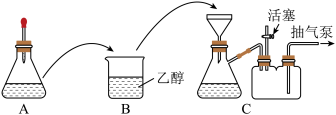
(1)配制溶液。称取一定质量的 晶体,放入锥形瓶中,溶解后滴加氨水,装置如图A所示(胶头滴管中吸有氨水)。
晶体,放入锥形瓶中,溶解后滴加氨水,装置如图A所示(胶头滴管中吸有氨水)。
①与烧杯相比,使用装置A作为反应器的优点是___________ 。
②滴加氨水时,有浅蓝色沉淀 生成;继续滴加氨水,沉淀消失,得到深蓝色
生成;继续滴加氨水,沉淀消失,得到深蓝色 溶液。写出
溶液。写出 与氨水反应的离子方程式:
与氨水反应的离子方程式:___________ 。
(2)制备晶体。将A中溶液转移至B中,析出 晶体:将B中混合物转移至装置C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,干燥。两次转移均需洗涤原容器,目的是
晶体:将B中混合物转移至装置C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,干燥。两次转移均需洗涤原容器,目的是___________ 。
(3)废液回收。从含有 、乙醇和氨水的废液中回收乙醇并获得
、乙醇和氨水的废液中回收乙醇并获得 、
、 的混合溶液,应加入的试剂是
的混合溶液,应加入的试剂是___________ (填化学式),回收乙醇的实验方法为___________ 。
(4)测定晶体中 的含量。请补充完整实验方案:取一定质量的
的含量。请补充完整实验方案:取一定质量的 晶体,加适量蒸馏水溶解
晶体,加适量蒸馏水溶解___________ ,干燥,灼烧至恒重。(须使用的试剂:蒸馏水, 溶液,
溶液,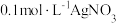 溶液)
溶液)
 为原料制备
为原料制备 并进行定量分析。
并进行定量分析。已知:

 。
。
(1)配制溶液。称取一定质量的
 晶体,放入锥形瓶中,溶解后滴加氨水,装置如图A所示(胶头滴管中吸有氨水)。
晶体,放入锥形瓶中,溶解后滴加氨水,装置如图A所示(胶头滴管中吸有氨水)。①与烧杯相比,使用装置A作为反应器的优点是
②滴加氨水时,有浅蓝色沉淀
 生成;继续滴加氨水,沉淀消失,得到深蓝色
生成;继续滴加氨水,沉淀消失,得到深蓝色 溶液。写出
溶液。写出 与氨水反应的离子方程式:
与氨水反应的离子方程式:(2)制备晶体。将A中溶液转移至B中,析出
 晶体:将B中混合物转移至装置C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,干燥。两次转移均需洗涤原容器,目的是
晶体:将B中混合物转移至装置C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,干燥。两次转移均需洗涤原容器,目的是(3)废液回收。从含有
 、乙醇和氨水的废液中回收乙醇并获得
、乙醇和氨水的废液中回收乙醇并获得 、
、 的混合溶液,应加入的试剂是
的混合溶液,应加入的试剂是(4)测定晶体中
 的含量。请补充完整实验方案:取一定质量的
的含量。请补充完整实验方案:取一定质量的 晶体,加适量蒸馏水溶解
晶体,加适量蒸馏水溶解 溶液,
溶液,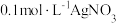 溶液)
溶液)
您最近半年使用:0次
名校
3 . 三氯化六氨合钴 是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生
是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生 、
、 。某实验小组利用下列方法制备
。某实验小组利用下列方法制备 并测定其氨的含量。
并测定其氨的含量。
I.制备晶体:
向锥形瓶中加入适量研细的 、
、 和蒸馏水,加热溶解后加入活性炭催化剂,冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀。抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤。在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥。
和蒸馏水,加热溶解后加入活性炭催化剂,冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀。抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤。在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥。
Ⅱ.氨含量的测定(装置如图所示):
称取mg样品于锥形瓶中,加水溶解。在另一锥形瓶中加入 标准HCl溶液并置于冰水浴中,从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右。然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中。取出锥形瓶,加入指示剂,用
标准HCl溶液并置于冰水浴中,从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右。然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中。取出锥形瓶,加入指示剂,用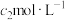 NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液
NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液 。
。

回答下列问题:
(1)Co元素在元素周期表的位置为______ ,基态 的价层电子排布式为
的价层电子排布式为_______ 。
(2)制备实验中,先加入过量的 ,冷却后,再加入浓氨水,生成
,冷却后,再加入浓氨水,生成 的化学方程式为
的化学方程式为___________ 。
(3)步骤I中水浴加热,恒温在60℃的原因为___________ ;将制得晶体过滤、洗涤、干燥,其中洗涤的具体操作是___________ 。
(4)由氨含量的测定实验,可得样品中氨的质量分数(以 计算)为
计算)为___________ 。(用含 、
、 、
、 、
、 、m的代数式表示):若省略“纯水冲洗导管内外”,会使测定结果
、m的代数式表示):若省略“纯水冲洗导管内外”,会使测定结果___________ (填“偏高”“偏低”或“无影响”)。
(5)小组成员查阅资料得知,若不加活性炭催化剂,制备产物主要是 。现有10mL浓度为
。现有10mL浓度为 的
的 或
或 溶液,用等浓度的
溶液,用等浓度的 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液20mL,则该溶液为
溶液20mL,则该溶液为____ {填“ ”或“
”或“ ”}溶液。
”}溶液。
 是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生
是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生 、
、 。某实验小组利用下列方法制备
。某实验小组利用下列方法制备 并测定其氨的含量。
并测定其氨的含量。I.制备晶体:
向锥形瓶中加入适量研细的
 、
、 和蒸馏水,加热溶解后加入活性炭催化剂,冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀。抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤。在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥。
和蒸馏水,加热溶解后加入活性炭催化剂,冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀。抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤。在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥。Ⅱ.氨含量的测定(装置如图所示):
称取mg样品于锥形瓶中,加水溶解。在另一锥形瓶中加入
 标准HCl溶液并置于冰水浴中,从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右。然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中。取出锥形瓶,加入指示剂,用
标准HCl溶液并置于冰水浴中,从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右。然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中。取出锥形瓶,加入指示剂,用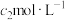 NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液
NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液 。
。
回答下列问题:
(1)Co元素在元素周期表的位置为
 的价层电子排布式为
的价层电子排布式为(2)制备实验中,先加入过量的
 ,冷却后,再加入浓氨水,生成
,冷却后,再加入浓氨水,生成 的化学方程式为
的化学方程式为(3)步骤I中水浴加热,恒温在60℃的原因为
(4)由氨含量的测定实验,可得样品中氨的质量分数(以
 计算)为
计算)为 、
、 、
、 、
、 、m的代数式表示):若省略“纯水冲洗导管内外”,会使测定结果
、m的代数式表示):若省略“纯水冲洗导管内外”,会使测定结果(5)小组成员查阅资料得知,若不加活性炭催化剂,制备产物主要是
 。现有10mL浓度为
。现有10mL浓度为 的
的 或
或 溶液,用等浓度的
溶液,用等浓度的 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液20mL,则该溶液为
溶液20mL,则该溶液为 ”或“
”或“ ”}溶液。
”}溶液。
您最近半年使用:0次
名校
解题方法
4 . 完成下述实验,装置或试剂不正确的是
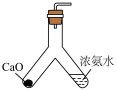 |  | 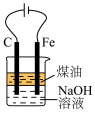 | 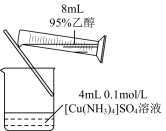 |
| A. 制备NH3 | B. 测量 O2体积 | C. 制备Fe(OH)2 | D.制备晶体Cu(NH3)4SO4·H2O |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 . 甘氨酸亚铁晶体是一种新型的固体整合补铁剂。其实验室合成路线为:
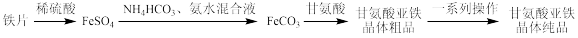
已知:
①相关物质的信息如下表所示
②含有多个配位原子的配体与同一中心离子通过整合配位成环而形成的配合物称为整合物。
(一)FeCO3固体的制备
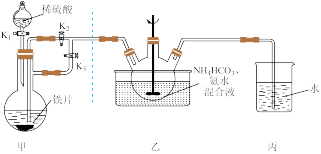
(1)实验开始时应先开K1和___________ ,关___________ (填“K2”或“K3”);一段时间后,改变开关状态,生成FeCO3。
(2)三颈瓶中生成FeCO3沉淀的离子方程式为___________ 。
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的NaOH溶液调节pH为5左右,pH过高或过低都会使产率下降,原因是___________ 。
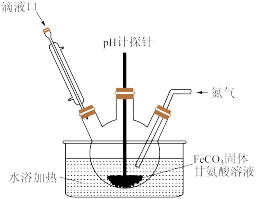
(4)当FeCO3固体完全溶解后,再通过滴液口加入乙醇,其作用是___________ 。
(5)反应结束后,过滤出产品粗品,依次用___________ 、___________ (填序号)洗涤,再经过一系列操作得纯品。
a. 热水 b. 冰水 c. 乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800 g于锥形瓶中,加3mol/LH2SO4溶液15 mL将样品溶解完全后,加入指示剂,立即用0.1000 mol/L(NH4)2Ce(SO4)3标准液滴定至终点,用去标准液20.20 mL(反应为Ce4++Fe2+=Ce3++Fe3+)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20 mL。
回答下列问题:
(6)滴定时应选择___________ 滴定管。
(7)甘氨酸亚铁晶体中Fe的质量分数为___________ %(保留小数点后一位)。
(8)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有H2NCH2COO-和Fe2+;Fe2+的配位数为6,且存在五元螯合环;该配合物整体量中心对称,甘氨酸亚铁晶体的结构简式为___________ 。
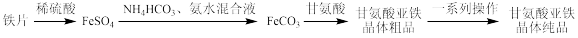
已知:
①相关物质的信息如下表所示
| 物质 | 化学式 | 摩尔质量 | 性质 |
| 甘氨酸 | H2NCH2COOH | 75g/mol | 两性物质,易溶于水,微溶于乙醇 |
| 甘氨酸亚铁晶体 | 易溶于水,溶解度随温度升高而增大;难溶于乙醇,在潮湿的空气中易被氧化 |
(一)FeCO3固体的制备

(1)实验开始时应先开K1和
(2)三颈瓶中生成FeCO3沉淀的离子方程式为
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的NaOH溶液调节pH为5左右,pH过高或过低都会使产率下降,原因是

(4)当FeCO3固体完全溶解后,再通过滴液口加入乙醇,其作用是
(5)反应结束后,过滤出产品粗品,依次用
a. 热水 b. 冰水 c. 乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800 g于锥形瓶中,加3mol/LH2SO4溶液15 mL将样品溶解完全后,加入指示剂,立即用0.1000 mol/L(NH4)2Ce(SO4)3标准液滴定至终点,用去标准液20.20 mL(反应为Ce4++Fe2+=Ce3++Fe3+)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20 mL。
回答下列问题:
(6)滴定时应选择
(7)甘氨酸亚铁晶体中Fe的质量分数为
(8)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有H2NCH2COO-和Fe2+;Fe2+的配位数为6,且存在五元螯合环;该配合物整体量中心对称,甘氨酸亚铁晶体的结构简式为
您最近半年使用:0次
解题方法
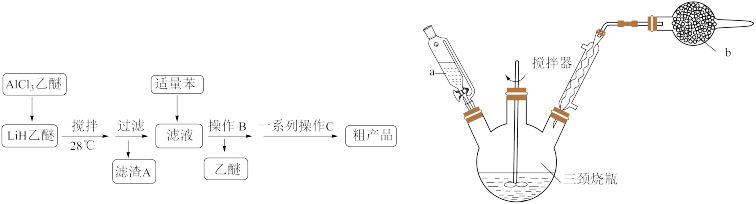
6 . 氢化铝锂( )以其优良的还原性广泛应用于医药、农药、香料、染料等行业,实验室按如图流程、装置开展制备实验(夹持、尾气处理装置已省略)。
)以其优良的还原性广泛应用于医药、农药、香料、染料等行业,实验室按如图流程、装置开展制备实验(夹持、尾气处理装置已省略)。
已知:① 难溶于烃,可溶于乙醚、四氢呋喃;
难溶于烃,可溶于乙醚、四氢呋喃;
②LiH、 在潮湿的空气中均会发生剧烈水解;
在潮湿的空气中均会发生剧烈水解;
③乙醚,沸点34.5℃,易燃,一般不与金属单质反应。请回答下列问题:
(1)仪器a的名称是___________ ;装置b的作用是___________ 。
(2)乙醚中的少量水分也会对 的制备产生严重的影响,以下试剂或操作可有效降低市售乙醚(含水体积分数为0.2%)含水量的是
的制备产生严重的影响,以下试剂或操作可有效降低市售乙醚(含水体积分数为0.2%)含水量的是___________ 。
a.钠 b.分液 c.五氧化二磷 d.通入乙烯
(3)下列说法正确的是___________
a. 能溶于乙醚,可能与
能溶于乙醚,可能与 可以形成二聚体有关
可以形成二聚体有关
b.滤渣A的主要成分是LiCl
c.为提高过滤出滤渣A的速度,可先加水让滤纸紧贴漏斗内壁
d.为提高合成 的速率,可将反应温度提高到50℃
的速率,可将反应温度提高到50℃
e.操作B可以在分液漏斗中进行
(4)该制备原理的不足之处是___________ 。
(5) (不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品
(不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品 ,记录量气管B起始体积读数
,记录量气管B起始体积读数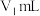 ,在分液漏斗中准确加入过量的四氢呋喃、水混合液15.0mL,打开旋塞至滴加完所有液体,立即关闭旋塞,调整量气管B,读数
,在分液漏斗中准确加入过量的四氢呋喃、水混合液15.0mL,打开旋塞至滴加完所有液体,立即关闭旋塞,调整量气管B,读数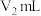 ,过量四氢呋喃的作用
,过量四氢呋喃的作用___________ ; 的质量分数为
的质量分数为___________ (已知25℃时,气体摩尔体积为 ,列出计算式即可)。
,列出计算式即可)。
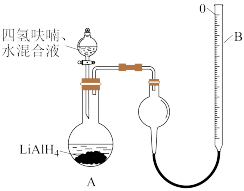
 )以其优良的还原性广泛应用于医药、农药、香料、染料等行业,实验室按如图流程、装置开展制备实验(夹持、尾气处理装置已省略)。
)以其优良的还原性广泛应用于医药、农药、香料、染料等行业,实验室按如图流程、装置开展制备实验(夹持、尾气处理装置已省略)。
已知:①
 难溶于烃,可溶于乙醚、四氢呋喃;
难溶于烃,可溶于乙醚、四氢呋喃;②LiH、
 在潮湿的空气中均会发生剧烈水解;
在潮湿的空气中均会发生剧烈水解;③乙醚,沸点34.5℃,易燃,一般不与金属单质反应。请回答下列问题:
(1)仪器a的名称是
(2)乙醚中的少量水分也会对
 的制备产生严重的影响,以下试剂或操作可有效降低市售乙醚(含水体积分数为0.2%)含水量的是
的制备产生严重的影响,以下试剂或操作可有效降低市售乙醚(含水体积分数为0.2%)含水量的是a.钠 b.分液 c.五氧化二磷 d.通入乙烯
(3)下列说法正确的是
a.
 能溶于乙醚,可能与
能溶于乙醚,可能与 可以形成二聚体有关
可以形成二聚体有关b.滤渣A的主要成分是LiCl
c.为提高过滤出滤渣A的速度,可先加水让滤纸紧贴漏斗内壁
d.为提高合成
 的速率,可将反应温度提高到50℃
的速率,可将反应温度提高到50℃e.操作B可以在分液漏斗中进行
(4)该制备原理的不足之处是
(5)
 (不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品
(不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品 ,记录量气管B起始体积读数
,记录量气管B起始体积读数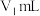 ,在分液漏斗中准确加入过量的四氢呋喃、水混合液15.0mL,打开旋塞至滴加完所有液体,立即关闭旋塞,调整量气管B,读数
,在分液漏斗中准确加入过量的四氢呋喃、水混合液15.0mL,打开旋塞至滴加完所有液体,立即关闭旋塞,调整量气管B,读数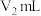 ,过量四氢呋喃的作用
,过量四氢呋喃的作用 的质量分数为
的质量分数为 ,列出计算式即可)。
,列出计算式即可)。
您最近半年使用:0次
2023-04-14更新
|
906次组卷
|
3卷引用:辽宁省沈阳市2023届高三下学期二模考试化学试题
名校
7 . 三氯化六氨合钴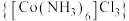 是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生
是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生 、
、 .某实验小组利用下列方法制备
.某实验小组利用下列方法制备 并测定其组成.
并测定其组成.
I.制备晶体:
向锥形瓶中加入适量研细的 、
、 和蒸馏水.加热溶解后加入活性炭催化剂.冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀.抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤.在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥.
和蒸馏水.加热溶解后加入活性炭催化剂.冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀.抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤.在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥.
Ⅱ.测定晶体组成:
(ⅰ)氨含量的测定(装置如图所示):
称取 样品于锥形瓶中,加水溶解.在另一锥形瓶中加入
样品于锥形瓶中,加水溶解.在另一锥形瓶中加入 标准HCl溶液并置于冰水浴中.从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右.然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中.取出锥形瓶,加入指示剂,用
标准HCl溶液并置于冰水浴中.从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右.然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中.取出锥形瓶,加入指示剂,用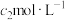 NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液
NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液 .
.

(ⅱ)钴含量的测定:
将上述左侧锥形瓶内样品残渣转移到碘量瓶中,冷却后加入足量KI溶液,立即盖上瓶塞并充分振荡后,加入浓盐酸,在暗处放置15min(还原产物为 )。然后加入蒸馏水和淀粉溶液,用
)。然后加入蒸馏水和淀粉溶液,用 标准溶液滴定至终点,记录消耗
标准溶液滴定至终点,记录消耗 标准溶液的体积(已知:
标准溶液的体积(已知: )。
)。
回答下列问题:
(1)制备实验中,生成 的化学方程式为
的化学方程式为______ 。
(2)“水浴加热至60℃”的原因为______ ;“洗涤”时适宜选择的洗涤剂为______ 。
(3)由氨含量的测定实验,可得样品中氨的质量分数为______ (用含 、
、 、
、 、
、 、m的代数式表示);若省略“纯水冲洗导管内外”,会使测定结果
、m的代数式表示);若省略“纯水冲洗导管内外”,会使测定结果______ (填“偏高”、“偏低”或“无影响”)。
(4)钴含量的测定实验中,含钴粒子发生反应的离子方程式为______ ;滴定终点时溶液颜色的变化为______ 。
(5)小组成员查阅资料得知,若不加活性炭催化剂,制备产物主要是 。现有10mL浓度为
。现有10mL浓度为 的
的 或
或 溶液,请设计实验区分:
溶液,请设计实验区分:______ 。
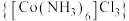 是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生
是一种橙黄色晶体,可溶于水和稀酸溶液、不溶于乙醇,与热的强碱溶液反应产生 、
、 .某实验小组利用下列方法制备
.某实验小组利用下列方法制备 并测定其组成.
并测定其组成.I.制备晶体:
向锥形瓶中加入适量研细的
 、
、 和蒸馏水.加热溶解后加入活性炭催化剂.冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀.抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤.在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥.
和蒸馏水.加热溶解后加入活性炭催化剂.冷却,加入浓氨水,继续冷却至10℃以下,缓慢加入双氧水,水浴加热至60℃左右并恒温20min,然后用冰水冷却,生成产品沉淀.抽滤,将沉淀溶解于50mL沸热的稀盐酸中,趁热过滤.在滤液中缓慢加入浓盐酸,立即有大量橙黄色晶体析出,冷却、过滤、洗涤、干燥.Ⅱ.测定晶体组成:
(ⅰ)氨含量的测定(装置如图所示):
称取
 样品于锥形瓶中,加水溶解.在另一锥形瓶中加入
样品于锥形瓶中,加水溶解.在另一锥形瓶中加入 标准HCl溶液并置于冰水浴中.从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右.然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中.取出锥形瓶,加入指示剂,用
标准HCl溶液并置于冰水浴中.从漏斗中加入足量20%的NaOH溶液,加热,保持微沸状态并持续1小时左右.然后取出插入标准HCl溶液中的导管,用纯水冲洗导管内外,洗涤液并入装有标准HCl溶液的锥形瓶中.取出锥形瓶,加入指示剂,用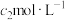 NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液
NaOH标准溶液滴定剩余的HCl,达到滴定终点时消耗NaOH标准溶液 .
.
(ⅱ)钴含量的测定:
将上述左侧锥形瓶内样品残渣转移到碘量瓶中,冷却后加入足量KI溶液,立即盖上瓶塞并充分振荡后,加入浓盐酸,在暗处放置15min(还原产物为
 )。然后加入蒸馏水和淀粉溶液,用
)。然后加入蒸馏水和淀粉溶液,用 标准溶液滴定至终点,记录消耗
标准溶液滴定至终点,记录消耗 标准溶液的体积(已知:
标准溶液的体积(已知: )。
)。回答下列问题:
(1)制备实验中,生成
 的化学方程式为
的化学方程式为(2)“水浴加热至60℃”的原因为
(3)由氨含量的测定实验,可得样品中氨的质量分数为
 、
、 、
、 、
、 、m的代数式表示);若省略“纯水冲洗导管内外”,会使测定结果
、m的代数式表示);若省略“纯水冲洗导管内外”,会使测定结果(4)钴含量的测定实验中,含钴粒子发生反应的离子方程式为
(5)小组成员查阅资料得知,若不加活性炭催化剂,制备产物主要是
 。现有10mL浓度为
。现有10mL浓度为 的
的 或
或 溶液,请设计实验区分:
溶液,请设计实验区分:
您最近半年使用:0次
8 . 钴及其化合物在工业生产中有着广阔的应用前景。已知: 不易被氧化,
不易被氧化, 具有强氧化性,
具有强氧化性, 具有较强还原性,
具有较强还原性, 性质稳定。
性质稳定。
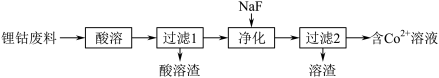
(1)从锂钴废料(主要成分为 )分离
)分离 。
。
① 的电子排布式为
的电子排布式为_______ 。
②“酸溶”时不选择浓 的理由是:
的理由是:_______ 。
③“净化”时,加 固体是将
固体是将 转化为沉淀,“净化”后溶液中
转化为沉淀,“净化”后溶液中 ,若“过滤1”后溶液中
,若“过滤1”后溶液中 浓度为1.0
浓度为1.0 ,则“净化”后
,则“净化”后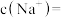
_______ 。[溶液体积变化忽略不计,不考虑其他离子影响。25℃时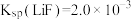 ]
]
(2)从由 制备
制备 。
。
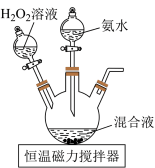
实验过程:称取研细的 10.0g和
10.0g和 50g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25
50g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 浓氨水,5
浓氨水,5 30%的
30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液,实验装置如图所示:
溶液,实验装置如图所示:
①由 制备
制备 溶液的离子方程式为
溶液的离子方程式为_______ 。
②分液漏斗中液体加入三颈烧瓶中的顺序为_______ 。
(3) 热分解制备
热分解制备 。
。
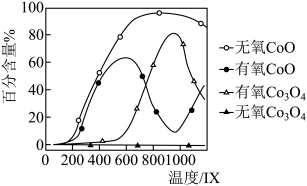
有氧和无氧环境下, 热解所得
热解所得 和
和 的百分含量与温度关系如图所示,请补充完整由
的百分含量与温度关系如图所示,请补充完整由 制备较纯净的
制备较纯净的 实验方案,取一定质量的
实验方案,取一定质量的 于热解装置中,
于热解装置中,_______ ,干燥。 (已知: 、
、 均难溶于水,
均难溶于水, 难溶于酸,
难溶于酸, 能溶于酸中,须使用的试剂有:1
能溶于酸中,须使用的试剂有:1
 ,蒸馏水,
,蒸馏水, 溶液)
溶液)
 不易被氧化,
不易被氧化, 具有强氧化性,
具有强氧化性, 具有较强还原性,
具有较强还原性, 性质稳定。
性质稳定。(1)从锂钴废料(主要成分为
 )分离
)分离 。
。
①
 的电子排布式为
的电子排布式为②“酸溶”时不选择浓
 的理由是:
的理由是:③“净化”时,加
 固体是将
固体是将 转化为沉淀,“净化”后溶液中
转化为沉淀,“净化”后溶液中 ,若“过滤1”后溶液中
,若“过滤1”后溶液中 浓度为1.0
浓度为1.0 ,则“净化”后
,则“净化”后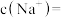
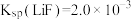 ]
](2)从由
 制备
制备 。
。实验过程:称取研细的
 10.0g和
10.0g和 50g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25
50g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中分别装有25 浓氨水,5
浓氨水,5 30%的
30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液,实验装置如图所示:
溶液,实验装置如图所示:
①由
 制备
制备 溶液的离子方程式为
溶液的离子方程式为②分液漏斗中液体加入三颈烧瓶中的顺序为
(3)
 热分解制备
热分解制备 。
。有氧和无氧环境下,
 热解所得
热解所得 和
和 的百分含量与温度关系如图所示,请补充完整由
的百分含量与温度关系如图所示,请补充完整由 制备较纯净的
制备较纯净的 实验方案,取一定质量的
实验方案,取一定质量的 于热解装置中,
于热解装置中, 、
、 均难溶于水,
均难溶于水, 难溶于酸,
难溶于酸, 能溶于酸中,须使用的试剂有:1
能溶于酸中,须使用的试剂有:1
 ,蒸馏水,
,蒸馏水, 溶液)
溶液)
您最近半年使用:0次
2023-09-02更新
|
209次组卷
|
3卷引用:江苏省镇江市丹阳市2023-2024学年高三上学期开学考试化学试题
9 .  (三氯化六氨合钴)是合成其他含钴配合物的理要原料,实验空中可由金属钴及其他原料制备
(三氯化六氨合钴)是合成其他含钴配合物的理要原料,实验空中可由金属钴及其他原料制备 。
。
已知:(1) 在
在 时恰好完全沉淀为
时恰好完全沉淀为 ;
;
(2)不同温度下 在水中的溶解度如图所示。
在水中的溶解度如图所示。
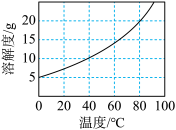
(一) 的制备
的制备
 易潮解,
易潮解,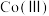 的氧化性强于
的氧化性强于 ,可用金属钴与氯气反应制备
,可用金属钴与氯气反应制备 。实验中利用如图装置(连接用橡胶管省略)进行制备。
。实验中利用如图装置(连接用橡胶管省略)进行制备。
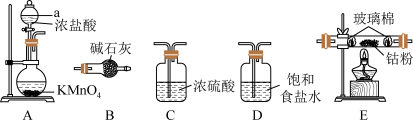
(1)用图中的装置组合制备 ,连接顺序为
,连接顺序为_______ 。装置B的作用是_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(二) 的制备
的制备
步骤如下:
I.在 锥形瓶内加入
锥形瓶内加入 研细的
研细的 ,
, 和
和 水,加热溶解后加入
水,加热溶解后加入 活性炭作催化剂。
活性炭作催化剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在 以下并缓慢加入
以下并缓慢加入 溶液。
溶液。
Ⅲ.在 下反应一段时间后,经过_______、_______、过滤、洗涤、干燥等操作,得到
下反应一段时间后,经过_______、_______、过滤、洗涤、干燥等操作,得到 晶体。
晶体。
(3)在加入浓氨水前,需在步骤I中加入 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因_______ 。
(4)步骤Ⅱ中在加入 浴液时,控制温度在
浴液时,控制温度在 以下并缓慢加入的目的是
以下并缓慢加入的目的是_______ 、_______ 。
(5)制备 的总反应的化学方程式为
的总反应的化学方程式为_______ 。
(6)步骤Ⅲ中的操作名称为_______ 、_______
 (三氯化六氨合钴)是合成其他含钴配合物的理要原料,实验空中可由金属钴及其他原料制备
(三氯化六氨合钴)是合成其他含钴配合物的理要原料,实验空中可由金属钴及其他原料制备 。
。已知:(1)
 在
在 时恰好完全沉淀为
时恰好完全沉淀为 ;
;(2)不同温度下
 在水中的溶解度如图所示。
在水中的溶解度如图所示。
(一)
 的制备
的制备 易潮解,
易潮解,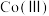 的氧化性强于
的氧化性强于 ,可用金属钴与氯气反应制备
,可用金属钴与氯气反应制备 。实验中利用如图装置(连接用橡胶管省略)进行制备。
。实验中利用如图装置(连接用橡胶管省略)进行制备。
(1)用图中的装置组合制备
 ,连接顺序为
,连接顺序为(2)装置A中发生反应的离子方程式为
(二)
 的制备
的制备步骤如下:
I.在
 锥形瓶内加入
锥形瓶内加入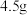 研细的
研细的 ,
, 和
和 水,加热溶解后加入
水,加热溶解后加入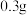 活性炭作催化剂。
活性炭作催化剂。Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在
 以下并缓慢加入
以下并缓慢加入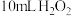 溶液。
溶液。Ⅲ.在
 下反应一段时间后,经过_______、_______、过滤、洗涤、干燥等操作,得到
下反应一段时间后,经过_______、_______、过滤、洗涤、干燥等操作,得到 晶体。
晶体。(3)在加入浓氨水前,需在步骤I中加入
 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因(4)步骤Ⅱ中在加入
 浴液时,控制温度在
浴液时,控制温度在 以下并缓慢加入的目的是
以下并缓慢加入的目的是(5)制备
 的总反应的化学方程式为
的总反应的化学方程式为(6)步骤Ⅲ中的操作名称为
您最近半年使用:0次
10 . 水合肼(N2H4•H2O)可用作抗氧化剂等,工业上常用尿素[CO(NH2)2]、NaOH、NaClO溶液反应制备水合肼。某兴趣小组在实验室用如下方法制备水合肼:将NaClO与NaOH的混合溶液滴入尿素水溶液中,在一定温度下加热,装置如图1所示(夹持及控温装置已略),充分反应后,仪器A中的溶液经蒸馏获得水合肼粗品,剩余溶液再进一步处理还可获得副产品NaCl和Na2CO3•10H2O。

已知:N2H4•H2O的沸点为118℃,具有强还原性。
回答下列问题:
(1)实验室常用Cl2和NaOH溶液制备NaClO溶液,通常用如图2装置制备Cl2时反应的化学方程式为_______ 。仪器A的名称是_______ ,仪器A中反应的离子方程式是_______ 。
(2)冷懝管的作用是_______ 。若滴加NaClO与NaOH的混合溶液的速度较快,水合肼的产率会下降,原因是_______ 。
(3)N2H4和NH3一样也能形成配位化合物,1mol配合物[P1(NH3)2(N2H4)2]Cl2中配位键的数目为_______ (NA表示阿伏加德罗常数的值)。
(4)水合肼是二元弱酸,在溶液中可发生类似NH3•H2O的电离。写出水合肼和HCl控物质的量之比为1:1反应的离子方程式_______ 。
(5)实验室可用碘测定水合肼的浓度,称取5.0g水合肼样品,加入适量水、稀硫酸、碳酸氢钠,配成500mL溶液,从中取出10.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,用0.200mol•L-1I2标准溶液进行滴定,滴定终点的现象是_______ 。测得消耗I2标准溶液的体积为17.50mL,则样品中水合肼(N2H4•H2O)的质量分数为_______ (保留3位有效数字,已知:N2H4•H2O+2I2+H2SO4+6NaHCO3=N2↑+4NaI+6CO2↑+Na2SO4+7H2O)。

已知:N2H4•H2O的沸点为118℃,具有强还原性。
回答下列问题:
(1)实验室常用Cl2和NaOH溶液制备NaClO溶液,通常用如图2装置制备Cl2时反应的化学方程式为
(2)冷懝管的作用是
(3)N2H4和NH3一样也能形成配位化合物,1mol配合物[P1(NH3)2(N2H4)2]Cl2中配位键的数目为
(4)水合肼是二元弱酸,在溶液中可发生类似NH3•H2O的电离。写出水合肼和HCl控物质的量之比为1:1反应的离子方程式
(5)实验室可用碘测定水合肼的浓度,称取5.0g水合肼样品,加入适量水、稀硫酸、碳酸氢钠,配成500mL溶液,从中取出10.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,用0.200mol•L-1I2标准溶液进行滴定,滴定终点的现象是
您最近半年使用:0次



