解题方法
1 . 含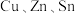 及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)写出基态 电子排布式
电子排布式___________ 。 与C均为第四主族元素,基态
与C均为第四主族元素,基态 原子的价电子中,两种自旋状态的电子数之比为
原子的价电子中,两种自旋状态的电子数之比为___________ 。
(2) 的空间结构名称为
的空间结构名称为___________ , 中心原子杂化方式为
中心原子杂化方式为___________ 。非金属性氧大于硫,能证明此关系成立的一种事实为___________ 。
(3) 的配位体是
的配位体是___________ , 形成配合物后
形成配合物后 键角会
键角会___________ (填“变大”、“变小”或“不变”),原因是成键电子对之间的排斥力___________ 孤电子对与成键电子对的排斥力(填“>”、“<”或“=”)。
(4)如图是硫的四种含氧酸根的结构:
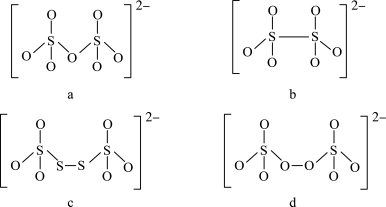
根据组成和结构推断,能在酸性溶液中将 转化为
转化为 的是
的是___________ (填序号),写出其离子反应方程式___________ 。
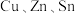 及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:(1)写出基态
 电子排布式
电子排布式 与C均为第四主族元素,基态
与C均为第四主族元素,基态 原子的价电子中,两种自旋状态的电子数之比为
原子的价电子中,两种自旋状态的电子数之比为(2)
 的空间结构名称为
的空间结构名称为 中心原子杂化方式为
中心原子杂化方式为(3)
 的配位体是
的配位体是 形成配合物后
形成配合物后 键角会
键角会(4)如图是硫的四种含氧酸根的结构:

根据组成和结构推断,能在酸性溶液中将
 转化为
转化为 的是
的是
您最近一年使用:0次
名校
解题方法
2 . 某小组进行如下“简单配合物的形成”的实验活动。
实验用品:试管、胶头滴管: 、
、 、
、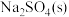 、
、 、蒸馏水、乙醇;
、蒸馏水、乙醇; 的
的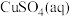 、
、 氨水。
氨水。
按要求回答下列问题。
(1)分别取下表中粉末少量于点滴板各孔穴中,加入足量蒸馏水溶解,对比观察现象,填写表中空白:
(2)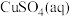 与氨水反应的实验
与氨水反应的实验
①向盛有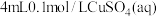 的试管中滴入几滴
的试管中滴入几滴 氨水实验现象为
氨水实验现象为_________ ;写出该反应的离子方程式:________________ 。
②继续加入氨水,得到深蓝色透明溶液。写出该反应的离子方程式:__________________ 。
③再加入乙醇,观察到析出深蓝色晶体。写出该晶体的化学式:__________________ 。
④经结构测定实验证明,步骤②中的深蓝色的配离子中:中心离子为_________ ,配位数为_________ ,配体为_________ 。
实验用品:试管、胶头滴管:
 、
、 、
、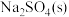 、
、 、蒸馏水、乙醇;
、蒸馏水、乙醇; 的
的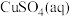 、
、 氨水。
氨水。按要求回答下列问题。
(1)分别取下表中粉末少量于点滴板各孔穴中,加入足量蒸馏水溶解,对比观察现象,填写表中空白:
固体物质 |  |  | 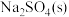 |  |
粉末颜色 | 白色 | 深褐色 | 白色 | 白色 |
溶液颜色 | 天蓝色 | 无色 | ||
实验结论 | ①溶液中呈无色的主要离子有 | |||
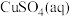 与氨水反应的实验
与氨水反应的实验①向盛有
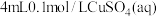 的试管中滴入几滴
的试管中滴入几滴 氨水实验现象为
氨水实验现象为②继续加入氨水,得到深蓝色透明溶液。写出该反应的离子方程式:
③再加入乙醇,观察到析出深蓝色晶体。写出该晶体的化学式:
④经结构测定实验证明,步骤②中的深蓝色的配离子中:中心离子为
您最近一年使用:0次
2023-05-02更新
|
247次组卷
|
2卷引用:天津市河西区2022-2023学年高二下学期4月期中考试化学试题
名校
3 . 下列说法不正确的是
| A.等离子体具有良好的导电性,冠醚能识别碱金属离子 |
| B.杂化轨道只能用来形成σ键或容纳未成键的孤电子对 |
| C.某元素气态基态原子的逐级电离能(kJ•mol﹣1)分别为 738、1451、7733、10540、13630、17995、21703, 当它与氯气反应时可能生成的阳离子是 X3+ |
| D.金属具有良好导电性,是因为金属晶体中“电子气”在电场作用下作定向移动 |
您最近一年使用:0次
名校
解题方法
4 .  是宇宙中最丰富的元素,
是宇宙中最丰富的元素, 位于第四周期且基态原子中有5个未成对电子,基态
位于第四周期且基态原子中有5个未成对电子,基态 原子的
原子的 能级与
能级与 能级的电子数相等,
能级的电子数相等,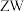 是
是 的等电子体,四种元素形成的配合物
的等电子体,四种元素形成的配合物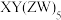 结构如下图所示,下列说法错误的是
结构如下图所示,下列说法错误的是
 是宇宙中最丰富的元素,
是宇宙中最丰富的元素, 位于第四周期且基态原子中有5个未成对电子,基态
位于第四周期且基态原子中有5个未成对电子,基态 原子的
原子的 能级与
能级与 能级的电子数相等,
能级的电子数相等,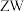 是
是 的等电子体,四种元素形成的配合物
的等电子体,四种元素形成的配合物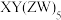 结构如下图所示,下列说法错误的是
结构如下图所示,下列说法错误的是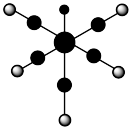
A.第一电离能: | B.电负性: |
| C.配体ZW中配位原子为Z | D.Y的最高价氧化物为碱性氧化物 |
您最近一年使用:0次
2024-03-29更新
|
591次组卷
|
4卷引用:化学(天津卷01)-2024年高考押题预测卷
(已下线)化学(天津卷01)-2024年高考押题预测卷湖北省圆创联盟2024届高三三月联合测评(一模)化学试卷湖北省高中名校联盟2023-2024学年高三下学期3月月考化学试题(已下线)山东省名校联盟2024届高三下学期5月模拟考试化学试题
5 . 化合物NaBH4和NaH与水的反应分别为①NaBH4+4H2O=Na[B(OH)4]+4H2↑;②NaH+H2O=NaOH+H2↑,下列说法错误的是
| A.电负性:H>B |
| B.①②中水均发生还原反应 |
| C.NaBH4和Na[B(OH)4]中提供孤电子对的均是氢原子 |
| D.当反应①、②转移的电子数相同时,产生H2的物质的量相等 |
您最近一年使用:0次
2024-03-22更新
|
336次组卷
|
2卷引用:天津市第一中学2023-2024学年高三下学期5月月考化学试卷
名校
解题方法
6 . 金属材料对于促进生产发展、改善人类生活发挥了巨大作用。
I.钢是人类使用最早的金属之一,至今仍被广泛应用于电气、电子等领域。
(1)写出基态Cu原子的核外电子排布式___________ 。涩法冶炼是以赤铜矿( )精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
)精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
(2)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为___ 。
(3)已知: 晶胞为立方体形,边长为
晶胞为立方体形,边长为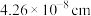 。根据图示,每个
。根据图示,每个 晶胞中含O原子的数目为
晶胞中含O原子的数目为___________ 个。计算 晶体的密度
晶体的密度
___________  (结果保留两位小数)。
(结果保留两位小数)。
(4)基态Na原子的价层电子轨道表示式为___________ 。
(5)NaCl熔点为:800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为:
 ,加入
,加入 的目的是
的目的是___________ 。
(6)除去 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是___________ 。
Ⅲ.钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(7) 原子的价电子排布式为
原子的价电子排布式为 ,它在元素周期表中的位置是
,它在元素周期表中的位置是___________ 。
(8) 易与
易与 形成
形成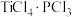 。下列关于
。下列关于 分子说法错误的是___________。
分子说法错误的是___________。
(9)钛溶于盐酸制得的三氯化钛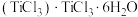 晶体有两种异构体:
晶体有两种异构体: (绿色)、
(绿色)、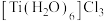 (紫色),两者配位数
(紫色),两者配位数___________ (选填“相同”或“不同”),绿色晶体中配体是___________ 。
I.钢是人类使用最早的金属之一,至今仍被广泛应用于电气、电子等领域。
(1)写出基态Cu原子的核外电子排布式
 )精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
)精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。(2)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为
(3)已知:
 晶胞为立方体形,边长为
晶胞为立方体形,边长为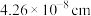 。根据图示,每个
。根据图示,每个 晶胞中含O原子的数目为
晶胞中含O原子的数目为 晶体的密度
晶体的密度
 (结果保留两位小数)。
(结果保留两位小数)。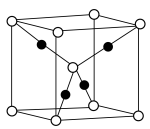
(4)基态Na原子的价层电子轨道表示式为
(5)NaCl熔点为:800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为:

 ,加入
,加入 的目的是
的目的是(6)除去
 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是Ⅲ.钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(7)
 原子的价电子排布式为
原子的价电子排布式为 ,它在元素周期表中的位置是
,它在元素周期表中的位置是(8)
 易与
易与 形成
形成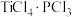 。下列关于
。下列关于 分子说法错误的是___________。
分子说法错误的是___________。| A.键角为120° | B.是极性分子 |
C.含有 键 键 | D.中心原子采取 杂化 杂化 |
(9)钛溶于盐酸制得的三氯化钛
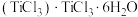 晶体有两种异构体:
晶体有两种异构体: (绿色)、
(绿色)、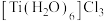 (紫色),两者配位数
(紫色),两者配位数
您最近一年使用:0次
2024-04-07更新
|
305次组卷
|
3卷引用:天津市红桥区2024届高三一模化学试题
名校
解题方法
7 . 实验测得Al与氯元素形成化合物的实际组成为 ,其球棍模型如图所示。已知
,其球棍模型如图所示。已知 在加热时易升华,与过量的NaOH溶液反应可生成
在加热时易升华,与过量的NaOH溶液反应可生成 -。下列说法不正确的是
-。下列说法不正确的是
 ,其球棍模型如图所示。已知
,其球棍模型如图所示。已知 在加热时易升华,与过量的NaOH溶液反应可生成
在加热时易升华,与过量的NaOH溶液反应可生成 -。下列说法不正确的是
-。下列说法不正确的是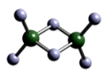
A. 属于分子晶体 属于分子晶体 |
B. 中Al原子为 中Al原子为 杂化 杂化 |
C. 中存在的化学键有极性共价键、配位键 中存在的化学键有极性共价键、配位键 |
D. 属于配合物 属于配合物 |
您最近一年使用:0次
2023-05-23更新
|
90次组卷
|
2卷引用:天津市朱唐庄中学2023-2024学年高二下学期3月检测化学试卷
名校
解题方法
8 . 请回答下列问题:
(1)5G芯片主要材质是高纯硅。基态Si原子核外电子的运动状态有_________ 种。
(2)高纯硅制备过程中会有 、
、 等中间产物生成。
等中间产物生成。
沸点:
_________  (填“>”或“<”);
(填“>”或“<”);
已知电负性:H>Si, 充分水解会生成两种酸和一种气体,写出该反应的化学方程式为
充分水解会生成两种酸和一种气体,写出该反应的化学方程式为______ 。
(3)复兴号高铁车体材质用到Mn、Co等元素。Mn的一种配合物化学式为:[ ],下列说法错误的是
],下列说法错误的是_________ (填字母标号)。
A.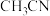 中σ键与π键数目之比为5:2
中σ键与π键数目之比为5:2
B.Mn原子的配位数为6
C.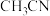 中C原子的杂化类型为
中C原子的杂化类型为 、
、
(4)FePO4是一种锂离子电池的正极材料,放电时生成LiFePO4。
①下列电子排布图表示的Li原子的状态中,能量最高的为_________ (填序号)。
a.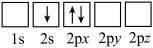 b.
b.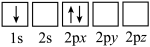
c.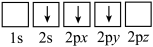
②锂离子电池充放电过程中,正极材料晶胞的组成变化如图所示。
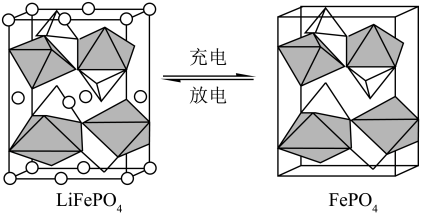
 的空间构型为
的空间构型为_________ 。正极材料在 和
和 之间转化时,每摩尔晶胞转移电子的物质的量为
之间转化时,每摩尔晶胞转移电子的物质的量为___________ mol。
(1)5G芯片主要材质是高纯硅。基态Si原子核外电子的运动状态有
(2)高纯硅制备过程中会有
 、
、 等中间产物生成。
等中间产物生成。沸点:

 (填“>”或“<”);
(填“>”或“<”);已知电负性:H>Si,
 充分水解会生成两种酸和一种气体,写出该反应的化学方程式为
充分水解会生成两种酸和一种气体,写出该反应的化学方程式为(3)复兴号高铁车体材质用到Mn、Co等元素。Mn的一种配合物化学式为:[
 ],下列说法错误的是
],下列说法错误的是A.
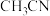 中σ键与π键数目之比为5:2
中σ键与π键数目之比为5:2B.Mn原子的配位数为6
C.
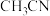 中C原子的杂化类型为
中C原子的杂化类型为 、
、
(4)FePO4是一种锂离子电池的正极材料,放电时生成LiFePO4。
①下列电子排布图表示的Li原子的状态中,能量最高的为
a.
 b.
b.
c.

②锂离子电池充放电过程中,正极材料晶胞的组成变化如图所示。

 的空间构型为
的空间构型为 和
和 之间转化时,每摩尔晶胞转移电子的物质的量为
之间转化时,每摩尔晶胞转移电子的物质的量为
您最近一年使用:0次
9 . 下列有关说法正确的是
A.Na2O和Na2O2固体中阳离子和阴离子个数比都是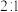 |
| B.CO2和SiO2的化学键类型和晶体类型相同 |
C. 和NH3都可以做为配合物的配体 和NH3都可以做为配合物的配体 |
| D.Al和N的原子轨道都有3个单电子 |
您最近一年使用:0次
10 . 关于 溶液,下列说法不正确的是
溶液,下列说法不正确的是
 溶液,下列说法不正确的是
溶液,下列说法不正确的是A. 中S原子的杂化方式为 中S原子的杂化方式为 |
B. 组成元素中电负性最大的是N元素 组成元素中电负性最大的是N元素 |
C. 所含有的化学键有离子键、极性共价键和配位键 所含有的化学键有离子键、极性共价键和配位键 |
D. 中,N原子是配位原子 中,N原子是配位原子 |
您最近一年使用:0次



