解题方法
1 . 下列说法不正确的是 ( )
| A.CS2中所有原子的最外层电子数均为8 |
| B.稳定性:HF>HCl>HBr>HI |
| C.已知NH5为离子化合物,则固体NH5中阴阳离子个数比为1:1 |
| D.由多种元素组成的多原子分子中,一定只存在极性键 |
您最近一年使用:0次
9-10高二·黑龙江·阶段练习
名校
解题方法
2 . 关于CS2,SO2,NH3三种物质的说法中正确的是( )
| A.CS2在水中的溶解度很小,是由于其属于极性分子 |
| B.SO2和NH3均易溶于水,原因之一是它们都是极性分子 |
| C.CS2为非极性分子,所以在三种物质中熔、沸点最低 |
| D.NH3在水中溶解度很大只是由于NH3分子有极性 |
您最近一年使用:0次
2020-11-05更新
|
672次组卷
|
32卷引用:2009-2010学年黑龙江佳一中高二第三学段考试化学试卷(选修3)
(已下线)2009-2010学年黑龙江佳一中高二第三学段考试化学试卷(选修3)【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二下学期4月月考化学试题云南省巧家县四中2018-2019学年高二上学期12月份考试化学试题云南省新平县一中2018-2019学年高二上学期12月考试化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题宁夏银川市银川二中2019-2020学年高二上学期第一次月考化学试题广东省潮州湘桥区南春中学2021-2022学年高二下学期第一次月考化学试题广东省佛山市顺德区罗定邦中学2022-2023学年高二下学期3月第一次月考化学试题广东省茂名化州市第三中学2021-2022学年高二下学期3月月考化学试题2014-2015湖北省襄阳市襄州一中等四校高二下学期期中联考化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:2.3 第2课时(已下线)2018年11月30日 《每日一题》一轮复习-键的极性与分子的极性云南省玉溪市江川二中2018-2019学年高二下学期开学考试化学试题(已下线)2019年3月24日 《每日一题》选修3-每周一测(已下线)2019年6月12日 《每日一题》 选修3-物质类别、键的极性及分子的极性之间的关系云南省云龙县第二中学2019-2020学年高二上学期期末考试化学试题云南省河口县高级中学2019-2020学年高二上学期期末考试化学试题第2章 化学键与分子间作用力——B拓展区综合拓展(鲁科版选修3)山西省太原市阳曲县第一中学2019-2020学年高二5月复学检测化学试题安徽省亳州市涡阳县第九中学2019-2020学年高二下学期期末考试化学试题(已下线)第35讲 分子结构与性质-2021年高考化学一轮复习名师精讲练广西防城港市防城中学2019-2020学年高二下学期期中考试化学试题四川省阿坝州九寨沟2019-2020学年高二上学期期末考试化学试题(已下线)第16单元 物质的结构与性质(选考)(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 课时3 溶解性 手性(已下线)考向37 分子结构与性质-备战2022年高考化学一轮复习考点微专题陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题(已下线)考点47 分子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第41练 分子结构与物质的性质-2023年高考化学一轮复习小题多维练(全国通用)吉林省长春市综合实验中学2021-2022学年高二上学期期末考试化学试题 (已下线)考点42 分子结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)云南省大理州实验中学2021-2022学年高二下学期化学期中考试题
名校
解题方法
3 . 下列说法中正确的是
| A.气体单质中,一定有σ键,可能有π键 |
| B.PCl3分子是非极性分子 |
| C.氢键键长一般定义为H…B的长度,而不是A-H…B的长度 |
D. 的VSEPR模型与离子的空间立体构型一致 的VSEPR模型与离子的空间立体构型一致 |
您最近一年使用:0次
2020-10-29更新
|
153次组卷
|
4卷引用:黑龙江省实验中学2023-2024学年高二下学期4月考化学试题
黑龙江省实验中学2023-2024学年高二下学期4月考化学试题四川省内江市第六中学2020-2021学年高二上学期第一次月考化学试题四川省内江市威远中学2020-2021学年高二上学期期中考试化学试题(已下线)练习15分子的结构与物质的性质-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)
名校
解题方法
4 . 标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图所示。下列分析正确的是
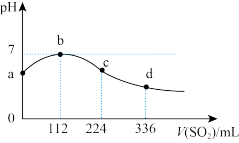

| A.a点对应溶液的导电性比d点强 |
| B.SO2是由极性键形成的非极性分子 |
| C.向d点的溶液中加入Ba(NO3)2溶液,产生BaSO4白色沉淀 |
| D.H2S饱和溶液的物质的量浓度为0.05 mol∙L-1 |
您最近一年使用:0次
名校
解题方法
5 . 配位化合物物广泛的应用于物质分离、定量测定.医药、催化等方面。利用氧化法可制备某些配位化合物。如2CoCl2+2NH4Cl+8NH3+H2O2=2[Co(NH3)5Cl]Cl2+2H2O
下列说法正确的是
下列说法正确的是
| A.该配位化合物的配位数为5 |
| B.提供孤电子对的成键原子是N和Cl |
| C.[Co(NH3)5Cl]2+中存在配位键、共价键和离子键 |
| D.氧化剂H2O2是非极性分子 |
您最近一年使用:0次
2020-08-22更新
|
957次组卷
|
10卷引用:黑龙江省佳木斯市三校联考2023-2024学年高三上学期第三次调研考试化学试题
黑龙江省佳木斯市三校联考2023-2024学年高三上学期第三次调研考试化学试题海南省儋州市第二中学2020-2021学年高二下学期3月月考化学试题山东省聊城市第三中学2021-2022学年高二下学期第一次质量检测化学试题湖南省邵东市第一中学2022-2023学年高二上学期第三次月考化学试题辽宁省葫芦岛市绥中县第一高级中学2022-2023学年高二下学期4月监测化学试题山东省菏泽市东明县第一中学2019-2020学年高二期末考试化学试题第四节 配合物与超分子(已下线)【知识图鉴】单元讲练测选择性必修2第三章01讲核心(已下线)第五章 物质结构与性质 元素周期律 必做实验提升(五) 简单配合物的形成与制备广东省顺德市(李兆基中学、郑裕彤中学、华侨中学)等2022-2023学年高二下学期4月期中考试化学试题
6 . 铍及其化合物的应用正日益被重视。
(1)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子的轨道表示式为__________ 。
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有______ (填字母)。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)氯化铍在气态时存在BeCl2分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。
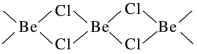
①a属于________ (填“极性”或“非极性”)分子。
②二聚分子(BeCl2)2中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为__________ (标出配位键)。
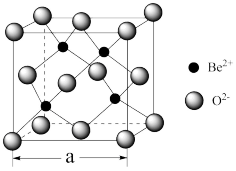
(4)BeO立方晶胞如下图所示,若BeO晶体的密度为d g·cm-3,则晶胞参数a=______ nm。
(1)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子的轨道表示式为
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)氯化铍在气态时存在BeCl2分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。

①a属于
②二聚分子(BeCl2)2中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为
(4)BeO立方晶胞如下图所示,若BeO晶体的密度为d g·cm-3,则晶胞参数a=

您最近一年使用:0次
2020-07-02更新
|
209次组卷
|
3卷引用:黑龙江省牡丹江市第二高级中学2022-2023学年高二下学期4月月考化学试题
名校
解题方法
7 . 下列说法正确的是( )
| A.第一电离能:Cl>S>P |
| B.共价键的极性:HF>HCl>HBr |
| C.在水中的溶解度:CH4>NH3 |
| D.酸性:HClO>HClO2>HClO3 |
您最近一年使用:0次
2020-05-20更新
|
37次组卷
|
2卷引用:黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高二下学期4月份月考化学试题
名校
8 . 下列说法中错误的是
A. 离子中心原子上的孤电子对数是1,立体构型为平面三角形 离子中心原子上的孤电子对数是1,立体构型为平面三角形 |
B.元素周期表第三周期主族元素中,简单离子半径最小的是 |
| C.金刚石转化为石墨为放热反应,说明相同条件下石墨比金刚石稳定 |
D. 、 、 都是非极性分子 都是非极性分子 |
您最近一年使用:0次
2020-05-18更新
|
324次组卷
|
4卷引用:黑龙江省哈尔滨市尚志中学2021-2022学年高二6月月考化学试题
解题方法
9 . 下列有关二氧化碳的描述正确的是( )
| A.含有非极性键 | B.是直线形分子 |
| C.属于极性分子 | D.结构式为C=O=O |
您最近一年使用:0次
2020-05-11更新
|
307次组卷
|
4卷引用:黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高二4月月考化学试题
11-12高三·山西太原·阶段练习
名校
解题方法
10 . 六氟化硫(SF6)分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是( )

| A.SF6各原子均达到最外层8电子稳定结构 |
| B.SF6易燃烧生成SO2 |
| C.SF6分子是含有极性键的非极性分子 |
| D.SF6是原子晶体 |
您最近一年使用:0次
2020-04-12更新
|
1176次组卷
|
17卷引用:黑龙江省鸡西实验中学2021-2022学年高二下学期第一次月考化学试题
黑龙江省鸡西实验中学2021-2022学年高二下学期第一次月考化学试题(已下线)2013届山西省太原五中高三8月月考化学试卷云南省昭通市彝良县第一中学2018-2019学年高二上学期12月考试化学试题福建省华安县第一中学2018-2019学年高二下学期第一次月考化学试题山东省聊城市东阿县第一中学2018-2019学年高二第二学期阶段性测试化学试题云南省永胜县第一中学2020-2021学年高二下学期6月份考试化学试题湖北省罗田县第一中学2021-2022学年高二下学期3月月考化学试题河北省秦皇岛市第一中学2022-2023学年高二上学期12月月考化学试题第3章 物质的聚集状态与物质性质 易错疑难集训(二)——A学习区 夯实基础(鲁科版选修3)(人教版2019)选择性必修2 第三章 晶体结构与性质 第二节 分子晶体与共价晶体 易错疑难集训(二)(已下线)第三单元 物质的聚集状态性质与物质性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)福建省龙岩市长汀县三级达标校2020-2021学年高二下学期期中考试化学试题北京师范大学第二附属中学2021-2022学年高二下学期期中考试化学试题(已下线)2022年湖北省高考真题变式题11-15选择性必修第二册 期末学业水平检测云南省玉溪师范学院附属中学2022-2023学年高二下学期期末考试化学试题北京师范大学第二附属中学2023-2024学年高二下学期期中考试化学试题



