1 . 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸(CH3COOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是
| A.CH3CH2OH能与水互溶 |
| B.NaClO通过氧化灭活病毒 |
| C.过氧乙酸相对分子质量为76 |
| D.氯仿的化学名称是四氯化碳 |
您最近一年使用:0次
2020-07-08更新
|
19883次组卷
|
65卷引用:贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题
贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题贵州省遵义市务川县汇佳中学2020-2021学年高二下学期第三次月考化学试题2020年全国统一考试化学试题(新课标Ⅰ)甘肃省会宁县第四中学2019-2020学年高二下学期期末考试化学试题(已下线)专题12 有机化合物-2020年高考真题和模拟题化学分项汇编江苏省扬州市扬州中学2021届高三开学检测化学试题辽宁省大连市辽宁师范大学附属中学2019-2020学年高一下学期期末考试化学试题河南省三门峡市第一高级中学2021届高三8月开学考试化学试题(已下线)小题必刷18 氯及其化合物——2021年高考化学一轮复习小题必刷(通用版)山东省泰安市第一实验学校2021届高三10月月考化学试题上海市七宝中学2021届高三上学期期中考试化学试题(已下线)热点1 化学与STSE-2021年高考化学专练【热点·重点·难点】江西省南昌市新建区第二中学2019-2020学年高二下学期期终考试化学试题(已下线)热点1 化学与STSE-2021年高考化学【热点·重点·难点】专练(山东专用)黑龙江省哈尔滨市第三十二中学2021届高三上学期期末考试化学试题 人教版2019必修第二册 第七章 第三~四节综合拔高练(已下线)专题09 常见有机物及其应用——备战2021年高考化学纠错笔记(已下线)小题02 化学与社会生产生活环境(STSE)——备战2021年高考化学经典小题考前必刷(全国通用)上海市行知中学2021届高三下学期3月月考化学试题(已下线)【苏州新东方】2020年10月江苏省苏州市高新区第一中学高二化学独立作业新疆乌鲁木齐市第八中学2020-2021学年高一下学期第一阶段考试化学试题(已下线)押全国卷理综第7题 化学与社会生产生活-备战2021年高考化学临考题号押题(课标全国卷)吉林省长春外国语学校2020-2021学年高一下学期期中考试化学(理科)试题河南省安阳市洹北中学2020-2021学年高二下学期第一次月考化学试题(苏教版2019)必修第二册专题8 有机化合物的获得与应用 C 高考挑战区山西省太原市2020-2021学年高一下学期期末考试化学试题西藏自治区拉萨那曲第二高级中学2020-2021学年高二下学期期末考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题(已下线)课时01 化学与生产、生活和环境-2022年高考化学一轮复习小题多维练(全国通用)内蒙古集宁新世纪中学2020-2021学年高二下学期期末考试化学试题(已下线)考向11 氯及其化合物-备战2022年高考化学一轮复习考点微专题吉林省抚松县泉阳镇抚松县第六中学2021-2022学年高二上学期化学与生活知识竞赛化学试题吉林省吉林市第二中学2020-2021学年高二下学期期中考试化学试卷江苏省常州市武进区礼嘉中学2021-2022学年高二上学期第一阶段教学质量调研化学试卷题(已下线)专题讲座(七) STSE与 化学可持续发展(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向30 烃的含氧衍生物-备战2022年高考化学一轮复习考点微专题(已下线)专题01 化学与STSE—2022年高考化学二轮复习讲练测-练习陕西省渭滨中学2021-2022学年高一上学期期中考试化学试题2020年全国卷Ⅰ理综化学高考真题变式题云南省峨山彝族自治县第一中学2021-2022学年高二上学期12月月考化学试题吉林省长春市实验中学2021-2022学年高二下学期4月月考化学试题(已下线)押全国卷理综第7题 化学与社会生产生活及传统文化-备战2022年高考化学临考题号押题(课标全国卷)(已下线)回归教材重难点01 化学与STSE与传统文化-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)查补易混易错点01 物质的组成、性质、分类及化学用语-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题01STSE化学用语-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题01STSE化学用语-五年(2018~2022)高考真题汇编(全国卷)(已下线)第01练 化学与科技社会生产生活、传统文化-2022年【暑假分层作业】高二化学(2023届一轮复习通用)山东省菏泽市鄄城县第一中学2021-2022学年高二下学期第二次月考化学试题黑龙江省双鸭山市集贤县一中、四中等2021-2022学年高二下学期期末考试化学试题专题4 生活中常用的有机物——烃的含氧衍生物 第一~二单元综合拔高练青海省西宁市七校2021-2022年高二下学期期末联考化学试题广东省揭阳华侨高级中学2021-2022学年高三上学期第三次阶段考试化学试题四川省邻水实验学校2021-2022学年高二下学期第二次月考理综化学试题云南省富源县第一中学2021-2022学年高二下学期3月月考化学试题黑龙江省双鸭山市饶河县高级中学2021-2022学年高二下学期期中考试化学试题(已下线)专题01 物质的组成与分类 传统文化-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题19 有机选择题题型分析(已下线)题型47 新型消毒剂的制备及用途江苏省苏州市苏州高新区第一中学2022-2023学年高一下学期5月月考化学试题4.1.1醇的性质和应用 课中广东省肇庆市第一中学2020--2021学年高二下学期期中考试化学试题河南省南阳市第一中学校2022-2023学年高二下学期4月月考化学试题(已下线)实验05 探究氯气的性质-【同步实验课】2023-2024学年高一化学教材实验大盘点(人教版2019必修第一册)云南省开远市第一中学校2023-2024学年高二上学期10月月考化学试题宁夏石嘴山市平罗中学2023-2024学年高二上学期第三次月考化学试题
2 . 研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____________ 。元素Mn与O中,第一电离能较大的是_________ ,基态原子核外未成对电子数较多的是_________________ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________ 和__________ 。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________________ ,原因是______________________________ 。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________ 。
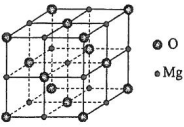
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________ nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________ nm。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为

您最近一年使用:0次
2017-08-08更新
|
8060次组卷
|
19卷引用:贵州省铜仁市思南中学2021届高三上学期第二次月考化学试题
贵州省铜仁市思南中学2021届高三上学期第二次月考化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅲ卷精编版)广东省广州市执信中学2018届高三上学期期中考试理综化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.17 物质结构与性质(已下线)【艺体生文化课百题突围系列-基础练测】专题2.17 物质结构与性质(选修)(已下线)《考前20天终极攻略》5月30日 物质结构与性质(已下线)解密21 物质的结构与性质(教师版)——备战2018年高考化学之高频考点解密步步为赢 高二化学暑假作业:作业十四 物质结构与性质(选修3)(已下线)2019年6月29日《每日一题》选修3—— 周末培优四川省南充市阆中中学2018-2019学年高二6月月考理科综合化学试题江西省临川一中2020届上学期第二次联合考试化学试题2020届湖南省湘潭市高三教学质量监测卷化学试题河北省衡水中学2020届高三下学期二月份网络教学质量监测理科综合化学试题宁夏海原县第一中学2019-2020学年高二下学期第一次月考化学试题陕西省榆林市绥德县绥德中学2020届高三第六次模拟考试化学试题河北省张家口市宣化区宣化第一中学2021届高三上学期10月月考化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练陕西省西安市高新第一中学2020届高三教学质量监测理综化学试题云南省玉溪第三中学2021-2022学年高三下学期3月入学考试理综化学试题
3 . 翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一
(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为_______ 。
(2)NaAlSi2O6所含元素中,第一电离能最小的是_______ ,原因是_______
(3)配合物K[Cr(C2O4)2(H2O)]中的配体是_______ ,H2O的沸点比CO2的高了许多,主要原因是_______ 。
(4)已知某FeSO4·xH2O的结构如图所示。

粒子内部的键角SO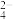
_______ H2O(填“>”“<”或“=”),从杂化类型及斥力大小角度说明判断的理由:_______ 。
(5)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式。
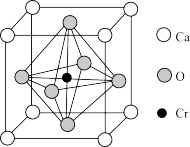
①该晶体的化学式为_______ 。
②已知钙离子、氧离子半径分别为100pm、140pm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为_______ pm。
(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为
(2)NaAlSi2O6所含元素中,第一电离能最小的是
(3)配合物K[Cr(C2O4)2(H2O)]中的配体是
(4)已知某FeSO4·xH2O的结构如图所示。

粒子内部的键角SO
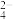
(5)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式。

①该晶体的化学式为
②已知钙离子、氧离子半径分别为100pm、140pm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
11-12高二下·云南玉溪·期末
4 . PH3是一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低。下列判断错误的是
| A.PH3分子呈三角锥形 |
| B.PH3分子是极性分子 |
| C.PH3沸点低于NH3沸点,因为P-H键键能低 |
| D.PH3分子稳定性低于NH3分子,因为N-H键键能高 |
您最近一年使用:0次
2021-04-21更新
|
2184次组卷
|
45卷引用:2015-2016学年贵州省思南中学高二下学期期末化学卷
2015-2016学年贵州省思南中学高二下学期期末化学卷贵州省织金县一中2018-2019学年高二上学期12月份考试化学试题(已下线)2011-2012学年云南省玉溪一中高二下学期期末考试化学试卷(已下线)2012-2013学年福建省师大附中高二下学期期末考试化学试卷(已下线)2014高考化学名师知识点精编 选修3物质结构与性质练习卷2014-2015黑龙江省哈尔滨六中高二上期末化学试卷2014-2015学年浙江省台州中学高二下第一次统练化学试卷2015-2016学年湖北沙市中学高二下第一次半月考化学试卷2015-2016学年山西省太原五中高二下3月周练化学试卷2015-2016学年山西大学附中高二5月模块诊断化学试卷河北省蠡县中学2016-2017学年高二6月月考化学试题河北省廊坊市第一中学2016-2017学年高二下学期6月月考化学试题福建省莆田第六中学2017-2018学年高二6月月考化学试题B【全国百强校】新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二下学期第一次调研化学试题【全国百强校】湖北省沙市中学2018-2019学年高二下学期期中考试化学试题新疆维吾尔自治区北京大学附属中学新疆分校2018-2019学年高二下学期期中考试化学试题西藏拉萨市八校2018-2019学年高二下学期期末联考化学试题河北省邢台市第二中学2018-2019学年高二下学期第四次月考化学试题上海市同济中学2016届高三上学期期中考试化学试题2020届高考化学二轮复习物质结构与性质专题练习云南省元阳县第三中学2019-2020学年高二上学期期末考试化学试题天津市静海区第一中学2020届高三3月统练化学试题2012年上海市高考化学试题上海市封浜高级中学2014-2015学年高三上学期期中考试化学试题山西省运城市永济涑北中学2019-2020学年高二下学期3月月考化学试题第2章 化学键与分子间作用力 易错疑难集训(三)——A学习区 夯实基础(鲁科版选修3)河北省新乐市第一中学2018--2019学年高二下学期第二次月考化学试题湖北省利川市第五中学2019年-2020学年高二下学期期末考试化学试题甘肃省兰州市第一中学2020-2021学年高二下学期4月月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高二4月月考化学试题湖北省十堰市2021届高三下学期4月调研考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期期中考试化学试题福建省连城一中2020-2021学年高二下学期第二次月考化学试题(已下线)第十二章能力提升检测卷(精练)-2022年一轮复习讲练测上海市上海中学2016—2017学年高一上学期期末考试化学试题2021年海南高考化学试题变式题1-10广东省江门市新会陈经纶中学2021-2022学年高二下学期期中考试化学试题上海市南洋模范中学2022届高三等级考模拟训练七化学试题新疆精河县高级中学2021-2022学年高二下学期期中考试化学试题河南省鄢陵县第一高级中学2021-2022学年高二下学期第三次考试化学试题(已下线)【知识图鉴】单元讲练测选择性必修2第二章02练基础山东省平邑县第一中学2022-2023学年高二下学期第一次月考化学试题广东省江门市开平市第二中学2021-2022学年高二下学期第7次段考化学试题广东省深圳市观澜中学2022-2023学年高二下学期月考(物质结构)化学试题天津市第九十五中学益中学校2023-2024学年高二下学期第一次月考化学试卷
名校
解题方法
5 . NH3与甲醛CH2O反应可以制备乌洛托品(六亚甲基四胺,分子结构为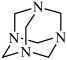 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
(1)基态氮原子的价电子轨道表达式为___________ ,第三电离能I3(C)___________ I3(N)(填“>”或“<)。
(2)NH3的空间构型为___________ ,CH2O中C采取的杂化类型为___________ 。CH2O中碳氢键与NH3中氮氢键相比,键长较长的是___________ 。
(3)乌洛托品为___________ (填“极性”或“非极性”)分子,分子中的所有N原子呈正四面体分布,所有C原子呈___________ 几何体分布,该分子可与H+形成配位键,电子对给予体为___________ 原子。
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为___________ 。乌洛托品比金刚烷(C10H16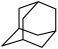 )水溶性更高,理由是
)水溶性更高,理由是___________ 。
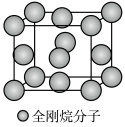
(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为___________ g/cm3。
 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:(1)基态氮原子的价电子轨道表达式为
(2)NH3的空间构型为
(3)乌洛托品为
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为
 )水溶性更高,理由是
)水溶性更高,理由是(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为

您最近一年使用:0次
2022-03-27更新
|
625次组卷
|
5卷引用:贵州省贵阳市五校2021-2022学年高三下学期联考理科综合化学试题(七)
贵州省贵阳市五校2021-2022学年高三下学期联考理科综合化学试题(七)四川省南充市2022届高三 适应性考试(二模)理综化学试题湖南省湘西自治州古丈县第一中学2021-2022学年高三下学期第二次模拟化学试题湖南省邵阳市第二中学2022-2023学年高三上学期第五次月考化学试题(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(结构与性质)
名校
6 . 下列几种氢键:① ;②
;② ;③
;③ ;④
;④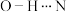 。氢键从强到弱的顺序排列正确的是
。氢键从强到弱的顺序排列正确的是
 ;②
;② ;③
;③ ;④
;④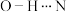 。氢键从强到弱的顺序排列正确的是
。氢键从强到弱的顺序排列正确的是| A.③>①>④>② | B.①>②>③>④ | C.③>②>①>④ | D.①>④>③>② |
您最近一年使用:0次
2021-02-19更新
|
1364次组卷
|
21卷引用:贵州省道真县民族中学2020届高三上学期开学考试理综化学试题
贵州省道真县民族中学2020届高三上学期开学考试理综化学试题2014-2015学年陕西省宝鸡中学高二下学期期末化学试卷A2015-2016学年内蒙古赤峰二中高二下4月月考化学试卷2015-2016学年辽宁省五校协作体高二下学期期中考试化学试卷(已下线)同步君 选修3 第二章 第三节 范德华力和氢键及其对物质性质的影响高中化学人教版 选修三 第2章 分子结构与性质 范德华力及其对物质性质的影响人教版2017-2018学年高二化学选修三同步训练:第二章 分子结构与性质(已下线)2018年12月1日 《每日一题》 一轮复习-周末培优(已下线)2019年3月20日 《每日一题》选修3-氢键的理解第4节 分子间作用力与物质性质——A学习区 夯实基础(鲁科版选修3)(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 课时2 分子间的作用力(已下线)模块同步卷07 第二章综合检测-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)2.4 分子间作用力-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2) (已下线)2.3 分子的结构与物质的性质(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)新疆昌吉教育共同体2020-2021学年高二下学期期末质量检测化学试题四川省遂宁市第二中学校2021-2022学年高二上学期期中考试化学试题云南省马关县第一中学2021-2022学年高二下学期2月份考试化学试题河南省新乡市河南师范大学附属中学2021-2022学年高二下学期3月月考化学试题(已下线)专题14 分子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)第三节 分子结构与物质的性质 第2课时 分子间作用力 分子的手性河北省唐山市迁西县职教中心2021-2022学年高二(普职融通二部)下学期4月月考化学试题
名校
解题方法
7 . 下列化学用语表示正确的是
A. 和 和 之间最强烈的氢键作用: 之间最强烈的氢键作用: |
B.硅的基态原子轨道表示式: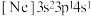 |
C. 中 中 的化合价: 的化合价: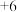 价 价 |
D. 的电子式: 的电子式: |
您最近一年使用:0次
名校
8 . 饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的离子方程式为
,反应的离子方程式为 。设
。设 为阿伏加德罗常数的值,下列说法
为阿伏加德罗常数的值,下列说法错误 的是
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的离子方程式为
,反应的离子方程式为 。设
。设 为阿伏加德罗常数的值,下列说法
为阿伏加德罗常数的值,下列说法A.消耗 ,反应转移的电子数为 ,反应转移的电子数为 |
B.消耗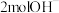 时,溶液中增加的 时,溶液中增加的 数目为 数目为 |
C.标准状况下,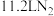 中含 中含 键数目为 键数目为 |
D. 液态水中含有的氢键数目少于 液态水中含有的氢键数目少于 |
您最近一年使用:0次
2024-04-08更新
|
312次组卷
|
3卷引用:贵州省贵阳市第六中学2024届高三下学期一模考试化学试题
11-12高二下·河北邢台·阶段练习
名校
解题方法
9 . 氨气溶于水中,大部分 与
与 以氢键结合形成
以氢键结合形成 。根据氨水的性质可推知
。根据氨水的性质可推知 的结构式为
的结构式为
 与
与 以氢键结合形成
以氢键结合形成 。根据氨水的性质可推知
。根据氨水的性质可推知 的结构式为
的结构式为A.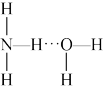 | B.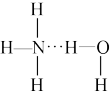 | C.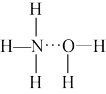 | D.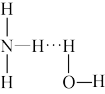 |
您最近一年使用:0次
2022-08-22更新
|
624次组卷
|
36卷引用:2015-2016学年贵州省思南中学高二下期中化学试卷
2015-2016学年贵州省思南中学高二下期中化学试卷(已下线)2011-2012学年河北省邢台一中高二下学期第四次月考化学试卷(已下线)2012-2013学年湖北省荆州市监利县柘木中学高二下第二次月考化学卷(已下线)同步君 选修3 第二章 第三节 范德华力和氢键及其对物质性质的影响吉林省松原市扶余县第一中学2016-2017学年高二下学期期中考试化学试题内蒙古包头市第三十三中学2016-2017学年高二下学期期末考试化学试题高中化学人教版 选修三 第2章 分子结构与性质 范德华力及其对物质性质的影响山东师范大学附属中学2017-2018学年高二下学期期中考试(理)化学试题山东省师范大学附属中学2017-2018学年高二下学期第七次学分认定考试(期中)(理)化学试题宁夏银川市银川二中2019-2020学年高二上学期第一次月考化学试题(已下线)专题11.2 分子结构与性质(讲)-《2020年高考一轮复习讲练测》第4节 分子间作用力与物质性质——A学习区 夯实基础(鲁科版选修3)山东省泰安市肥城市泰西中学2019-2020学年高二下学期5月月考化学试题高一必修第一册(苏教2019)专题5 第二单元 微粒之间的相互作用力2(已下线)第36讲 分子结构与性质(精讲)-2021年高考化学一轮复习讲练测(人教版2019)选择性必修2 第二章 分子结构与性质 学思用(已下线)(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构 学思用(已下线)(人教版2019)选择性必修2 第二章 分子结构与性质 第一节 共价键 学思用(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 第2课时 分子间作用力与分子的手性鲁科版2019选择性必修2第2章 微粒间相互作用与物质性质 第4节 分子间作用力山东省新泰市第一中学2020-2021学年高二下学期第一次阶段性考试化学试题河南省开封市五县2020-2021学年高二下学期月考化学试题(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点34 分子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)5.2.2 共价键 分子间作用力-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)(已下线)第2.3.2讲 分子间作用力 分子的手性-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)专题3 微粒间作用力与物质性质 第四单元 分子间作用力分子晶体 第1课时范德华力 氢键第三节 分子结构与物质的性质 第2课时 分子间作用力 分子的手性(已下线)第30讲 分子结构与性质(练)-2023年高考化学一轮复习讲练测(新教材新高考)2023年广西高中学生竞赛(高一、高二同卷)化学试题2023年第37届中国化学奥林匹克广西预选赛化学试题3.4.1分子间作用力 课中(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)上海市洋泾中学2023-2024学年高三上学期9月月考化学试题
10 . 甲~丁均为短周期主族元素,在元素周期表中的相对位置如图所示,丁的最高价氧化物对应的水化物在同周期中酸性最强,下列说法正确的是
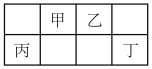

| A.原子半径:甲>乙>丙 | B.非金属性:丁>丙>乙 |
| C.丙与乙形成的化合物是分子晶体 | D.最简单氢化物的沸点:乙>甲>丁 |
您最近一年使用:0次
2022-12-22更新
|
707次组卷
|
4卷引用:选择题6-10



