1 . W、X、Y、Z、R为原子序数依次增大的短周期主族元素,五种元素组成的某化合物可用于治疗肝昏迷及其他精神疾病,该化合物的结构简式如图所示。下列说法正确的是
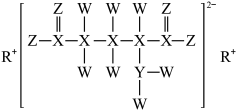
| A.简单氢化物的沸点:X>Y>Z |
| B.原子半径:R>X>Y>Z>W |
| C.R分别与Z和W形成的化合物中化学键类型完全相同 |
| D.X、Y、Z分别与W形成的化合物均是极性分子 |
您最近半年使用:0次
名校
2 . 下列对实验事实或物质用途的解释正确的是
| 实验事实或物质用途 | 解释 | |
| A | 用红热的铁针刺水晶柱表面凝固的石蜡,石蜡在不同方向熔化的快慢不同 | 水晶内部质点排列有序,导热性各向异性 |
| B | 工业上常用液氨作制冷剂 | 断裂NH3中H—N需要吸收能量 |
| C | 蔗糖易溶于水,难溶于四氯化碳 | 蔗糖和四氯化碳都是有机物,这违背了“相似相溶”规律 |
| D | 紫红色碘的四氯化碳溶液中,加入浓碘化钾水溶液,紫色变浅 | 碘在水中溶解性比碘在四氯化碳中溶解性好 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-22更新
|
113次组卷
|
2卷引用:陕西省汉中市多校联考2023-2024学年高二下学期期中考试化学试卷
解题方法
3 . 回答下列问题:
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气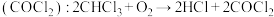 ,光气
,光气 分子的立体构型是
分子的立体构型是________ 形。
(2)某有机物的结构简式为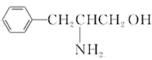 。该有机物分子是
。该有机物分子是____________ (填“极性”或“非极性”)分子,该有机物分子中采取 杂化的原子对应元素的电负性由大到小的顺序为
杂化的原子对应元素的电负性由大到小的顺序为____________ 。
(3)乙二胺 分子中氮原子杂化类型为
分子中氮原子杂化类型为_________________ 。
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸( )是一种弱酸,其分子结构可表示为
)是一种弱酸,其分子结构可表示为 ,肼
,肼 被亚硝酸氧化时便可得到氢叠氮酸
被亚硝酸氧化时便可得到氢叠氮酸 ,发生的反应为
,发生的反应为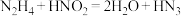 。
。 的酸性和醋酸相近,可微弱电离出
的酸性和醋酸相近,可微弱电离出 和
和 。
。
①叠氮酸根能与许多金属离子等形成配合物,如 ,根据价层电子对互斥理论判断
,根据价层电子对互斥理论判断 的空间构型为
的空间构型为________________ 。
②下列有关说法正确的是_____________ (填序号)。
A. 中含有5个
中含有5个 键
键
B. 中的三个氮原子均采用
中的三个氮原子均采用 杂化
杂化
C. 、
、 、
、 、
、 都是极性分子
都是极性分子
D.肼 的沸点高达
的沸点高达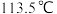 ,说明肼分子间可形成氢键
,说明肼分子间可形成氢键
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气
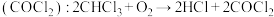 ,光气
,光气 分子的立体构型是
分子的立体构型是(2)某有机物的结构简式为
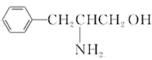 。该有机物分子是
。该有机物分子是 杂化的原子对应元素的电负性由大到小的顺序为
杂化的原子对应元素的电负性由大到小的顺序为(3)乙二胺
 分子中氮原子杂化类型为
分子中氮原子杂化类型为(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(
 )是一种弱酸,其分子结构可表示为
)是一种弱酸,其分子结构可表示为 ,肼
,肼 被亚硝酸氧化时便可得到氢叠氮酸
被亚硝酸氧化时便可得到氢叠氮酸 ,发生的反应为
,发生的反应为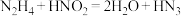 。
。 的酸性和醋酸相近,可微弱电离出
的酸性和醋酸相近,可微弱电离出 和
和 。
。①叠氮酸根能与许多金属离子等形成配合物,如
 ,根据价层电子对互斥理论判断
,根据价层电子对互斥理论判断 的空间构型为
的空间构型为②下列有关说法正确的是
A.
 中含有5个
中含有5个 键
键B.
 中的三个氮原子均采用
中的三个氮原子均采用 杂化
杂化C.
 、
、 、
、 、
、 都是极性分子
都是极性分子D.肼
 的沸点高达
的沸点高达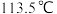 ,说明肼分子间可形成氢键
,说明肼分子间可形成氢键
您最近半年使用:0次
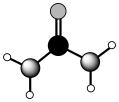
4 . 1828年,德国化学家弗里德里希 维勒首次使用无机物质氰酸铵与硫酸铵人工合成了尿素,揭开了人工合成有机物的序幕。尿素在农业生产中扮演者重要的角色,其结构如图所示。下列有关说法错误的是
维勒首次使用无机物质氰酸铵与硫酸铵人工合成了尿素,揭开了人工合成有机物的序幕。尿素在农业生产中扮演者重要的角色,其结构如图所示。下列有关说法错误的是
 维勒首次使用无机物质氰酸铵与硫酸铵人工合成了尿素,揭开了人工合成有机物的序幕。尿素在农业生产中扮演者重要的角色,其结构如图所示。下列有关说法错误的是
维勒首次使用无机物质氰酸铵与硫酸铵人工合成了尿素,揭开了人工合成有机物的序幕。尿素在农业生产中扮演者重要的角色,其结构如图所示。下列有关说法错误的是
A.结构中元素第一电离能由大到小: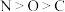 |
| B.分子中N原子与C原子的杂化不同 |
| C.该物质在水中溶解度较大 |
| D.基态碳原子核外有6种不同空间运动状态的电子 |
您最近半年使用:0次
解题方法
5 . 回答下列问题
(1)在 分子中,CO
分子中,CO 的价层电子对的空间构型为
的价层电子对的空间构型为___________ ,以极性键相结合,具有正四面体结构的分子是___________ ,以极性键相结合,具有三角锥形结构的分子是___________ ,以极性键相结合,具有V形结构的分子是___________ 。
(2)元素As与N同族。预测As的氢化物分子的空间结构为___________ ,其沸点比NH3的___________ (填“高”或“低”),其判断理由是___________ 。
(1)在
 分子中,CO
分子中,CO 的价层电子对的空间构型为
的价层电子对的空间构型为(2)元素As与N同族。预测As的氢化物分子的空间结构为
您最近半年使用:0次
解题方法
6 . 蛋白质分子结构的一部分如图所示,下列说法正确的是
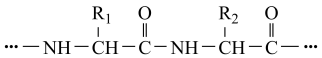
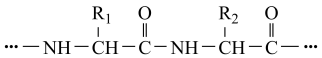
| A.沸点:NH3<H2O | B.中子数为8的碳原子: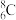 |
| C.核电荷数:C>N>O>H | D.基态原子的未成对电子数:O>C>N |
您最近半年使用:0次
7 . 如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:
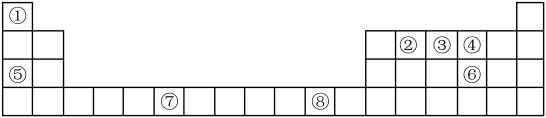
(1)⑧号元素在周期表中的位置是___________ ,其最高能层的电子占据的原子轨道电于云轮廓为___________ 形。
(2)④、⑤、⑥的简单离子的离子半径由小到大的顺序为___________ (用元素符号表示、下同)。
(3)元素①②③可形成原子个数比为1:1:1的共价化合物,分子中各原子最外层均达到8电子或2电子的稳定结构,试写出其电子式___________ ,该分子为___________ (填“极性分子”或“非极性分子”)。
(4)画出⑦的基态原子价层电子轨道表示式___________ 。
(5)④的简单氢化物比⑥的简单氢化物沸点更高,原因是___________ 。

(1)⑧号元素在周期表中的位置是
(2)④、⑤、⑥的简单离子的离子半径由小到大的顺序为
(3)元素①②③可形成原子个数比为1:1:1的共价化合物,分子中各原子最外层均达到8电子或2电子的稳定结构,试写出其电子式
(4)画出⑦的基态原子价层电子轨道表示式
(5)④的简单氢化物比⑥的简单氢化物沸点更高,原因是
您最近半年使用:0次
名校
解题方法
8 . 下列物质性质的变化规律与化学键无关的是
A. 、 、 、 、 、 、 的热稳定性依次减弱 的热稳定性依次减弱 |
B. 、 、 、 、 、 、 的熔点依次降低 的熔点依次降低 |
C. 易液化 易液化 |
D. 、 、 、 、 、 、 的熔点逐渐降低 的熔点逐渐降低 |
您最近半年使用:0次
名校
9 . “冰面为什么滑?”这与冰层表面的结构有关(如图)。下列说法错误的是


| A.第一层固态冰中,水分子间通过氢键形成空间网状结构,密度比液态水小 |
| B.第二层“准液体”水分子之间形成的氢键较第一层多 |
| C.当高于一定温度时,“准液体”中的水分子与下层冰连接的氢键断裂,产生“流动性水分子”,使冰面变滑 |
D.冰融化成水的过程, |
您最近半年使用:0次
名校
10 . 下列说法正确的是
| A.分子晶体中分子间作用力越大,该物质越稳定 |
| B.平面三角形分子一定是非极性分子 |
| C.24Mg32S晶体中电子总数与中子总数之比为1:1 |
| D.H2S和SiF4分子中各原子最外层都满足8电子结构 |
您最近半年使用:0次
2024-01-08更新
|
62次组卷
|
2卷引用:陕西省汉中市西乡县第一中学2023-2024学年高二下学期3月月考化学试题



