1 . (1)常温下,乙醇在___________ (填“环己烷或乙酸”)中溶解度更大,主要原因是___________ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___________ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
您最近一年使用:0次
解题方法
2 . 图中每条折线表示周期表ⅣA~ⅦA中的某一族元素简单氢化物的沸点变化,每个小黑点代表一种氢化物。下列说法正确的是


| A.d代表的是CH4 |
| B.沸点的高低顺序是HF>H2O>NH3 |
| C.NH3的沸点是第ⅤA元素形成的氢化物中沸点最高的 |
D.根据NH3·H2O NH NH +OH-,氨分子和水分子之间最主要存在的氢键形式O—H…N +OH-,氨分子和水分子之间最主要存在的氢键形式O—H…N |
您最近一年使用:0次
2021-05-13更新
|
483次组卷
|
4卷引用:考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)山东省泰安肥城市2020-2021学年高二下学期期中考试化学试题(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)第二章分子结构与性质(提升卷)
3 . (1)氢键是微粒间的一种常见作用力,如存在于醋酸分子间( )和硝酸分子内(
)和硝酸分子内( )等。已知邻氨基苯甲醛(
)等。已知邻氨基苯甲醛( )的熔点为39℃,对氨基苯甲醛(
)的熔点为39℃,对氨基苯甲醛( )的熔点为71℃,请说明对氨基苯甲醛的熔点比邻氨基苯甲醛高的原因
)的熔点为71℃,请说明对氨基苯甲醛的熔点比邻氨基苯甲醛高的原因___ 。
(2)请用一个化学方程式并结合适当的文字说明HClO、H2CO3和HCO 酸性的强弱
酸性的强弱___ 。
 )和硝酸分子内(
)和硝酸分子内( )等。已知邻氨基苯甲醛(
)等。已知邻氨基苯甲醛( )的熔点为39℃,对氨基苯甲醛(
)的熔点为39℃,对氨基苯甲醛( )的熔点为71℃,请说明对氨基苯甲醛的熔点比邻氨基苯甲醛高的原因
)的熔点为71℃,请说明对氨基苯甲醛的熔点比邻氨基苯甲醛高的原因(2)请用一个化学方程式并结合适当的文字说明HClO、H2CO3和HCO
 酸性的强弱
酸性的强弱
您最近一年使用:0次
名校
4 . 下列说法正确的是
| A.湿法炼铜可通过铁单质置换硫酸铜水溶液中的铜,湿法炼锌可通过电解硫酸锌溶液制备锌单质 |
| B.碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 |
| C.根据某元素氧化物对应的水化物酸性强弱判断非金属性强弱 |
| D.HF的热稳定性很好,主要是因为HF分子间存在氢键 |
您最近一年使用:0次
2021-05-12更新
|
372次组卷
|
5卷引用:浙江省五校2021届高三下学期5月联考化学试题
浙江省五校2021届高三下学期5月联考化学试题(已下线)【浙江新东方】【2021.5.19】【SX】【高三下】【高中化学】【SX00128】(已下线)单科化学-2021年秋季高三开学摸底考试卷02(课标全国专用)四川省成都高新实验中学2021-2022学年高三上学期入学考试化学试题湖南省耒阳市第一中学2022届高三下学期5月月考化学试题
解题方法
5 . (1)乙醇和二甲醚互为同分异构体,乙醇的沸点(78.5℃)远高于二甲醚的沸点(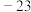 ℃),原因是
℃),原因是_______ 。
(2) 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式_______ 。
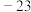 ℃),原因是
℃),原因是(2)
 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式
您最近一年使用:0次
6 . (1)对羟基苯甲酸( )的熔点(213~217°C)比邻羟基苯甲酸(
)的熔点(213~217°C)比邻羟基苯甲酸( )的熔点(135~136℃)高,原因是
)的熔点(135~136℃)高,原因是____ 。
(2)钠的金属性比镁强,从结构的角度说明理由_____ 。
 )的熔点(213~217°C)比邻羟基苯甲酸(
)的熔点(213~217°C)比邻羟基苯甲酸( )的熔点(135~136℃)高,原因是
)的熔点(135~136℃)高,原因是(2)钠的金属性比镁强,从结构的角度说明理由
您最近一年使用:0次
解题方法
7 . (1) N2H6Cl2属于离子化合物,且每个原子都满足稳定结构。N2H6Cl2的电子式为____ 。
(2)一定条件下,测定HF的相对分子质量时,实验数据明显大于理论值,原因是_____ 。
(2)一定条件下,测定HF的相对分子质量时,实验数据明显大于理论值,原因是
您最近一年使用:0次
名校
解题方法
8 . 某小组用温度传感器探究液态物质挥发过程中体系温度变化的大小和快慢。如图a连接装置,将滤纸固定于温度传感器测量端,并插入待测液中使滤纸吸附待测液,待温度示数稳定后,开始采集数据,约10s后取出温度传感器置于空气中放置,采集到的温度变化如图b、图c所示。下列说法不正确 的是:


| A.由图b,分子间作用力越弱,气化速率越快 |
| B.由图c,正丁醇气化温差小于乙醚,是因为正丁醇更稳定 |
| C.由图d,X的相对分子量可能小于Y |
| D.由图d,X、Y可以分别为正己烷、正戊烷 |
您最近一年使用:0次
2021-05-04更新
|
593次组卷
|
2卷引用:浙江省台州市2021届高三4月选考科目教学质量评估试题(二模)化学试题
2016高二·全国·课时练习
名校
解题方法
9 . 下列关于氢键的说法正确的是
A.由于氢键的作用,使NH3、H2O、HF的沸点反常,且沸点高低顺序为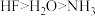 |
| B.氢键只能存在于分子间,不能存在于分子内 |
| C.生命体中许多大分子内存在氢键 |
| D.相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多 |
您最近一年使用:0次
2021-05-02更新
|
189次组卷
|
9卷引用:考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 易错疑难集训(三)(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)同步君 选修3 第二章 第三节 范德华力和氢键及其对物质性质的影响高中化学人教版 选修三 第2章 分子结构与性质 范德华力及其对物质性质的影响人教版2017-2018学年高二化学选修三同步训练:2.3 分子的性质(第2课时)山东省滨州市惠民县第二中学致远高中部2020-2021学年高二上学期期中考试化学试题广东省揭阳市普宁市华侨中学2021-2022学年高二下学期第一次月考化学试题(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)
2021·浙江·模拟预测
解题方法
10 . 请回答下列问题:
(1)NH3的沸点(-33.5℃)高于NF3的沸点(-129℃)的主要原因是_______ 。
(2)化学式为N2H4C,属离子化合物,各原子均具有稀有气体稳定结构。写出它的电子式_______ 。
(3) 常压下,SO3的沸点(44.8℃)比SO2的沸点(-10℃)高,其主要原因是_______ 。
(1)NH3的沸点(-33.5℃)高于NF3的沸点(-129℃)的主要原因是
(2)化学式为N2H4C,属离子化合物,各原子均具有稀有气体稳定结构。写出它的电子式
(3) 常压下,SO3的沸点(44.8℃)比SO2的沸点(-10℃)高,其主要原因是
您最近一年使用:0次



