1 . (1)已知乙醛的沸点为20.8℃,乙醇的沸点为78℃。乙醛沸点比乙醇沸点低的主要原因是______ 。
(2)有科学家在实验室条件下将干冰制成了原子晶体。则同是原子晶体的 和
和 硬度大小关系
硬度大小关系
______  (填“>”、“<”或“=”),从结构的角度说明理由
(填“>”、“<”或“=”),从结构的角度说明理由______ 。
(2)有科学家在实验室条件下将干冰制成了原子晶体。则同是原子晶体的
 和
和 硬度大小关系
硬度大小关系
 (填“>”、“<”或“=”),从结构的角度说明理由
(填“>”、“<”或“=”),从结构的角度说明理由
您最近一年使用:0次
20-21高一下·浙江绍兴·阶段练习
2 . ①绿矾化学式:_______ ;
②共价化合物COCl2电子式:_______ ;
③NH3与H2O的热稳定性由大到小顺序:_______
④HF与HCl的沸点由低到高顺序:_______
⑤硫酸氢钠溶液与亚硫酸氢钠溶液反应的离子方程式:_______ 。
②共价化合物COCl2电子式:
③NH3与H2O的热稳定性由大到小顺序:
④HF与HCl的沸点由低到高顺序:
⑤硫酸氢钠溶液与亚硫酸氢钠溶液反应的离子方程式:
您最近一年使用:0次
名校
3 . 下列“类比”合理的是
A.氯气能使湿润的pH试纸先变红后褪色, 也使湿润的pH试纸先变红后褪色 也使湿润的pH试纸先变红后褪色 |
B. 与盐酸反应生成 与盐酸反应生成 和 和 ,则 ,则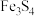 也可盐酸反应生成 也可盐酸反应生成 和 和 |
C. 是直线型分子,则 是直线型分子,则 也是直线型分子 也是直线型分子 |
D. 的沸点高于 的沸点高于 ,则 ,则 的沸点高于 的沸点高于 |
您最近一年使用:0次
2021-03-16更新
|
410次组卷
|
2卷引用:浙江省宁波“十校”2021届高三3月联考化学试题
2021高三·浙江·专题练习
解题方法
4 . 冰晶胞中水分子的空间排列方式与金刚石晶胞类似,如图:

下列有关冰晶胞说法正确的是

下列有关冰晶胞说法正确的是
| A.冰晶胞内水分子间以共价键结合 |
| B.每个冰晶胞平均含有4个水分子 |
| C.水分子间的氢键无方向性和饱和性 |
| D.实验测得冰中氢键的作用力为18.5kJ/mol,而冰的熔化热为5.0kJ/mol,这说明冰熔化成水,氢键部分被破坏。 |
您最近一年使用:0次
20-21高一·浙江·阶段练习
解题方法
5 . (1)在物质CO2、P2O5、CaO、SO2中,有一种物质在某些化学性质或分类上与其他几种物质不同,这种物质是__ 。
(2)气态氢化物热稳定性HF大于HCl的主要原因是__ 。
(3)常温下,一体积的水可以溶解700体积的氨气,原因是_ 。
(4)根据现有元素周期律推算,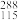 Mc位于元素周期表的第
Mc位于元素周期表的第__ 周期第__ 族。
(5)已知2K2S+K2SO3+3H2SO4=3K2SO4+3S↓+3H2O,若氧化产物比还原产物多8.0g,则转移电子的数目为__ 。
(6)以物质的类别为横坐标,化合价为纵坐标绘制的图象叫价类图。如图是铁的价类图,写出Y在潮湿的空气中转化为图中同类别物质的化学方程式__ 。

(7)铝制品表面有致密的氧化物薄膜。将一小块铝制品废弃物放入足量的浓NaOH溶液后所发生的氧化还原反应的离子方程式为__ 。
(2)气态氢化物热稳定性HF大于HCl的主要原因是
(3)常温下,一体积的水可以溶解700体积的氨气,原因是
(4)根据现有元素周期律推算,
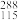 Mc位于元素周期表的第
Mc位于元素周期表的第(5)已知2K2S+K2SO3+3H2SO4=3K2SO4+3S↓+3H2O,若氧化产物比还原产物多8.0g,则转移电子的数目为
(6)以物质的类别为横坐标,化合价为纵坐标绘制的图象叫价类图。如图是铁的价类图,写出Y在潮湿的空气中转化为图中同类别物质的化学方程式

(7)铝制品表面有致密的氧化物薄膜。将一小块铝制品废弃物放入足量的浓NaOH溶液后所发生的氧化还原反应的离子方程式为
您最近一年使用:0次
6 . 下列说法正确的是
| A.二氧化氯泡腾片和75%酒精均可杀灭COVID-19,二者消毒时均表现为强氧化性 |
| B.邻羟基苯甲醛比对羟基苯甲醛熔点、沸点低,主要原因是邻羟基苯甲醛形成分子内氢键 |
| C.硫、白磷、臭氧、C60、氩、水等物质固态时都是分子晶体,分子内都存在共价键 |
| D.石油裂化、煤的气化、苯的硝化、胆矾的风化、蜡烛的熔化等过程中都属于化学变化 |
您最近一年使用:0次
解题方法
7 . 下列说法不正确 的是
| A.在有机化工中,氯气是合成塑料、橡胶、农药和人造纤维的重要原料 |
| B.常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关 |
| C.为了防止月饼等富脂食品氧化变质,延长食品的保质期,常在包装袋中放入生石灰 |
| D.燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施 |
您最近一年使用:0次
解题方法
8 . (1)已知NH3、PH3常温下都是气体,试比较二者沸点高低:NH3______ PH3,并解释原因______
(2)NH4I与PH4I结构相似加热条件下,用化合物PH4I和烧碱反应制取PH3的化学方程式______
(2)NH4I与PH4I结构相似加热条件下,用化合物PH4I和烧碱反应制取PH3的化学方程式
您最近一年使用:0次
9 . (1)用一个离子反应方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱______ 。
(2)冰的密度比水的密度小,能浮在水面上。主要原因是______ 。
(3)用平衡移动原理解释为什么用饱和食盐水除去氯气中的杂质气体
______ 。
 和
和 结合
结合 能力的相对强弱
能力的相对强弱(2)冰的密度比水的密度小,能浮在水面上。主要原因是
(3)用平衡移动原理解释为什么用饱和食盐水除去氯气中的杂质气体

您最近一年使用:0次
解题方法
10 . 羟氨( )可看作氨分子内的一个氢原子被羟基取代的衍生物。下列说法
)可看作氨分子内的一个氢原子被羟基取代的衍生物。下列说法不正确 的是
 )可看作氨分子内的一个氢原子被羟基取代的衍生物。下列说法
)可看作氨分子内的一个氢原子被羟基取代的衍生物。下列说法| A.羟氨易溶于水是由于其与水分子形成分子间氢键 |
| B.羟氨既有氧化性又有还原性 |
| C.羟氨的水溶液显碱性,可与盐酸发生反应 |
D.羟氨分子中 原子、 原子、 原子与羟基 原子与羟基 原子共线 原子共线 |
您最近一年使用:0次



